
【题目】下列溶液中可以盛放在玻璃瓶中,但不能用磨口玻璃塞的是
A. 氯化铝溶液 B. 氢氟酸
C. 氢氧化钠溶液 D. 氯化钠溶液
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在怛容条件下,反应:2SO2 ( g ) + O2 ( g ) ![]() 2SO3( g ) ;△H =-QkJ·mol-1在上述条件下分别充入的气体和反应放出的热量 ( Q>0 )如下表所列:
2SO3( g ) ;△H =-QkJ·mol-1在上述条件下分别充入的气体和反应放出的热量 ( Q>0 )如下表所列:
容 器 | SO2 (mol) | O2(mol) | N2(mol) | Q(kJ·mol-1) |
甲 | 2 | 1 | 0 | Q1 |
乙 | 1 | 0.5 | 0 | Q2 |
丙 | 1 | 0.5 | 1 | Q3 |
根据以上数据,下列叙述正确的是
A. 在上述条件下反应生成 lmolSO3 固体放热 Q/2 kJ B. 2Q3 <2Q2=Q1<Q
C. Ql =2 Q2= 2Q3 = Q D. 2Q2 = 2Q3 < Q1 < Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法正确的是
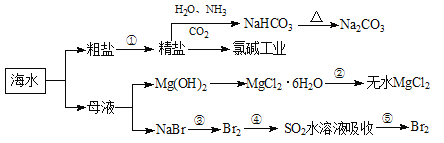
A.第①步中除去粗盐中的SO![]() 、Ca2+、Mg2+、Fe3+等杂质,加入试剂的顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
、Ca2+、Mg2+、Fe3+等杂质,加入试剂的顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.制取NaHCO3的反应是利用其溶解度小于NaCl
C.从第③④⑤步的目的是浓缩、富集溴单质,这三步中溴元素均被氧化
D.过程②中结晶出的MgCl2·6H20可在空气中受热脱水制得无水MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有CO、N2、H2、CO2和少量水蒸气的混合气体,依次通过足量的灼热氧化铜、浓氢氧化钠溶液、浓硫酸后,剩余的气体是
A.N2 B.N2和H2 C.N2和C02 D.H2和CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质氧化性、还原性的强弱,不仅与物质的结构有关,还与浓度和反应温度有关,下列各组物质由于浓度不同而发生不同反应的是:
A. Cu与HNO3 B. Cu与FeCl3 C.Zn与HCl D.FeCl3与NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用烃A(相对分子质量为28)可以合成有价值的高分子F(HO[C4H4O4]nH),合成路线如下:
![]()
(1)请画出A的空间结构____________。
(2)用系统命名法给B、D命名,B____________、D____________。
(3)写出下列变化的反应类型:
A→B____________;
B→C____________;
E→F____________。
(4)写出生成F的化学反应方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)A、B、C、D是原子序数依次增大的短周期主族元素,A、C在元素周期表中的相位置如图,A元素最外层与次外层上的电子数之差为3,B为地壳中含最最多的金属元素。
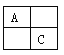
(1)D的离子结构示意图为_____________。
(2)B、C、D形成的简单离子半径由大到小的顺序: > > (写离子符号)
(3)A的最高价氧化物对应的水化物是乙,现将过量Cu加入到60 mL 10.0 mol/L乙的浓溶液中,充分反应,共收集到4.48L(标准状况)气体,则该气体的成分是_________,反应中电子转移数为____________。若使上述中反应后剩余的铜片继续溶解,可向其中加入稀硫酸,写出反应的离子方程式: 。
(4)将两份足量的B单质分别加入到等体积等浓度的硫酸和NaOH溶液中,充分反应生成气体的体积比为__________,若将反应后所得的溶液混合,会生成白色沉淀,发生反应的离子方程式为_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 某反应正、逆反应的活化能分别为EakJ/mol、EbkJ/mol,则△H=-(Ea-Eb)kJ/mol
B. H2的热值为142.9kJ/g,则有2H2 (g)+O2(g)=2H2O (l) △H=-285.8kJ/mol
C. 将浓度为0.1mol/LHF溶液加水不断稀释过程中,  始终保持减小
始终保持减小
D. 混合前![]() ,等体积的混合后溶液中:
,等体积的混合后溶液中: 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。某兴趣小组的实验数值结果大于57.3 kJ·mol-1(中和热),原因可能是

A. 实验装置中小烧杯杯中低于大烧杯杯口
B. 用浓硫酸代替了稀硫酸
C. 分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D. 用温度计测定NaOH溶液起始温度后未洗涤,直接测定H2SO4溶液的温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com