
卫生部发出公告,自2011年5月1日起,禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。下列对于过氧化钙(CaO2)的叙述错误的是( )
A. CaO2具有氧化性,对面粉可能具有增白作用
B. CaO2中阴阳离子的个数比为1:1
C. CaO2和水反应时,每产生1 mol O2转移电子4 mol
D. CaO2和CO2反应的化学方程式为:2CaO2 +2CO2 =2CaCO3+O2
 |
科目:高中化学 来源: 题型:
草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO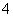 +H2C2O4+H+——Mn2++CO2↑+H2O(未配平)。用4 mL 0.001 mol·L-1KMnO4溶液与2 mL 0.01 mol·L-1H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
+H2C2O4+H+——Mn2++CO2↑+H2O(未配平)。用4 mL 0.001 mol·L-1KMnO4溶液与2 mL 0.01 mol·L-1H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2 | 20 | |
| Ⅱ | 2 | 20 | 10滴饱和MnSO4溶液 |
| Ⅲ | 2 | 30 | |
| Ⅳ | 1 | 20 | 1 mL蒸馏水 |
(1)该反应中氧化剂和还原剂的物质的量之比为________________________________________________________________________。
(2)如果研究催化剂对化学反应速率的影响,使用实验______和______(用Ⅰ~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,使用实验______和______。
(3)对比实 验Ⅰ和Ⅳ,
验Ⅰ和Ⅳ, 可以研究________对化学反应速率的影响,实验Ⅳ中加入1 mL蒸馏水的目的是__________________________________________
可以研究________对化学反应速率的影响,实验Ⅳ中加入1 mL蒸馏水的目的是__________________________________________ ________________________。
________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸铵是一种常用的化肥,其工业生产流程如下图,请回答下列问题。
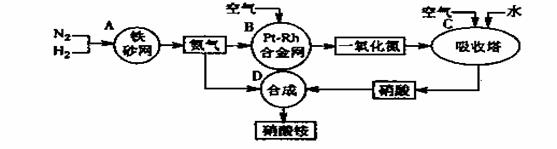
⑴写出反应容器B中发生反应的化学方程式: 。
⑵吸收塔C中通入空气的目的是 ;
A、B、C、D四个反应容器中发生的反应,属于氧化还原反应的是 (填反应容器代号)。
⑶浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因: 。
⑷金属铜与浓硝酸反应的离子方程式是 ,该反应中浓硝酸表现的性质是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H2C2O4 H2O+CO↑+CO2↑ 实验室可以用下图所示装置,设计一个实验,用草酸固体分解,证明该反应生成物中有CO和CO2。回答下列问题:

(1)浓硫酸的作用为 ,应放在 中(填仪器名称)
(2)装置的正确连接顺序为(填接口的代码字母)
(3)能说明生成物中有CO的现象是
(4)能证明生成物中有CO2的现象是
(5) 该套实验装置有什么缺陷,如何改进?
(6) 写出H2C2O4与乙二醇反应的方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式的是( )
A.足量的硫酸铝溶液与纯碱溶液反应: 2A13++3CO32-+3H2O =2A1(OH)3↓+3CO2↑
B. NaHS溶液的水解方程式: HS-+H2O H3O++S2-
H3O++S2-
C. Fe(OH)3与足量的HI溶液反应: Fe(OH)3+3H+=Fe3++3H2O
D.向亚硫酸氢铵溶液中加入足量的NaOH溶液: NH4++OH-=NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D为四种短周期元素,已知A、C同主族,B、C、D同周期;A的气态氢化物比C的气态氢化物稳定;B的阳离子比D的阳离子氧化性强;B的阳离子比C的阴离子少一个电子层。下列叙述正确的是( )
A.原子序数:A>C>B>D B.单质熔点:D>B, A>C
C.原子半径:D>B>C>A D.简单离子半径:D>B>C>A
查看答案和解析>>
科目:高中化学 来源: 题型:
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol· L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60 mL B.45 mL C.30 mL D.15 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
利用低温技术可用于处 理废气中的氮氧化物。在恒容密闭容器中发生下列化学反应:4NH3(g)+5O2(g)
理废气中的氮氧化物。在恒容密闭容器中发生下列化学反应:4NH3(g)+5O2(g)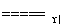 4NO(g)+6H2O(g) ΔH=Q kJ·mol-1(Q<0),有关说法正确的是
4NO(g)+6H2O(g) ΔH=Q kJ·mol-1(Q<0),有关说法正确的是
A.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
B.平衡时,其他条件不变,增加NH3的浓度,废气中NO的转化率减小
C.单位时间内生成NH3和H2O的物质的量比为2∶3时,反应达到平衡
D.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
斯坦福大学B.M. Trost教授提出了绿色化学的核心概念——原子经济性。我们常用原子利用率来衡量化学反应过程的原子经济性,其计算公式为:
原子利用率= ×100%
×100%
下面是新型自来水消毒剂ClO2的四种生产方法,请填空:
(1)氯酸钠和盐酸法:本方法的方程式为2NaClO3+4HCl===2NaCl+2ClO2↑+Cl2↑+2H2O,此方法的原子利用率为________%(保留一位小数,下同)。
(2)电解亚氯酸钠法:本方法是用惰性电极电解亚氯酸钠溶液,原子利用率为62.2%,其阳极电极反应式为:ClO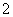 -e-===ClO2,阴极电极反应式为_______________。
-e-===ClO2,阴极电极反应式为_______________。
(3)亚氯酸钠和氯气法:本方法的原子利用率为53.6%,此反应的化学方程式为____________________________________。
(4)联合工艺法:本方法的反应原理由三步组成:
①电解氯化钠溶液NaCl+3H2O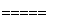 NaClO3+3H2↑
NaClO3+3H2↑
②氢气和氯气合成氯化氢
③生成二氧化氯2NaClO3+4HCl===2NaCl+2ClO2↑+Cl2↑+2H2O此方法的原子利用率最大为________%。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com