
能正确表示下列反应的离子方程式的是( )
A.足量的硫酸铝溶液与纯碱溶液反应: 2A13++3CO32-+3H2O =2A1(OH)3↓+3CO2↑
B. NaHS溶液的水解方程式: HS-+H2O H3O++S2-
H3O++S2-
C. Fe(OH)3与足量的HI溶液反应: Fe(OH)3+3H+=Fe3++3H2O
D.向亚硫酸氢铵溶液中加入足量的NaOH溶液: NH4++OH-=NH3·H2O
科目:高中化学 来源: 题型:
在容积为2 L的密闭容器中,一定条件下发生化学反应:2NO(g)+2CO(g)N2(g)+2CO2(g) ΔH=-746.4 kJ·mol-1。起始反应时NO和CO各为4 mol,10秒钟后达到化学平衡,测得N2为1 mol。下列有关反应速率的说法中,正确的是
A.反应前5秒钟内,用NO表示的平均反应速率为0.1 mol·L-1·s-1
B.达到平衡后,升高温度,正反应速率将减小,逆反应速率将增大
C.达到平衡后,反应速率的关系有:v正(CO)=2v逆(N2)
D.保持容器体积不变,往容器中充入1 mol O2,正、逆反应速率都不改变
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下MO3-与M-发生反应;MO3-+5M-+6H+ == 3M2+3H2O,则下列关于M元素的叙述中正确的是
A.M位于元素周期表的第VA族 B.M的氢化物的水溶液呈酸性
C.MO3-中的M元素只能被还原 D.M2在常温常压下一定是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
葡萄糖在体内富氧条件下被氧化生成二氧化碳和水,在缺氧条件下则生成一种有机酸A。


②将A进行如下图所示的反应,其中C和C′是同系物,C′是甲酸(HCOOH)。
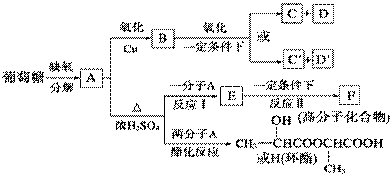
回答下列问题:
(1)C和D′属于_______(填序号,下同)。
①同系物 ②同类物质 ③同分异构体 ④同素异形体
(2) E可以发生的反应类型:_______(填序号,下同)
①消去反应 ②加成反应 ③水解反应 ④取代反应 ⑤氧化反应 ⑥缩聚反应
(3)写出D的分子式和F的结构简式:D____________,F____________,
(4)写出反应类型:(Ⅰ)__________,(Ⅱ)__________
(5)写出下列转化的化学方程式:
A生成H的反应
A与HBr反应
C′与银氨溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
卫生部发出公告,自2011年5月1日起,禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。下列对于过氧化钙(CaO2)的叙述错误的是( )
A. CaO2具有氧化性,对面粉可能具有增白作用
B. CaO2中阴阳离子的个数比为1:1
C. CaO2和水反应时,每产生1 mol O2转移电子4 mol
D. CaO2和CO2反应的化学方程式为:2CaO2 +2CO2 =2CaCO3+O2
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
amolFeS与bmolFe3O4投入到VL cmol/L的硝酸溶液中恰好完全反应,假设只产生NO气体。所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的硝酸为( )
A.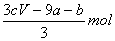 B.(a+3b)mol C.
B.(a+3b)mol C.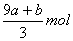 D.(cV-3a-9b)mol
D.(cV-3a-9b)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
某恒容容器内发生的可逆反应的化学平衡常数表达式为:K=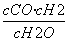 。能判断该反应一定达到化学平衡状态的依据是
。能判断该反应一定达到化学平衡状态的依据是
①容器中气体的平均相对分子质量不随时间而变化 ②v正(H2O)=v逆(H2) ③容器中气体的密度不随时间而变化 ④容器中气体总质量不随时间而变化 ⑤消耗n mol H2的同时消耗n mol CO
A.①②③ B.①②③④
C.② D.①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
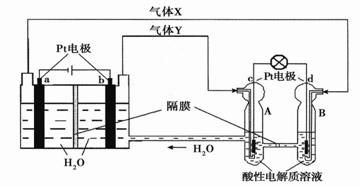
“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如下图所示(部分条件及物质未标出)。
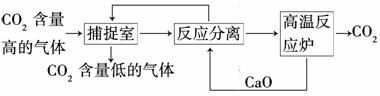
下列有关该方法的叙述中正确的是( )
A.能耗大是该方法的一大缺点
B.整个过程中,只有一种物质可以循环利用
C.“反应分离”环节中,分离物质的基本操作是蒸发结 晶、过滤
晶、过滤
D.该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇等产品
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com