

| 0.735g |
| 0.7500g |


科目:高中化学 来源: 题型:
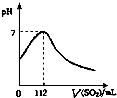 在标准状况下,向100mL氢硫酸溶液中通入二氧化硫气体,溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为( )
在标准状况下,向100mL氢硫酸溶液中通入二氧化硫气体,溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为( )| A、0.5 mol?L─1 |
| B、0.05 mol?L─1 |
| C、1 mol?L─1 |
| D、0.1 mol?L─1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| O | - 4 |
| 实验 编号 | 反应温度 (利用水浴加热) | 稀硫酸溶液 | MnSO4固体 | 0.10mol/LKMnO4溶液 | 褪色时间 |
| 1 | 65℃ | - | - | 1.0mL | 100s |
| 2 | 65℃ | 10滴 | - | 1.0mL | 90s |
| 3 | 75℃ | 10滴 | - | 1.0mL | 40s |
| 4 | 75℃ | 10滴 | 加入少许 | 1.0mL | 3s |
查看答案和解析>>
科目:高中化学 来源: 题型:
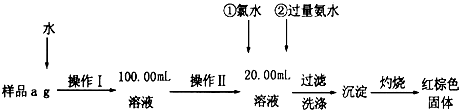
查看答案和解析>>
科目:高中化学 来源: 题型:
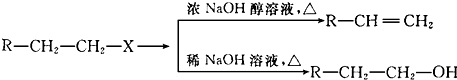
 合成
合成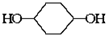 .(部分试剂和反应条件已略去)
.(部分试剂和反应条件已略去)
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
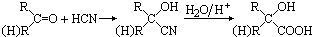 ,CO和H2按物质的量之比1:2可以制得G,有机玻璃可按如图路线合成:
,CO和H2按物质的量之比1:2可以制得G,有机玻璃可按如图路线合成: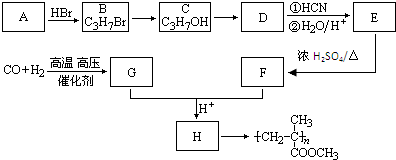
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 原子半径(10-10m) | 1.30 | 0.82 | 0.99 | 1.11 | 0.90 | 1.18 |
| 最高或最低化合价 | +2 | +3 | +7 | +4 | +2 | +3 |
| -1 | -4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、配置浓硫酸的酒精溶液时,要将酒精缓慢注入浓硫酸中,并充分搅拌 |
| B、用pH试纸测量某溶液的酸碱度时,必须先用水润湿pH试纸 |
| C、中和滴定实验中,眼睛要始终注视滴定管中液面的变化 |
| D、实验室做醛的银镜反应时,一般采用水浴加热混合液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com