
 2H2��+O2��
2H2��+O2�� 2H2��+O2��
2H2��+O2�� 2H2��+O2��
2H2��+O2�� CO+3H2
CO+3H2 CH3OH��g��+H2O��g������H="-49.0" kJ/mol,���CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ��
CH3OH��g��+H2O��g������H="-49.0" kJ/mol,���CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ��
 CH3OH��g����ƽ�ⳣ��:
CH3OH��g����ƽ�ⳣ��:| �¶�/�� | 0 | 100 | 200 | 300 | 400 |
| ƽ�ⳣ�� | 667 | 13 | 1.9��1 | 2.4��1 | 1��1 |
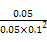 =100,ѡ��C��ȷ;��������Ӧ�Ƿ��ȵ�,��������¶Ȳ����ڷ�Ӧ���ת��,��D��,��ѡAC��
=100,ѡ��C��ȷ;��������Ӧ�Ƿ��ȵ�,��������¶Ȳ����ڷ�Ӧ���ת��,��D��,��ѡAC��

 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO2 (g)+ H2(g) ��H 2 = ?41 kJ/mol����ʼʱ���ܱ������г���1.00 molCO��1.00 molH2O���ֱ��������ʵ�飬̽��Ӱ��ƽ������أ�����������ͬ�Ҳ������κθ���Ӧ��Ӱ�죩��ʵ���������±���
CO2 (g)+ H2(g) ��H 2 = ?41 kJ/mol����ʼʱ���ܱ������г���1.00 molCO��1.00 molH2O���ֱ��������ʵ�飬̽��Ӱ��ƽ������أ�����������ͬ�Ҳ������κθ���Ӧ��Ӱ�죩��ʵ���������±���| ʵ���� | �������/L | �¶�/��C |
| �� | 2.0 | 1200 |
| �� | 2.0 | 1300 |
| �� | 1.0 | 1200 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Q1+Q2+Q3 | B��1.5Q1-0.5Q2+0.5Q3 |
| C��0.5Q1-1.5Q2+0.5Q3 | D��0.5(Q1+Q2+Q3) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 O2(g)=FeO(s)����H����272.0 kJ��mol��1
O2(g)=FeO(s)����H����272.0 kJ��mol��1 O2(g)=Al2O3(s)����H����1675.7 kJ��mol��1
O2(g)=Al2O3(s)����H����1675.7 kJ��mol��1
 Na2S(s)��4H2O(g)
Na2S(s)��4H2O(g)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO2(g)����H1="-393.5" kJ/mol;
CO2(g)����H1="-393.5" kJ/mol; O2(g)
O2(g) H2O(g)����H2="-241.8" kJ/mol;
H2O(g)����H2="-241.8" kJ/mol; O2(g)
O2(g) CO2(g)����H3="-283.0" kJ/mol;
CO2(g)����H3="-283.0" kJ/mol; CO(g)+H2(g)����H=��������,�÷�Ӧƽ�ⳣ���ı���ʽΪK=��������������������;�����¶�,��Kֵ��������(��������С�����䡱)��
CO(g)+H2(g)����H=��������,�÷�Ӧƽ�ⳣ���ı���ʽΪK=��������������������;�����¶�,��Kֵ��������(��������С�����䡱)��  CO2(g)+H2(g),�õ�����2������:
CO2(g)+H2(g),�õ�����2������:| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ���� ��ʱ��/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ���� | �� | �� | CO | H2 |
| ȼ����/(kJ��mol��1) | 1 366 | 5 518 | 283 | 286 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������


 Fe3��(aq)��3OH��(aq) ��H��a kJ/mol
Fe3��(aq)��3OH��(aq) ��H��a kJ/mol H��(aq)��OH��(aq) ��H��b kJ/mol
H��(aq)��OH��(aq) ��H��b kJ/mol�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

 CO(NH2)2(l)��H2O(g)��
CO(NH2)2(l)��H2O(g)��| A�����NH3��Ũ�� | B������ѹǿ |
| C����ʱת�����ɵ����� | D��ʹ�ø���Ч�Ĵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

A����Ӧ����ƽ��״̬ʱ�� |
B����Ӧ�ﵽƽ��� |
| C����ϵ����ѹǿ���䣬˵����Ӧ�Ѵ�ƽ�� |
| D�����������ܶȱ��ֲ��䣬˵����Ӧ�Ѵ�ƽ�� |
 ��
��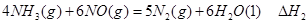 ��
�� ��
�� ��
�� ��
�� ����֮���ϵ�ı���ʽ��
����֮���ϵ�ı���ʽ�� ��_________��
��_________��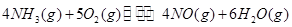
 ��
��


| ʱ��/Ũ�� |   |   |   |   |
| ��ʼ | 4.0 | 5.5 | 0 | 0 |
| ��2min | 3.2 | a | 0.8 | 1.2 |
| ��4min | 2.0 | 3.0 | 2.0 | 3.0 |
| ��6min | 2.0 | 3.0 | 2.0 | 3.0 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com