
I 铁及其化合物之间的相互转化可用下式表示:
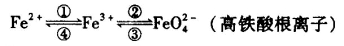
回答下列有关问题:
(1)检验硫酸铁溶液中是否存在Fe2+的方法是___________________。
(2)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2 = 2Na2FeO4+2Na2O+2Na2SO4+O2↑
该反应中的还原剂是___________,每生成l mol Na2FeO4转移____________mol电子。
(3)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:
Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:_______________。
②若反应过程中转移了0.3 mol电子,则还原产物的物质的量为___________。
II某化学小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备 。已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。
。已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。
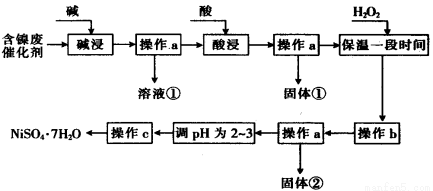
部分阳离子以氢氧化物形式沉淀时的pH如下:

(1)“碱浸”过程中发生反应的离子方程式是
(2)“酸浸”时所加入的酸是 (填化学式)。
(3)加入H2O2时发生反应的离子方程式为
(4)操作b为调节溶液的pH,你认为pH的调控范围是
(5)NiS04·7Hz0可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型。NiMH中的M表示储氢金属或合金。该电池在充电过程中总反应的化学方程式是Ni(OH)2+M=NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为 。
科目:高中化学 来源:2016届福建省、霞浦七中、周宁十中高三上期中联考化学试卷(解析版) 题型:选择题
下列各组在溶液中的反应,不管反应物量的多少,都只能用同一个离子方程式来表示的是
A.FeBr2与Cl2
B. HCl与Na2CO3
C.Ba(OH) 2与H2SO4
D.Ca(HCO3) 2与NaOH
查看答案和解析>>
科目:高中化学 来源:2016届山东省威海市乳山市高三上学期期中测试化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z在元素周期表中的相对位置如图,下列推论合理的是
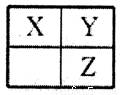
A.若Z的核电荷数是Y的两倍,则X为碳元素
B.若X、Y、Z的单质常温下都是气体,则Y为氧元素
C.若X、Y、Z都是非金属元素,则它们气态氢化物的水溶液都显酸性
D.若X、Y、Z的原子序数之和等于25,则它们都是非金属元素
查看答案和解析>>
科目:高中化学 来源:2016届北京市海淀区高三上学期期中测试化学试卷(解析版) 题型:填空题
亚氯酸钠(NaClO2)是一种高效氧化剂和优质漂白剂。一种以氯酸钠(NaClO3)为原料制备NaClO2 粗品的工艺流程如下图所示:
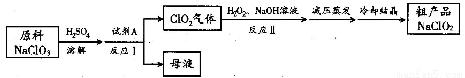
已知:
①纯ClO2 易分解爆炸,空气中ClO2 的体积分数在10%以下比较安全;
②NaClO2 在碱性溶液中稳定存在,在酸性溶液中迅速分解;
③含水NaClO2 受热易分解。
(1) 试剂A 可以选择___________(填字母序号)。
a. SO2 b. 浓硝酸 c. KMnO4
(2) 反应Ⅱ的离子方程式为_________。
(3) 下列关于上述流程的说法中,合理的是________(填字母序号)。
a. 反应Ⅰ进行过程中应持续鼓入空气
b. 反应Ⅰ后得到的母液中,溶质的主要成分是NaCl
c. 反应Ⅱ中NaOH 应过量
(4) 已知压强越大,物质的沸点越高。反应Ⅱ结束后采用“减压蒸发”操作的原因是____________。
(5) 中间产物二氧化氯(ClO2)在生产生活中也有广泛应用。用ClO2 处理泄漏的氰化钠(NaCN),得到无毒的NaCl、N2 和CO2。若处理含NaCN4×10-5mol ·L-1的废水 1000L,至少需要ClO2 的质量为___________g。
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期半期考试化学试卷(解析版) 题型:选择题
下列反应原理不符合工业冶炼金属实际情况的是
A. 2HgO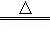 2Hg+O2↑
2Hg+O2↑
B. 2NaCl(熔融) 2Na+Cl2↑
2Na+Cl2↑
C. 2MgO(熔融)  2Mg+O2↑
2Mg+O2↑
D. Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
查看答案和解析>>
科目:高中化学 来源:2016届四川省巴中市普通高中高三10月诊断性测试理综化学试卷(解析版) 题型:实验题
实验室用乙醇和必要的无机试剂制取1,2-二溴乙烷的装置如下图,1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18g/cm,3沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。请回答以下问题:
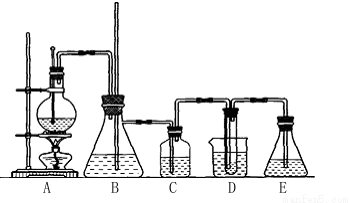
(1)装置A的烧瓶中装入乙醇和浓硫酸的混合液后还需加入 。
烧瓶内发生的反应的化学方程式为 。
(2)装置B的作用是 。
(3)装置C中盛有10%的NaOH溶液,其作用是 。
(4)装置D中试管中装有液溴,实验开始后观察到的主要现象是 。
(5)开始反应时需向装置D中的烧杯里加入冰水,这是为了 。
(6)装置E的作用 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江哈尔滨附属中学高二上期中化学试卷(解析版) 题型:选择题
已知下列热化 学方程式:C(s)+O2(g) = CO2(g) ΔH=-393.5 kJ·mol-1
学方程式:C(s)+O2(g) = CO2(g) ΔH=-393.5 kJ·mol-1
2H2(g)+O2(g) = 2H2O(g) ΔH=-483.6 kJ·mol-1
现有0.2 mol的炭粉和氢气组成的气、固混合物在氧气中完全燃烧,共放出63.53 kJ热量,则炭粉与氢气的物质的量之比为
A.1:1 B.1:2 C.2:3 D.3:2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一上11月月考化学试卷(解析版) 题型:选择题
下列仪器常用于物质分离的是
①漏斗 ②试管 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥研钵
A.①③④ B.①②⑥ C.①③⑤ D.①③⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏银川市高一上学期期中测试化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法正确的是
A.48克O2和O3的混合物含有氧原子数3NA
B.22.4L甲烷(CH4)所含的原子数为5NA
C.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA
D.在20℃,1.01×105Pa(即在标准状况)时,11.2L氧气所含的原子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com