
【题目】塑化剂主要用作塑料的增塑剂,也可作为农药载体、驱虫剂和化妆品等的原料.添加塑化剂(DBP)可改善白酒等饮料的口感,但超过规定的限量会对人体产生伤害.其合成线路图如图I所示:
已知以下信息:① ![]()
② ![]() (-R1、R2表示氢原子或烃基)
(-R1、R2表示氢原子或烃基)
③C为含两个碳原子的烃的含氧衍生物,其核磁共振氢谱图如图Ⅱ所示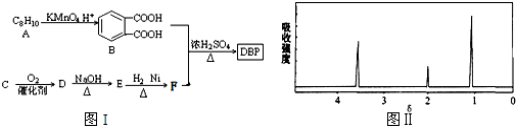
(1)C的结构简式为 , E中所含官能团的名称是;
(2)写出下列有关反应的化学方程式:
①E和H2以物质的量比1:1反应生成F:;
②B和F以物质的量比1:2合成DBP:;该反应的反应类型为;
(3)同时符合下列条件的B的同分异构体有种,写出其中任意两种同分异构体的结构简式。
①不能和NaHCO3溶液反应
②能发生银镜反应
③遇FeCl3溶液显紫色
④核磁共振氢谱显示苯环上只有一种氢原子
【答案】
(1)CH3CH2OH;碳碳双键和醛基
(2)CH3CH=CHCHO+H2 ![]() CH3CH=CHCH2OH;
CH3CH=CHCH2OH; ![]() ;取代反应(或酯化反应)
;取代反应(或酯化反应)
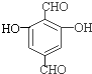
(3)6;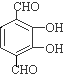 、
、 
【解析】A反应生成邻苯二甲酸,结合信息①可知A为 ![]() ,C为含两个碳原子的烃的含氧衍生物,由核磁共振氢谱可知含有3种H原子,结合信息②可知D含有醛基,则C为CH3CH2OH、D为CH3CHO,E为CH3CH2=CHCHO,E和H2以物质的量比1:1反应生成F,B和F以物质的量比1:2合成DBP,合成DBP为酯化反应,则F为CH3CH2=CHCH2OH,DBP为
,C为含两个碳原子的烃的含氧衍生物,由核磁共振氢谱可知含有3种H原子,结合信息②可知D含有醛基,则C为CH3CH2OH、D为CH3CHO,E为CH3CH2=CHCHO,E和H2以物质的量比1:1反应生成F,B和F以物质的量比1:2合成DBP,合成DBP为酯化反应,则F为CH3CH2=CHCH2OH,DBP为 ![]() 。
。
(1)C的结构简式为CH3CH2OH,E为CH3CH2=CHCHO,含有碳碳双键、醛基,
所以答案是:CH3CH2OH;碳碳双键、醛基;
(2)①E和H2以物质的量比1:1反应生成F的方程式为:CH3CH=CHCHO+H2 ![]() CH3CH=CHCH2OH;
CH3CH=CHCH2OH;
所以答案是:CH3CH=CHCHO+H2 ![]() CH3CH=CHCH2OH;
CH3CH=CHCH2OH;
②B和F以物质的量比1:2合成DBP的方程式为: ![]() +2CH3CH2=CHCH2OH
+2CH3CH2=CHCH2OH ![]()
![]() +2H2O,属于取代反应,
+2H2O,属于取代反应,
所以答案是: ![]() +2CH3CH2=CHCH2OH
+2CH3CH2=CHCH2OH ![]()
![]() +2H2O,取代反应;
+2H2O,取代反应;
(3)同时符合下列条件的B( ![]() )的同分异构体:①不能和NaHCO3溶液反应,不含羧基;②能发生银镜反应,含有醛基③遇FeC13溶液显紫色,含有酚羟基;④核磁共振氢谱显示苯环上只有一种氢原子,符合条件的同分异构体有:
)的同分异构体:①不能和NaHCO3溶液反应,不含羧基;②能发生银镜反应,含有醛基③遇FeC13溶液显紫色,含有酚羟基;④核磁共振氢谱显示苯环上只有一种氢原子,符合条件的同分异构体有:  、
、  、
、 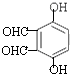 、
、 ![]() 、
、 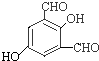 、
、 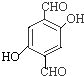 ,所以答案是6;
,所以答案是6;  、
、  、
、  、
、 ![]() 、
、  、
、  (任写两种即可)。
(任写两种即可)。


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】用FeCl3溶液腐蚀印刷电路板上铜箔的反应是:2Fe3++Cu=2Fe2++ Cu2+。下列有关说法错误的是
A.Cu是还原剂,被腐蚀B.FeCl3是氧化剂
C.该反应是置换反应D.该反应属于离子反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关阿伏伽德罗常数的值的说法正确的是
A.等于6.02×1023
B.0.012kg12C所含的原子数
C.1mol氯气所含的微粒数
D.是物质的量的单位
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。 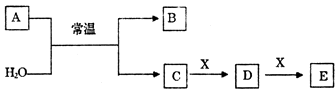
(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式: .
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则:
①组成单质A的元素在周期表中的位置为 .
②X可能为(填代号).
a.NaHCO3 b.Na2CO3 c.Na2SO3 d.Al(OH)3
(3)若A为淡黄色粉末,回答下列问题:
①1molA与足量的H2O充分反应时转移的电子数目为 .
②A的电子式为。
③若X为一种造成温室效应的气体.则鉴别等浓度的D、E两种溶液,可选择的试剂为(填代号).
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红.
则A与H2O反应的化学反应方程式为 . E是(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】异丙苯是一种重要的有机化工原料.异丙苯的结构简式为 ![]() .
.
(1)异丙苯中至少有个碳原子共平面.
(2)异丙苯有多种同分异构体,其中一溴代物只有两种的芳香烃是(填结构简式).
(3)由异丙苯制备对溴异丙苯的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与应用的说法正确的是( )
A.甲醇可以使蛋白质变性,常用于食品保鲜
B.氧化铝熔点高,常用子制造耐火材枓
C.氧化钠可用作呼吸面具中的供氧剂
D.常温下,可用铁槽车或铝槽车运输稀硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释实验事实的离子方程式正确的是( )
A.纯碱溶液显碱性的原因:CO32﹣+2H2O ![]() H2CO3+2OH﹣
H2CO3+2OH﹣
B.氯化铁溶液腐蚀铜线路板Cu+Fe3+=Cu2++Fe2+
C.稀硫酸与氢氧化钡溶液恰好中和:Ba2++OH﹣+H++SO42﹣=BaSO4↓+H2O
D.氯气溶于水:Cl2+H2O=H++Cl﹣+HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组测定某过氧化氢溶液中过氧化氢的浓度,进行如下实验:取20.00mL的该过氧化氢溶液加水稀释至250.00mL,取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式为:2MnO ![]() +5H2O2+6H+═2Mn2++8H2O+5O2↑.据此作答:
+5H2O2+6H+═2Mn2++8H2O+5O2↑.据此作答:
(1)滴定时,将高锰酸钾标准溶液注入(填“酸式”或“碱式”)滴定管中;滴定到达终点的现象是: .
(2)配置标准溶液时使用的KMnO4固体中如果含有少量K2SO4杂质,则对测定结果的影响是 . (填“偏大”、“偏小”或“不变”)
(3)重复滴定四次,分别耗用c mol/LKMnO4标准溶液的体积为:0.99V mL、1.03V mL、1.28VmL、0.98V mL,则原过氧化氢溶液中的物质的量浓度为molL﹣1 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com