
【题目】以甲醛和苯酚为主要原料,经如图所示系列转化可合成酚醛树脂和重要有机合成 中间体 D(部分反应条件和产物略去):

(1)CH3OH 的名称为_____。
(2)C 中所含官能团的名称是_____。
(3)反应②的化学方程式是_____。
(4)下列关于 A 的性质,能反映支链对苯环结构产生影响的是_____(填字母)。
a.能与氢氧化钠溶液反应 b.能使酸性高锰酸钾溶液褪色 c.稀溶液中加浓溴水产生沉淀
(5)E(C8H10O2)与 B 的水解产物互为同分异构体,1 mol E 可与 2 mol NaOH 反应,其核磁共振氢谱显示有 3 种峰且峰面积之比为 3∶1∶1,符合条件的 E 共有_____种。
(6) 完成下面以 CH3OH 和 CH3ONa 为 原 料 ( 其 他 无 机 试 剂 任 选 ) 制 备 化 合 物CH3COCH2COOCH3 的合成路线。 CH3OH――△→… ___________________________________________
【答案】甲醇 酯基、醚键 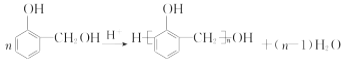 c 4
c 4 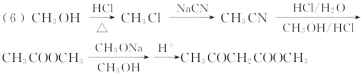
【解析】
根据合成路线流程图,反应①中苯酚与甲醛反应生成A(C7H8O2),该反应属于加成反应,根据酚醛树脂的结构可知A为![]() ,其他物质根据所给结构及已知条件对物质的反应进行分析解答。
,其他物质根据所给结构及已知条件对物质的反应进行分析解答。
(1) CH3OH的名称为甲醇;
(2) C是对甲氧基苯乙酸甲酯,所含官能团有酯基、醚键;
(3) 反应②为![]() 发生缩聚反应生成
发生缩聚反应生成![]() 的反应,反应的方程式为
的反应,反应的方程式为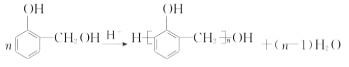 ;
;
(4) A为![]() 。a.分子中含有酚羟基,能与氢氧化钠溶液反应,与苯环上的支链无关,故a不选;b. 分子中含有酚羟基,能被酸性高锰酸钾溶液氧化为粉红色的物质,与苯环上的支链无关,故b不选;c.稀溶液中加浓溴水产生沉淀,与苯环上的羟基有关,故c选,故选c;
。a.分子中含有酚羟基,能与氢氧化钠溶液反应,与苯环上的支链无关,故a不选;b. 分子中含有酚羟基,能被酸性高锰酸钾溶液氧化为粉红色的物质,与苯环上的支链无关,故b不选;c.稀溶液中加浓溴水产生沉淀,与苯环上的羟基有关,故c选,故选c;
(5) 1molE(C8H10O2)可与2molNaOH反应,说明含有2mol羟基,其核磁共振氢谱显示有3种峰且峰面积之比为3:1:1,符合条件的E有![]() 、
、![]() 、
、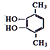 、
、![]() ,共4种;
,共4种;
(6)以CH3OH为原料制备化合物CH3COCH2COOCH3。根据题干中B到D的转化过程,可以首先将CH3OH转化为CH3Cl,再转化为CH3CN,水解为乙酸甲酯,最后根据题干信息转化即可。合成路线为![]() 。
。


 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
【题目】规范的实验操作是实验安全的基础,下列实验操作合理的是
A. 给试管中的固体加热时,试管口斜向上45度,且不能对着人
B. 用氢气还原氧化铜时,先通一会儿氢气,然后再点燃酒精灯加热
C. 实验结束,将废液倒入下水道排出实验室,以免污染实验室
D. 用燃着的酒精灯去点燃另一盏酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列实验现象解释正确的是
实验内容 | 实验现象 | 相关解释 | |
A | 等量的Cu分别与等体积足量的浓硝酸和稀硝酸反应 | 浓硝酸反应后呈绿色,稀硝酸反应后呈蓝色 | c(Cu2+)不同 |
B | NH3与Cl2混合 | 生成白烟 | NH3与Cl2发生化合反应生成NH4Cl |
C | 往Fe(OH)3胶体中逐滴滴入稀盐酸 | 先出现红褐色沉淀,后沉淀溶解 | 先胶体聚沉,后Fe(OH)3溶解 |
D | 加热硝酸铜固体,将带火星的木条伸入所得的气体中 | 生成红棕色气体,带火星木条复燃 | 2Cu(NO3)2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和热的测定是高中重要的定量实验。取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:
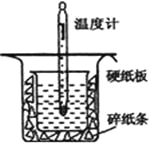
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是_________,除此之外,装置中的一个明显错误是 ______________________。
(2)若改用60mL 0.25mol·L-1 H2SO4和50mL 0.55mol·L-1NaOH溶液进行反应与上述实验相比,所放出的热量_________________(填“相等”、“不相等”),若实验操作均正确,则所求中和热_________________(填“相等”“不相等”)。
(3)实验数据如下表:
①请填写下表中的空白:
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | ___________ |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热ΔH=__________ ( 取小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,将3 mol A气体和1 mol B气体混合于固定容积为2 L的密闭容器中,发生反应:3A(g)+B(g) ![]() C(g)+2D(s)。2 min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是( )
C(g)+2D(s)。2 min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是( )

A. 若混合气体的密度不再改变时,该反应不一定达到平衡状态
B. 2 min后,加压会使正反应速率加快,逆反应速率变慢
C. 反应过程中A和B的转化率之比为3∶1
D. 开始到平衡,用A表示的化学反应速率为0.3 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生石灰遇水生成熟石灰,下列对此反应过程中化学键变化的判断正确的是
A.断裂离子键和共价键,形成离子键和共价键B.只断裂离子键,形成离子键和共价键
C.只断裂共价键,形成共价键D.离子键和共价键在反应前后没有变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO(g)与H2O(g)反应的能量变化如图所示,有关两者反应的说法正确的是( )

A. 该反应为吸热反应
B. 该反应不需要加热就能进行
C. 1 molCO(g)和1mol H2O(g)具有的总能量大于1 molCO2(g)和1 molH2(g)具有的总能量
D. 1 molCO2(g)和1 molH2(g)反应生成1 molCO(g)和1mol H2O(g)要放出41 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、生产密切相关,下列说法错误的是 ( )
A. Ge(32号元素)的单晶可以作为光电转换材料用于太阳能电池
B. 工业生产玻璃、水泥,均需要用石灰石为原料
C. 将二氧化硫添加于红酒中可以起到杀菌和抗氧化作用
D. 纳米铁粉和FeS都可以高效地去除被污染水体中的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其原理是相同的。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com