
| 23.4g |
| 0.5mol |
| 86.4g |
| 108g/mol |
| 23.4g |
| 0.5mol |
| 86.4g |
| 108g/mol |
| 5.8g |
| 0.1mol |
| 17.4g |
| 0.3mol |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、AgNO3 |
| B、CuSO4 |
| C、Na2CO3 |
| D、MgSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ | ||
B、金属铝溶于氢氧化钠溶液:Al+2OH-=AlO
| ||
| C、金属铝溶于盐酸中:2Al+6H+=2Al3++3H2↑ | ||
| D、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化物:CO2 NO SO2 H2O |
| B、碱:NaOH KOH Ba(OH)2 Na2CO3 |
| C、铵盐:NH4Cl NH4NO3 (NH4)2SO4 NH3?H2O |
| D、酸:NaHSO3 HCl H2SO4 HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓烟主要是由生成的大量NH4Cl造成的 |
| B、以上物质的水解都生成对应的酸和碱 |
| C、CCl4和SiCl4的分子结构相似,故CCl4也容易发生水解 |
| D、NH3属于弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
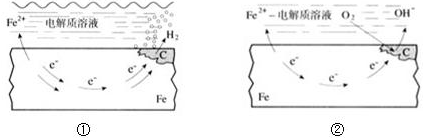
| A、碳表面发生氧化反应 |
| B、钢铁被腐蚀的最终产物为FeO |
| C、生活中钢铁制品的腐蚀以图①所示为主 |
| D、图②中,正极反应式为O2+4e-+2H2O═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
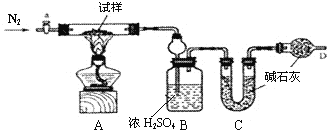
| 序号 | a | b | c | d | E |
| 数据 | m1、m2、m3 | m2、m3、m4、m5 | m1、m2、m4 | m1、m4、m5 | m1、m3、m5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com