
【题目】下列物质间的转化过程,属于氧化反应的是( )
A.Mg→MgO
B.CaO→CaCO3
C.Cl2→NaCl
D.H2SO4→SO2
科目:高中化学 来源: 题型:
【题目】CuSO4是一种重要的化工原料,有关制备途径及性质如下图所示。下列说法错误的是( )

A.途径①所用混酸中H2SO4与HNO3的最佳物质的量之比为3:2
B.与途径①、③相比,途径②更好地体现了绿色化学思想
C.生成等量的硫酸铜,三个途径中参加反应的硫酸的物质的量①=②<③
D.利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年冬季,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
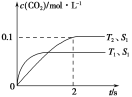
据此判断:
①该反应的ΔH________0(填“>”或“<”)。
②在T2温度下,0~2 s内的平均反应速率v(N2)________。
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。
④若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________(填代号)。
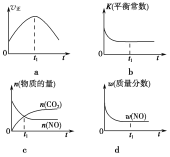
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
例如:
CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g) ΔH1=-867 kJ/mol
2NO2(g) ![]() N2O4(g) ΔH2=-56.9 kJ/mol
N2O4(g) ΔH2=-56.9 kJ/mol
写出CH4(g)催化还原N2O4(g)生成N2(g)和H2O(g)的热化学方程式:_______________________
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。催化剂b表面发生的电极反应式为__________________________。
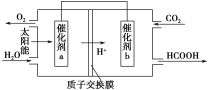
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.某试样焰色反应呈黄色,则试样中可能含有K+
B.广泛pH试纸测得某新制氯水的pH为4
C.配制240mL某溶液,应选240mL容量瓶
D.可用排饱和食盐水来收集纯净的氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 用![]() 表示原子:
表示原子:
(1)中性原子的中子数N=_______________。
(2)AXn+共有x个电子,则该阳离子的中子数N=___________。
(3)AXn-共有x个电子,则该阴离子的中子数 N=___________。
(4)12C16O2分子中的中子数N=______________。
II. 将Zn棒和Cu棒用导线连接后,放入硫酸铜溶液中,构成如图所示装置。回答下列问题:
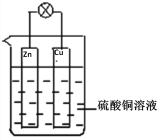
(1)Zn棒为原电池的_____极,其电极反应式为________________________;
(2)Cu棒为原电池的_____极,电极反应式为________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:

已知:(1)铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(2)溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学反应方程式为2Na2SiO3+2NaAlO2+2H2O=Na2A12Si2O8↓+4NaOH。请回答下列问题:
(1)铝土矿中Al2O3与氢氧化钠溶液反应的离子方程式为_________________________________。
(2)在工艺流程中“酸化”时,加入的最佳物质B是________,理由是_______________________,写出酸化过程发生反应的化学方程式:________________________________。
(3)工业上用Al2O3与C、Cl2在高温条件下反应制取AlCl3,理论上每消耗6.0 g碳单质,转移1 mol电子,则反应的化学方程式为__________________________________。
(4)某同学推测铝与氧化铁发生铝热反应得到的熔融物中还含有Fe2O3,设计了如下方案来验证:取一块该熔融物投入少量稀硫酸中,反应一段时间后,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有Fe2O3。
则物质甲是_________(填化学式),请判断该同学设计的实验方案的合理性_________(填“合理”或“不合理”)。原因是_______________________________________(若合理,则不用填写)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】EHPB是合成治疗高血压和充血性心力衰竭的药物的中间体,合成路线如下:
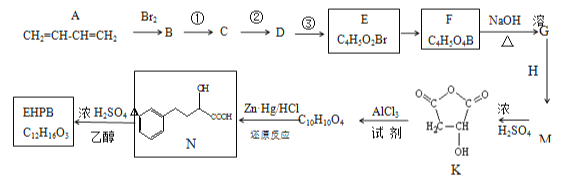
已知:ⅰ.碳碳双键容易被氧化
ⅱ. ![]()
(1)A的名称为______,E中含氧官能团的名称为_______。
(2)E由B经①、②、③合成。
a.①的反应试剂和条件是__。 b.③ 的反应类型是______。
(3)M的结构简式为__________。
(4)EHPB不能与NaHCO3反应,写出有机物N→EHPB的化学方程式为_____________。
(5)有机物N有多种同分异构体,其中能满足下列条件的同分异构体有_________种。
a.含有酚羟基 b.能发生水解反应且能发生银镜反应c.苯环上的一氯代物只有一种 d.核磁共振氢谱有5组峰
(6)请写出由苯和乙二醇制取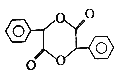 的转化过程________,无机试剂任选。
的转化过程________,无机试剂任选。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是
A. 铁与盐酸反应:2Fe+6H+=2Fe3++3H2↑
B. 过氧化钠与反应:2O22-+2H2O=4OH-+O2↑
C. 碳酸氢钠与稀盐酸反应:CO32-+2H+=CO2↑+ H2O
D. 氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH-=Fe(OH)3↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com