
【题目】下列各组混合物中,能用分液漏斗进行分离的是( )
A.碘和四氯化碳B.水和四氯化碳
C.酒精和水D.汽油和植物油
科目:高中化学 来源: 题型:
【题目】等电子原理:原子数相同、最外层电子总数相同的分子互称为等电子体。等电子体的结构、物理性质均相似。
(1)根据以上原理,仅由第二周期元素组成的共价化合物分子中,互为等电子体的是__________和__________;________和________。
(2)此后,等电子原理又有发展。例如:由短周期元素组成的粒子,只要其原子总数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与NO![]() 互为等电子体的分子有:_________(写出一种即可)。
互为等电子体的分子有:_________(写出一种即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄红色液体二氯化二硫可以作为贵稀金属的萃取剂,由硫与氯气再50℃~60℃直接化合而成。装置图如下:

(1)二氯化二硫遇水会反应,生成硫、二氧化硫和刺鼻的酸雾,其化学方程式为______。
(2)A装置中所盛试剂为__________。
(3)操作过程中:
①先通入N2,理由是_________________。
②通入少量Cl2后,装置B采用________(填“水浴”或“油浴”)加热1h。
③停止加热,加大通入氯气量,维持16h。制备二氯化二硫为______(填“放热”或“吸热”)反应。
(4)二氯化二硫的电子式为______________。
(5)装置C的作用是__________,同时制得有价值的工业产品为___________。
(6)为了得到更纯净的二硫化二氯,需要在装置B、C之间安装干燥管,其内盛试剂为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
磷及其化合物是生活生产中重要的组成部分,以下是一些常见的磷的化合物:
(1)与磷同主族、比磷多一个周期的元素基态原子的价层电子排布为___________.
(2)磷与同周期相邻的两种元素的第一电离能由大到小的顺序为__________。(用元素符号表示)。
(3)亚磷酸(H3PO3)是一种常见的无机酸,其与过量的NaOH溶液反应生成Na2HPO3,请画出亚磷酸的分子结构_______。亚磷酸可作还原剂将Cu2+还原为单质,得到的电子填充到________轨道。
(4)己知PBr5晶体中存在PBr4+,和Br-两种离子,则PBr4+,中心P原子杂化类型为___,该离子的几何构型为______。而PCl5晶体中存在PCl4+和另一种阴离子,该阴离子配位数为6,请写出该离子的化学式:______。PBr5晶体中不能形成与PCl5晶体一样的阴离子的原因可能是:_________。
(5)铝和白磷在一定条件下可以制备磷化铝(AlP),磷化铝晶胞的结构如图,可以将其看做Si晶体的“广义等电子体”,可做半导体材料.
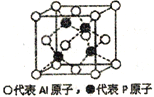
①根据“广义等电子原理”,下列物质中,可能是半导体的有____________.
A. SiC B.CaO2 C. GaAs D.Si3N4 E.BN
②磷化铝中,Al原子的配位数为_______,若该晶胞密度为dg/cm3,用NA表示阿伏伽德罗常数,则该晶体的边长为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期主族元素,原子序数由A到E逐渐增大。①A元素最外层电子数是次外层电子数的2倍。 ②B的阴离子和C的阳离子与氖原子的电子层结构相同。③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移。④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体,此淡黄色固体能与AB2反应可生成B的单质。⑤D的气态氢化物与其最高价含氧酸间能发生氧化还原反应。请写出:
(1)A元素的最高价氧化物的电子式_____________。
(2)B元素在周期表中的位置_____________。
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有 ______________ 。
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为______________。
(5)C与D能形成2:1的化合物,用电子式表示该化合物的形成过程的______________。
(6)元素D与元素E相比,能证明这两种元素非金属性谁更强的事实是___________(填选项序号)。
a.常温下D的单质和E的单质状态不同
b.E的氢化物比D的氢化物稳定
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列行为中符合安全要求的是( )
A.进入煤矿井时,用火把照明
B.实验时,将水倒入浓硫酸配制稀硫酸
C.用点燃的火柴在液化气钢瓶口检验是否漏气
D.节日期间,在开阔的广场燃放烟花爆竹
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是用实验室制得的乙烯(C2H5OH![]() CH2=CH2↑+H2O)与溴水作用制取1,2﹣二溴乙烷的部分装置图,根据图示判断下列说法正确的是
CH2=CH2↑+H2O)与溴水作用制取1,2﹣二溴乙烷的部分装置图,根据图示判断下列说法正确的是

A. 装置①和装置③中都盛有水,其作用相同
B. 装置②和装置④中都盛有NaOH溶液,其吸收的杂质相同
C. 产物可用分液的方法进行分离,1,2﹣二溴乙烷应从分液漏斗的上口倒出
D. 制备乙烯和生成1,2﹣二溴乙烷的反应类型分别是消去反应和加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是
A. 2 mol水的摩尔质量和1 mol水的摩尔质量
B. 200 mL 1 mol·L-1氯化钙溶液中c(Cl-)和100 mL 2 mol·L-1氯化钾溶液中c(Cl-)
C. 标准状况下,22.4 L一氧化碳中氧原子数和16 g二氧化硫中氧原子数
D. 2 mol·L-1H2SO4溶液中的H+个数与1 mol·L-1HCl溶液中的H+个数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】V L浓度为1.000 mol·L-1的盐酸,欲使其浓度增大1倍,采取的措施合理的是
A. 向原溶液中通入常温常压下的HCl气体22.4V L,使其完全溶解
B. 将溶液加热浓缩到0.5V L
C. 向原溶液中加入10.00 mol·L-1的盐酸0.2V L,再稀释至1.5V L
D. 向原溶液中加入V L 3 mol·L-1的盐酸混合均匀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com