
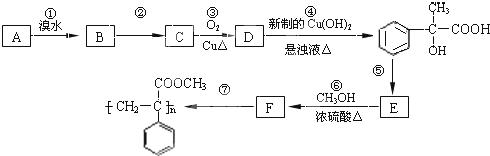
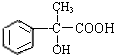
 的分子式
的分子式 ,则C为
,则C为 ,故A为
,故A为 ,B为
,B为 ,反应⑤为消去反应,则E为
,反应⑤为消去反应,则E为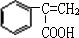 ,E与据此发生在酯化反应生产F为
,E与据此发生在酯化反应生产F为 ,F发生加聚反应生成高聚物,据此解答.
,F发生加聚反应生成高聚物,据此解答. ,则C为
,则C为 ,故A为
,故A为 ,B为
,B为 ,反应⑤为消去反应,则E为
,反应⑤为消去反应,则E为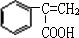 ,E与据此发生在酯化反应生产F为
,E与据此发生在酯化反应生产F为 ,F发生加聚反应生成高聚物,
,F发生加聚反应生成高聚物, 的分子式为C9H10O3,含有羧基、羟基,可以发生水解反应,消去反应,不能发生加聚反应、水解反应,故答案为:C9H10O3;BD;
的分子式为C9H10O3,含有羧基、羟基,可以发生水解反应,消去反应,不能发生加聚反应、水解反应,故答案为:C9H10O3;BD; ,F结构简式为
,F结构简式为 ,故答案为:
,故答案为: ;
; ;
; +O2
+O2| Cu |
| △ |
 +2H2O,
+2H2O, +O2
+O2| Cu |
| △ |
 +2H2O;
+2H2O;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、食盐水、糖水和冰水都是饮料,属于混合物 |
| B、某物质只含有一种元素,则该物质一定是单质 |
| C、烧碱属于碱,纯碱属于盐 |
| D、CuSO4?5H2O是一种混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
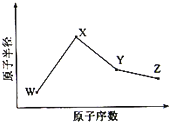
| 元素编号 | 元素性质或原子结构 |
| W | 原子电子层数与核外电子数相等 |
| X | 原子核外L层上s能级的电子总数为p能级上的电子总数的一半 |
| Y | 元素的原子半径在短周期中最大(除稀有气体外) |
| Z | 原子核外p能级上的电子总数等于s能级上的电子总数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
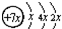 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com