
【题目】某兴趣小组为研究乙酸乙酯的制取,进行如下实验。
[实验一]用乙醇和乙酸制取乙酸乙酯
甲、乙同学分别使用图1、图2装置制取乙酸乙酯。

(1)甲同学在制得乙酸乙酯后,将乙酸乙酯与饱和碳酸钠溶液分离的仪器是___。
(2)制取乙酸乙酯的化学方程式为__。
(3)图1导管末端不能插入饱和碳酸钠溶液,而图2装置中的仪器C的末端可以插入饱和碳酸钠溶液的原因是__。
[实验二]现欲分离乙酸乙酯、乙酸、乙醇的混合物,如图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法,在方框内填入所分离的有关物质的名称:

(4)写出各有关物质的名称:A__,E__。
(5)写出加入的试剂:a___,b___。
(6)写出有关的操作方法:①___,②___,③__。
【答案】分液漏斗 CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O 仪器C上方有一较大容积的空间,液体不会倒流到A 乙酸乙酯 乙酸 饱和碳酸钠 稀硫酸 分液 蒸馏 蒸馏
CH3COOCH2CH3+H2O 仪器C上方有一较大容积的空间,液体不会倒流到A 乙酸乙酯 乙酸 饱和碳酸钠 稀硫酸 分液 蒸馏 蒸馏
【解析】
往乙醇中加入浓硫酸,再加入乙酸,配制反应液,在大试管或圆底烧瓶内加热制取乙酸乙酯,由于乙酸、乙醇易挥发,所以乙酸乙酯中混有乙酸和乙醇,可利用饱和Na2CO3溶液去除乙酸、溶解乙醇、降低乙酸乙酯的溶解度,但同时注意防止倒吸。
若想分离反应生成的混合液中的三种物质,可先利用饱和碳酸钠溶液分离出乙酸乙酯中的乙酸和乙醇,再蒸馏分离所得的乙酸钠与乙醇的混合物,从而获得乙醇,最后再加入稀硫酸,将乙酸钠转化为乙酸,再蒸馏,便可获得乙酸。
(1)乙酸乙酯与饱和碳酸钠溶液不互溶,二者分层,所以分离方法为分液,分离所用的仪器是分液漏斗。答案为:分液漏斗;
(2)乙醇与乙酸在浓硫酸、加热条件下反应,可制得乙酸乙酯,制取乙酸乙酯的化学方程式为CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O。答案为:CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O。答案为:CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(3)若插入液面下,图1导管与图2装置中的仪器C中都会产生负压,但图1导管内的空间小,倒吸的液体能进入反应装置内,而图2的干燥管内的空间大,倒吸的液体不能进入反应装置内,所以图1导管末端不能插入饱和碳酸钠溶液,而图2装置中的仪器C的末端可以插入饱和碳酸钠溶液的原因是仪器C上方有一较大容积的空间,液体不会倒流到A。答案为:仪器C上方有一较大容积的空间,液体不会倒流到A;
(4)由前面的分析可知,先将乙酸乙酯与乙酸和乙醇分离开,此时需加入能与乙酸反应、能溶解乙醇、且降低乙酸乙酯溶解度的物质;后来将乙酸盐转化为乙酸,需加入酸性比乙酸强且不易挥发的酸,所以各有关物质的名称:A为乙酸乙酯,E为乙酸。答案为:乙酸乙酯;乙酸;
(5)由上面分析可知,加入的试剂为:a为饱和碳酸钠,b为稀硫酸。答案为:饱和碳酸钠;稀硫酸;
(6)先将分层液体分离,应分液;再将乙醇与乙酸钠分离,应蒸馏;最后将乙酸从溶液中蒸出,应蒸馏,所以有关的操作方法为:①为分液,②为蒸馏,③为蒸馏。答案为:分液;蒸馏;蒸馏。


科目:高中化学 来源: 题型:
【题目】现有7瓶失去标签的试剂瓶,已知它们盛装的液体可能是乙醇、乙酸、苯、乙酸乙酯、油脂、葡萄糖溶液、蔗糖溶液。现通过如下实验来确定各试剂中所装液体的名称。
实验步骤和方法 | 实验现象 |
①把7瓶液体依次标号为A、B、C、D、E、F、G后闻气味 | 只有F、G两种液体没有气味 |
②各取少量于试管中加水稀释 | 只有C、D、E三种液体不溶解而浮在水上层 |
③分别取少量7种液体于试管中加新制的 | 只有B使沉淀溶解,F中产生砖红色沉淀 |
④各取C、D、E少量于试管中,加稀 | 只有C中仍有分层现象,且在D的试管中闻到特殊香味 |
(1)试写出下列序号代表的液体名称:
A________,B________,C_______,D_______,E______,F______,G________。
(2)写出在D中加入![]() 溶液并加热的化学方程式:_______。
溶液并加热的化学方程式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(b)![]() 、(d)
、(d)![]() 、(p)
、(p)![]() 的分子式均为C6H6,下列说法正确的是
的分子式均为C6H6,下列说法正确的是
A. b的同分异构体只有d和p两种B. b、d、p的二氯代物均只有三种
C. b、d、p均可与酸性高锰酸钾溶液反应D. b、d、p中只有b的所有原子处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于取代反应的是( )
A.在催化剂存在条件下苯与溴反应制溴苯
B.ClCH2CH=CH2+NaOH![]() HOCH2CH=CH2+NaCl
HOCH2CH=CH2+NaCl
C.乙酸乙酯在碱性条件下水解
D.在一定条件下苯与氢气反应制环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双酚A是食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害更大。下列有关双酚A的叙述不正确的是

A. 双酚A的分子式是C15H16O2
B. 双酚A的核磁共振氢谱显示氢原子数之比是1:2:2:3
C. 反应①中,1 mol双酚A最多消耗2 mol Br2
D. 反应②的产物中只有一种官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混合酸,加入反应器中;
②向室温下的混合酸中逐滴加入一定量的苯,充分振荡;
③在50~60℃下发生反应,直至反应结束;
④除去混合酸后,粗产品依次用蒸馏水和5%![]() 溶液洗涤,最后再用蒸馏水洗涤;
溶液洗涤,最后再用蒸馏水洗涤;
⑤将用无水![]() 干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
请回答下列问题:
(1)配制一定比例的浓硫酸与浓硝酸的混合酸时,操作的注意事项是_______________________________。
(2)步骤③中,为了使反应在50~60℃下进行,常用的方法是___________________________________。
(3)步骤④中洗涤粗硝基苯应使用的仪器是___________________________________________________。
(4)步骤④中粗产品用5%![]() 溶液洗涤的目的是___________________________________________。
溶液洗涤的目的是___________________________________________。
(5)纯硝基苯是无色、密度比水_______________________________(填“小”或“大”)的油状液体,它具有________味。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,![]() 二氯丙烷
二氯丙烷![]() 是一种重要的化工原料,工业上可用丙烯加成法制备,主要副产物为
是一种重要的化工原料,工业上可用丙烯加成法制备,主要副产物为![]() 氯丙烯
氯丙烯![]() ,反应原理为:
,反应原理为:
Ⅰ![]()
![]() CH2ClCHClCH3(g) H1= -134KJ/mol-1
CH2ClCHClCH3(g) H1= -134KJ/mol-1
Ⅱ![]()
![]() CH2=CHCH2Cl(g)+HCl(g) H2= -102KJ/mol-1
CH2=CHCH2Cl(g)+HCl(g) H2= -102KJ/mol-1
请回答下列问题:
![]() 已知
已知![]()
![]()
![]() 的活化能
的活化能![]() 正
正![]() 为132KJ/mol-1,则该反应的活化能
为132KJ/mol-1,则该反应的活化能![]() 逆
逆![]() 为__________ KJ/mol-1。
为__________ KJ/mol-1。
![]() 一定温度下,向恒容密闭容器中充入等物质的量的
一定温度下,向恒容密闭容器中充入等物质的量的![]() 和
和![]() ,在催化剂作用下发生反应Ⅰ、Ⅱ,容器内气体的压强随时间的变化如下表所示。
,在催化剂作用下发生反应Ⅰ、Ⅱ,容器内气体的压强随时间的变化如下表所示。
时间 | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
压强 | 80 |
|
|
|
|
|
|
①若用单位时间内气体分压的变化来表示反应速率,即ν=![]() ,则前
,则前![]() 内平均反应速率ν(CH2ClCHClCH3)=__________kPamin-1(保留小数点后2位
内平均反应速率ν(CH2ClCHClCH3)=__________kPamin-1(保留小数点后2位![]() 。
。
②该温度下,若平衡时HCl的体积分数为![]() ,则丙烯的平衡总转化率α=__________;反应Ⅰ的平衡常数
,则丙烯的平衡总转化率α=__________;反应Ⅰ的平衡常数![]() ________
________![]() 为以分压表示的平衡常数,保留小数点后2位
为以分压表示的平衡常数,保留小数点后2位![]() 。
。
![]() 某研究小组向密闭容器中充入一定量的
某研究小组向密闭容器中充入一定量的![]() 和
和![]() ,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得
,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得![]() 的产率与温度的关系如图所示。
的产率与温度的关系如图所示。

下列说法错误的是____________![]() 填代号
填代号![]() 。
。
![]() 使用催化剂A的最佳温度约为250℃
使用催化剂A的最佳温度约为250℃
![]() 相同条件下,改变压强会影响
相同条件下,改变压强会影响![]() 的产率
的产率
c.![]() 点是对应温度下
点是对应温度下![]() 的平衡产率
的平衡产率
![]() 提高
提高![]() 反应选择性的关键因素是控制温度
反应选择性的关键因素是控制温度
(4)在四个恒容密闭容器中充入相应量的气体(如图):

发生反应2N2O(g)![]() 2N2(g)+O2(g) △H,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示:
2N2(g)+O2(g) △H,容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图所示:

容器II、Ⅳ的体积为1L,容器Ⅳ中的物质也在470℃下进行反应,起始反应速率:
①![]() 正(N2O)____逆(N2O)。(填“>”“<”或“=”)
正(N2O)____逆(N2O)。(填“>”“<”或“=”)
②图中A、B、C三点处容器内密度最大的点是____(填“A”“B”或“C”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,甲烷与氯气在光照条件下反应,不涉及的实验现象是( )
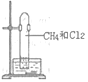
A.气体的黄绿色变浅至消失B.试管内壁上有油珠附着
C.试管内水面上升D.试管内有白烟生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知气态烃A的密度是相同状况下氢气密度的14倍,有机物A~E能发生如图所示一系列变化,则下列说法错误的是

A. A分子中所有原子均在同一平面内
B. A→B所用试剂为![]()
C. 分子式为![]() 的酯有3种
的酯有3种
D. 等物质的量的B、D分别与足量钠反应生成气体的量相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com