【答案】
分析:A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大.A元素的原子半径最小,则A为H元素;B元素原子的最外层电子数是内层电子数的2倍,则内层电子数为2,最外层电子数为4,即B为C元素;C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐,即C为N元素;D与E同主族,D处于第二周期、E处于第三周期,E元素原子的最外层电子数比次外层电子数少2,E元素最外层电子数为6,则E为S元素,D为氧元素;F的原子序数最大,故F为Cl元素,据此解答.
解答:解:A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大.A元素的原子半径最小,则A为H元素;B元素原子的最外层电子数是内层电子数的2倍,则内层电子数为2,最外层电子数为4,即B为C元素;C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐,即C为N元素;D与E同主族,D处于第二周期、E处于第三周期,E元素原子的最外层电子数比次外层电子数少2,E元素最外层电子数为6,则E为S元素、D为氧元素;F的原子序数最大,故F为Cl元素,
(1)B为C,位于元素周期表中的第二周期第ⅣA族,故答案为:第二周期第ⅣA族;
(2)氧气与钠反应生成的化合物可作潜水面具中的供氧剂,该化合物为Na
2O
2,过氧化钠与水反应的离子方程式为2Na
2O
2 +2H
2 O=4Na
++4OH
-+O
2↑,
故答案为:2Na
2O
2 +2H
2 O=4Na
++4OH
-+O
2↑;
(3)同主族自上而下非金属性减弱,故非金属性O>S,O元素的电子能力较强;
a.沸点属于物理性质,不能说明非金属性强弱,故a错误;
b.二者形成的化合物中,O元素的原子显负价,说明O吸引电子的能力强,故b正确;
c.氢化物越稳定,中心元素的非金属性越强,得电子能力强,故c正确;
d.氢化物的水溶液酸性强弱,不能说明中心元素的得电子能力强弱,如HF为弱酸、HCl为强酸,但F原子得电子能力更强,故d错误;
故答案为:氧;bc;
(4)A、C、D、E可形成两种酸式盐为NaHSO
3和NaHSO
4,离子反应为HSO
3-+H
+=SO
2↑+H
2O,
故答案为:HSO
3-+H
+=SO
2↑+H
2O;
(5)由元素H、C、O组成的一元酸X为日常生活中的调味剂,则X为醋酸,元素H、Cl组成的化合物为HCl.醋酸是弱酸、盐酸是强酸,随反应进行醋酸可以继续电离出氢离子,与Zn反应的速率更快,故反应过程中两溶液中反应速率的大小关系是:X>Y,
故答案为:>;
(6)电解饱和食盐水,阴极生成氢气,物质的量为
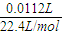
=0.0005mol,由2NaCl+2H
2O

2NaOH+Cl
2↑+H
2↑可知,n(NaOH)=0.0005mol×2=0.001mol,故c(OH
-)=
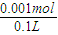
=0.01mol/L,c(H
+)=
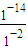
mol/L=10
-12mol/L,故pH=-lg10
-12=12,
故答案为:12.
点评:本题考查位置结构性质关系、常用化学用语、影响反应速率的因素、电解原理计算等,难度中等,推断元素是解题的关键.

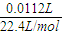 =0.0005mol,由2NaCl+2H2O
=0.0005mol,由2NaCl+2H2O 2NaOH+Cl2↑+H2↑可知,n(NaOH)=0.0005mol×2=0.001mol,故c(OH-)=
2NaOH+Cl2↑+H2↑可知,n(NaOH)=0.0005mol×2=0.001mol,故c(OH-)=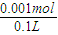 =0.01mol/L,c(H+)=
=0.01mol/L,c(H+)=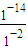 mol/L=10-12mol/L,故pH=-lg10-12=12,
mol/L=10-12mol/L,故pH=-lg10-12=12,

 名校课堂系列答案
名校课堂系列答案 [化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.
[化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.