

| һ������ |


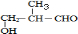 ��C��D������ȥ��Ӧ����DΪ
��C��D������ȥ��Ӧ����DΪ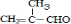 ��D�е�̼̼˫����̼��˫���������ӳ�����E����EΪ
��D�е�̼̼˫����̼��˫���������ӳ�����E����EΪ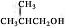 ��E��F������ȥ��Ӧ����FΪ
��E��F������ȥ��Ӧ����FΪ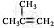 ���������֪��H��±��������HӦ����F��HCl�ӳ����ã�HΪ
���������֪��H��±��������HӦ����F��HCl�ӳ����ã�HΪ ��������֪��2������Ϣ�ɵã�G����2��H��2��Na��Ӧ���ã���GӦ����8��Cԭ�ӣ�GӦΪ
��������֪��2������Ϣ�ɵã�G����2��H��2��Na��Ӧ���ã���GӦ����8��Cԭ�ӣ�GӦΪ ��������Ҫ����л���Ľṹ�����ʽ����⣮
��������Ҫ����л���Ľṹ�����ʽ����⣮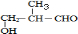 ��C��D������ȥ��Ӧ����DΪ
��C��D������ȥ��Ӧ����DΪ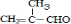 ��D�е�̼̼˫����̼��˫���������ӳ�����E����EΪ
��D�е�̼̼˫����̼��˫���������ӳ�����E����EΪ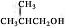 ��E��F������ȥ��Ӧ����FΪ
��E��F������ȥ��Ӧ����FΪ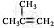 ���������֪��H��±��������HӦ����F��HCl�ӳ����ã�HΪ
���������֪��H��±��������HӦ����F��HCl�ӳ����ã�HΪ ��������֪��2������Ϣ�ɵã�G����2��H��2��Na��Ӧ���ã���GӦ����8��Cԭ�ӣ�GӦΪ
��������֪��2������Ϣ�ɵã�G����2��H��2��Na��Ӧ���ã���GӦ����8��Cԭ�ӣ�GӦΪ ��
��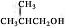 ������ȥ��Ӧ����
������ȥ��Ӧ����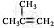 ����Ӧ�ķ���ʽΪCH3CH��CH3��CH2OH
����Ӧ�ķ���ʽΪCH3CH��CH3��CH2OH| Ũ���� |
| �� |
 ��Na�Ĵ����·���ȡ����Ӧ����
��Na�Ĵ����·���ȡ����Ӧ���� ����Ӧ�ķ���ʽΪ2��CH3��3CCl+2Na
����Ӧ�ķ���ʽΪ2��CH3��3CCl+2Na| һ������ |
| Ũ���� |
| �� |
| һ������ |
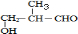 ����������Ӧ����������ΪCH2OHCH��CH3��COOH��ͨ��������Ӧ���е����۷�Ӧ���ɾ�������Ӧ����ʽΪ��
����������Ӧ����������ΪCH2OHCH��CH3��COOH��ͨ��������Ӧ���е����۷�Ӧ���ɾ�������Ӧ����ʽΪ��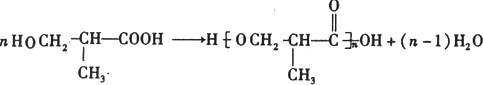 ��
��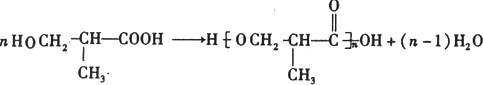 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��2H2SO4��Ũ��+Cu
| ||||
B��2H2SO4��Ũ��+C
| ||||
C��H2SO4��Ũ��+NaCl
| ||||
D��H2SO4+Na2SO3
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
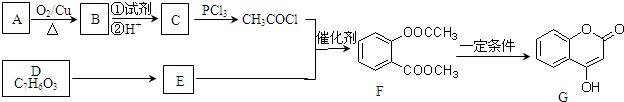
| PCl3 |
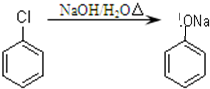 ����ȡ���ӣ������ǻ�һ�㲻��ֱ�������������������ᱽ������
����ȡ���ӣ������ǻ�һ�㲻��ֱ�������������������ᱽ������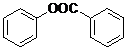 ����һ����Ҫ���л��ϳ��м��壮��д���Ա����ױ�Ϊԭ����ȡ�û�����ĺϳ�·������ͼ����ԭ�����ã���
����һ����Ҫ���л��ϳ��м��壮��д���Ա����ױ�Ϊԭ����ȡ�û�����ĺϳ�·������ͼ����ԭ�����ã���| O2 |
| ���� |
| CH3CH2OH |
| ŨH2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


 ��5�����й��ڻ�����I��II��V��VI��˵����ȷ����
��5�����й��ڻ�����I��II��V��VI��˵����ȷ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 2 |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����0.1 mol?L-1 NaHCO3��Һ�У�c��Na+����c��HCO3-����c��CO32-����c��H2CO3�� |
| B����0.1 mol?L-1 Na2CO3��Һ�У�c��OH-��-c��H+��=c��HCO3-��+2c��H2CO3�� |
| C����0.2 mol?L-1 NaHCO3��Һ�м�������0.1 mol?L-1 NaOH��Һ��c��CO32-����c��HCO3-����c��OH-����c��H+�� |
| D��CH3COONa��CH3COOH�����Һһ�����ڣ�c��Na+��=c��CH3COO-��=c��CH3COOH����c��H+��=c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ͨ��ˮ�У���Һ�����ԣ�Cl2+H2O?2H++Cl-+ClO- | ||||
B����ͭ���缫���CuSO4��Һ��2Cu2++2H2O
| ||||
| C��NaHS���뷽��ʽ��NaHS?Na++HS- | ||||
| D��NH4Clˮ�ⷴӦ��NH4++2H2O?NH3?H2O+H3O+ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com