
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) ![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t ℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_________________________________。
(2)该反应为________反应(填“吸热”或“放热”)。
(3)某温度下,各物质的平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为______。
(4)若830 ℃时,向容器中充入1 mol CO、5 mol H2O,反应达到平衡后,其化学平衡常数K______1.0(填“大于”“小于”或“等于”)。
(5)830 ℃时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的体积。平衡____移动(填“向正反应方向”“向逆反应方向”或“不”)。
(6)若1 200 ℃时,在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、2 mol·L-1、4 mol·L-1、4 mol·L-1,则此时上述反应的平衡移动方向为__________(填“正反应方向”“逆反应方向”或“不移动”)。
【答案】 ![]() 吸热 700 ℃ 等于 不 逆反应方向
吸热 700 ℃ 等于 不 逆反应方向
【解析】(1)化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,因此该反应的化学平衡常数表达式K=![]() 。(2)根据表中数据可知随着反应的进行平衡常数逐渐增大,这说明升高温度平衡向正反应方向进行,所以该反应为吸热反应。(3)某温度下,各物质的平衡浓度符合3c(CO2)·c(H2)=5c(CO)·c(H2O),则此时浓度熵是[c(CO)·c(H2O)]/[c(CO2)·c(H2)]=0.6,所以此时的温度为700℃。(4)平衡常数只与温度有关系,温度不变平衡常数不变,则反应达到平衡后,其化学平衡常数K等于1.0。(5)反应前后体积不变,在其他条件不变的情况下,扩大容器的体积,平衡不移动。(6)若1 200 ℃时,在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、2 mol·L-1、4 mol·L-1、4 mol·L-1,则此时浓度熵是[c(CO)·c(H2O)]/[c(CO2)·c(H2)]=4>2.6,所以上述反应的平衡移动方向为逆反应方向。
。(2)根据表中数据可知随着反应的进行平衡常数逐渐增大,这说明升高温度平衡向正反应方向进行,所以该反应为吸热反应。(3)某温度下,各物质的平衡浓度符合3c(CO2)·c(H2)=5c(CO)·c(H2O),则此时浓度熵是[c(CO)·c(H2O)]/[c(CO2)·c(H2)]=0.6,所以此时的温度为700℃。(4)平衡常数只与温度有关系,温度不变平衡常数不变,则反应达到平衡后,其化学平衡常数K等于1.0。(5)反应前后体积不变,在其他条件不变的情况下,扩大容器的体积,平衡不移动。(6)若1 200 ℃时,在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、2 mol·L-1、4 mol·L-1、4 mol·L-1,则此时浓度熵是[c(CO)·c(H2O)]/[c(CO2)·c(H2)]=4>2.6,所以上述反应的平衡移动方向为逆反应方向。


科目:高中化学 来源: 题型:
【题目】t℃时,向xgKNO3不饱和溶液中,加入agKNO3或蒸发掉bg水恢复到t℃,溶液均达到饱和,据此下列推论错误的是
A. 在t℃时,KNO3的溶解度为100a/b g
B. 若原溶液中溶质质量分数为![]() ,则x=2b
,则x=2b
C. 若原不饱和溶液蒸发掉2b g水,恢复到原温度,能析出2a gKNO3
D. 在t℃时所配得的KNO3溶液中溶质质量分数≤![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.向KI溶液中通入适量Cl2后,溶液颜色变深
B.向KCl溶液中滴加几滴酚酞试液,溶液颜色变红
C.溴水与NaCl溶液混合时,会发生置换反应
D.NaCl溶液在空气中会被氧化,故需要密封保存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】安妥明是一种有机合成药物,能促进胆固醇分解和排泄,降低血液粘度,有抗血栓的作用。下图是以苯酚为主要有机原料制备安妥明的主要成分(N)和高分子化合物(M)的合成路线:
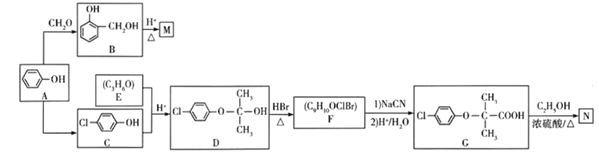
回答下列问题:
(1)CH2O的化学名称是_____________________。
(2)反应A→C和B→M的反应类型分别为_________________、_____________________。
(3)反应E+C→D为加成反应,则E的结构简式为_______________________。
(4)写出D→F的化学方程式:______________________________________。
(5)有机物X是G的同分异构体,且X、G中含有相同的官能团,X的苯环上有两个取代基,氯原子、醚键与苯环直接相连,则满足要求的X的结构有_____种,其中核磁共振氢谱中有6种不同化学环境的氢,峰面积比为2:2:2:2:2:1,写出符合条件的分子的结构简式:_________。
(6)根据题中信息写出利用乙烷合成丙酸乙酯的合成路线:______________________(其他无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列热化学方程式:
①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ/mol
②H2(g)+![]() O2(g)===H2O(l) ΔH2=-285.8 kJ/mol
O2(g)===H2O(l) ΔH2=-285.8 kJ/mol
③CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH3=-870.3 kJ/mol
可以计算出2C(s)+2H2(g)+O2(g)===CH3COOH(l)的反应热为( )
A.ΔH=+244.1 kJ/mol B.ΔH=-488.3 kJ/mol
C.ΔH=-996.6 kJ/mol D.ΔH=+996.6 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大。I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)![]() I3-(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )
I3-(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )

A. 反应I2(aq)+I-(aq)![]() I3 -(aq)的ΔH>0
I3 -(aq)的ΔH>0
B. 利用该反应可以除去硫粉中少量的碘单质
C. 在上述平衡体系中加入CCl4,平衡不移动
D. 25℃时,在上述平衡体系中加入少量KI固体,平衡常数K小于680
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水资源非常重要,联合国确定2003年为国际淡水年。海水淡化是海岛地区提供淡水的重要手段,所谓海水淡化是指除去海水中的盐分以获得淡水的工艺过程(又称海水脱盐),其方法较多,如反渗透法、水合物法、电渗透法、离子交换法和压渗法等。下列方法中也可以用来进行海水淡化的是( )
A.过滤法B.蒸馏法C.分液法D.冰冻法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com