
【题目】铁与下列物质反应所得产物中铁为+3价的是
A. 硫磺B. 稀硫酸C. 硫酸铜溶液D. 氯气
科目:高中化学 来源: 题型:
【题目】水煤气(![]() 和
和![]() )是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:![]()
![]()
![]()
![]()
1.该反应的平衡常数![]() 随温度的升高而________(选填“增大”“ 减小”或“不变”)
随温度的升高而________(选填“增大”“ 减小”或“不变”)
2.上述反应达到平衡后,将体系中的![]() 部分移走,平衡________(选填“向左移”“向右移”或“不移动”下同)。达到平衡后,增加H2O(g)的浓度,平衡_____________
部分移走,平衡________(选填“向左移”“向右移”或“不移动”下同)。达到平衡后,增加H2O(g)的浓度,平衡_____________
3.下列事实能说明该反应在一定条件下已达到平衡状态的有_______(填序号)。
A.单位体积内每消耗![]() 的同时生成
的同时生成![]()
B.混合气体总物质的量保持不变
C.生成![]() 的速率与消耗
的速率与消耗![]() 的速率相等
的速率相等
D.![]() 、
、![]() 、
、![]() 的浓度相等
的浓度相等
4.某温度下,将![]() 和足量的炭充入2
和足量的炭充入2 ![]() 的密闭容器中,发生如下反应,
的密闭容器中,发生如下反应,![]()
![]()
![]() ,达到平衡时测得
,达到平衡时测得![]() ,则此温度下
,则此温度下![]() 的转化率为________。
的转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:由环戊二烯可以合成二聚环戊二烯![]() ,下列有机物能够合成
,下列有机物能够合成![]() 的组合是( )
的组合是( )
①1,3-丁二烯 ②2-甲基-l,3-丁二烯 ③1,3-戊二烯 ④2,3-二甲基-l,3-丁二烯
⑤2,3-二甲基-l,3-戊二烯 ⑥乙炔 ⑦丙炔 ⑧2-丁炔
A. ①、⑦及④、⑧ B. ⑤、⑥及③、⑧
C. ①、③及②、⑧ D. ②、⑧及④、⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在pH=1的无色溶液中,以下离子可以大量共存的是( )
A.K+、Al3+、HCO3-、Cl- B.AlO2-、Cl-、K+、Na+
C.NO3-、Fe2+、K+、SO42- D.Al3+、NH4+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用镁还原硝基苯制取反式偶氮苯。实验原理如下:
2![]() +4Mg+8CH3OH→
+4Mg+8CH3OH→![]() +4Mg(OCH3)2+4H2O
+4Mg(OCH3)2+4H2O
已知:①Mg(OCH3)2在水中极易水解。
②反式偶氮苯产品在紫外线照射后部分转化为顺式偶氮苯。

⑴在反应装置中,加入原料及溶剂,搅拌下加热回流。反应加入的镁条应用砂纸打磨干净的的原因是___________。
⑵反应结束后将反应液倒入冰水中,用乙酸中和至中性,即有反式偶氮苯粗产品析出,抽滤,滤渣用95%乙醇水溶液重结晶提纯。
①为了得到较大颗粒的晶体,加入乙酸时需要___________(填“缓慢加入”、“快速加入”)。
②烧杯中的反式偶氮苯转入布氏漏斗时,杯壁上往往还粘有少量晶体,需选用液体将杯壁上的晶体冲洗下来后转入布氏漏斗,下列液体最合适的是___________。
A.冰水 B.饱和NaCl溶液
C.95%乙醇水溶液 D.滤液
③抽滤完毕,应先断开___________之间的橡皮管,以防倒吸。
④重结晶操作包括“加热溶解、趁热过滤、冷却结晶、抽滤、洗涤、干燥”。上述重结晶过程中的___________操作除去了不溶性杂质。
⑶薄层色谱分析中,极性弱的物质,在溶剂中扩散更快。某同学采用薄层色谱分析所得偶氮苯,实验开始时和展开后的斑点如图所示,则反式偶氮苯比顺式偶氮苯的分子极性___________(填“强”或“弱”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以废旧铅蓄电池的含铅废料(主要含Pb、PbO、PbO2、PbSO4)和稀H2SO4为原料制备高纯PbO,实现铅的再生利用。其主要流程如下:
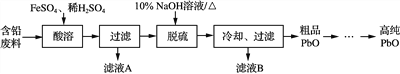
(1) 酸溶过程中加热的目的是______________。酸溶时,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是________________________。
(2) 检验滤液A中是否含有Fe2+,可选用下列________试剂(选填序号)。
a. KSCN溶液 b. 氯水 c. 酸性KMnO4溶液
(3) 写出脱硫过程发生主要反应的离子方程式__________________。
(4) 冷却过滤后对所得的固体进行洗涤的操作________________。
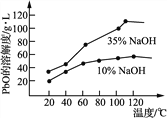
(5) PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)![]() NaHPbO2(aq)
NaHPbO2(aq)
其溶解度曲线如图所示。结合上述溶解度曲线,简述由粗品PbO得到高纯PbO的操作____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com