
【题目】如图为一种微生物燃料电池结构示意图,关于该电池叙述正确的是( ) 
A.正极反应式为MnO2+4H++2e﹣═Mn2++2H2O
B.微生物所在电极区放电时发生还原反应
C.放电过程中,H+从正极区移向负极区
D.若用该电池给铅蓄电池充电,MnO2 电极质量减少8.7g,则铅蓄电池阴极增重9.6g
 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】在冰晶石(Na3[AlF6])晶胞中,[AlF6]3﹣占据的位置相当于NaCl晶胞中Cl﹣占据的位置,则冰晶石晶胞中含有的原子数与NaCl晶胞中含有的原子数之比为( )
A.2:1
B.3:2
C.5:2
D.5:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是( ) 
①分子式为C15H14O7
②1mol儿茶素A在一定条件下最多能与7mol H2加成
③等质量的儿茶素A分别与足量的金属钠和氢氧化钠反应消耗金属钠和氢氧化钠的物质的量之比为1:1
④1mol儿茶素A与足量的浓溴水反应,最多消耗Br2 4mol.
A.①②
B.②③
C.③④
D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种核电荷数依次增加的短周期元素, A 的原子中没有中子,B 原子的最外层电子数是内层电子数的两倍,C是短周期元素中金属性最强的, D和C相邻, E和F的最高价氧化物对应的水化物都是强酸。回答下列问题:
(1)写出B在元素周期表中的位置_______,C的离子结构示意图_______________。
(2)E的最简单氢化物的电子式_____________。F的最高价氧化物对应的水化物的化学式_______________。
(3)证明C比D活泼的实验依据是_______________。
(4)单质D在 B的最高氧化物中燃烧的化学方程式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某体积可变的密闭容器盛有适量的A和B的混合气体,在一定条件下发生反应:A(g)+3B(g)![]() 2C(g),若维持温度和压强不变,当达到平衡时,容器的体积为2L,其中C气体的体积占10%,下列推断正确的是
2C(g),若维持温度和压强不变,当达到平衡时,容器的体积为2L,其中C气体的体积占10%,下列推断正确的是
①原混合气体的体积为2.4L ②原混合气体的体积为2.2L
③反应达平衡时,气体A消耗掉0.1L ④反应达平衡时,气体B消耗掉0.1L
A. ②③ B. ②④ C. ①③ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们常用催化剂来选择反应进行的方向.如图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].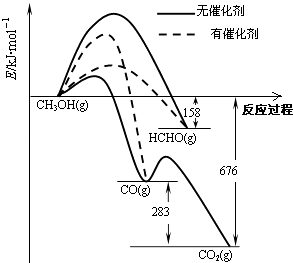
(1)①在有催化剂作用下,CH3OH与O2反应主要生成(填“CO、CO2”或“HCHO”).2HCHO(g)+O2(g)═2CO(g)+2H2O(g)△H= .
②甲醇制取甲醛可用Ag作催化剂,含有AgCl会影响Ag催化剂的活性.用氨水可以溶解除去其中的AgCl,写出该反应的离子方程式: .
(2)已知:CO(g)+2H2(g)CH3OH(g)△H=﹣a kJmol﹣1 .
①经测定不同温度下该反应的平衡常数如下:
温度(℃) | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4molL﹣1、c(H2)=0.4molL﹣1、c(CH3OH)=0.8molL﹣1 , 则此时v正v逆(填“>”、“<”或“=”).
②某温度下,在体积固定的2L的密闭容器中将1mol CO和2mol H2混合,测得不同时刻的反应前后压强关系如下:
时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
则0~15min,用H2表示的平均反应速率为 , 达到平衡时CO的转化率为 .
(3)利用钠碱循环法可除去SO2 , 消除SO2对环境的污染.吸收液吸收SO2的过程中,pH随n(SO32﹣):n(HSO3﹣)变化关系如下表:
n(SO32﹣):n(HSO3﹣) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①根据上表判断NaHSO3溶液显性.
②在NaHSO3溶液中离子浓度关系正确的是 (填字母).
a.c(Na+)=2c(SO32﹣)+c(HSO3﹣)
b.c(Na+)>c(HSO3﹣)>c(H+)>c(SO32﹣)>c(OH﹣)
c.c(H2SO3)+c(H+)=c(SO32﹣)+(OH﹣)
d.c(Na+)+c(H+)=c(SO32﹣)+c(HSO3﹣)+c(OH﹣)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com