
| n |
| V |
| ||
| ||
| ||
| ||
| n |
| V |
| 0.4mol |
| 0.25L |


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
| A、氟气通入水中:2F2+2H2O═4F-+4H++O2 |
| B、向小苏打溶液中加入过量的石灰水:Ca2++2OH-+2HCO3-═CaCO3↓+CO32-+2H2O |
| C、硫氢化钠溶液与盐酸反应:S2-+2H+═H2S↑? |
| D、FeBr2溶液与等摩Cl2反应:2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Q1相等Q2 |
| B、Q1大于Q2 |
| C、Q1小于Q2 |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、锌跟稀硫酸反应制取氢气,加入少量的硫酸铜能加快反应速率 |
| B、镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀 |
| C、为保护海轮的船壳,常在船壳外面镶上锌块 |
| D、钢铁在发生析氢腐蚀和吸氧腐蚀时,负极反应是相同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
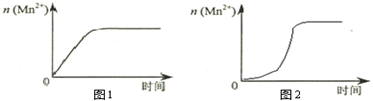
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | t | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com