
【题目】已知:反应aA(g)+bB(g) ![]() cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
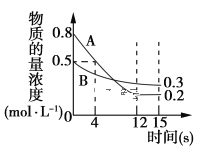
(1)从反应开始到12 s时,用A表示的反应速率为________。
(2)经测定前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式为______________。
(3)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L-1·s-1;乙:v(B)=0.12 mol·L-1·s-1;丙:v(C)=9.6 mol·L-1·min-1;则甲、乙、丙三个容器中反应速率由快到慢的顺序为________。
(4)下表所列数据是反应CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)![]() H1在不同温度下的化学平衡常数(K)。
H1在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
①由表中数据判断![]() H1_______0(填“>”“=”或“<”);
H1_______0(填“>”“=”或“<”);
②某温度下,将2molCO和6molH2充入2L密闭容器,充分反应,达平衡后,测得c(CO)=0.2mol·L-1,则CO的转化率为__________,此时的温度为_______________从上表中选择)
(5)将CH4转化成CO,工业上常采用催化转化技术,其反应原理为:
CH4(g)+3/2O2(g)![]() CO(g)+2H2O(g)
CO(g)+2H2O(g)![]() H=-519kJ·mol-1。工业上,为选择合适的催化剂,分别对X、Y、Z三 种催化剂进行了如下实验(其他条件相同)
H=-519kJ·mol-1。工业上,为选择合适的催化剂,分别对X、Y、Z三 种催化剂进行了如下实验(其他条件相同)
①X在T1℃时催化效率最高,能使正反应速率加快约3×105倍;
②Y在T2℃时催化效率最高,能使正反应速率加快约3×105倍;
③Z在T3℃时催化效率最高,能使逆反应速率加快约1×106倍;
已知:T1> T2> T3,根据上述信息,你认为在生产中应该选择的适宜催化剂是__(填“X”、“Y”或“Z”)选择的理由是_______________________________________________。
【答案】0.05 mol·L-1·s-1 3A(g)+B(g) ![]() 2C(g) 乙>甲>丙 < 80% 250℃ Z 催化效率高且活性温度低
2C(g) 乙>甲>丙 < 80% 250℃ Z 催化效率高且活性温度低
【解析】
(1)根据![]() 进行计算;
进行计算;
(2)计算出12s内用A表示的化学反应速率,可以计算出a与b的比值,利用题给4s内v(C)=0.05molL-1s-1,计算出abc的最简整数比;
(3)将不同速率转化为同一物质的用相同单位进行描述的速率进行比较;
(4)①由表中数据可知,温度越高平衡常数越小,说明升高温度平衡向逆反应方向移动,正反应为放热反应;
②根据CO的平衡浓度计算平衡时CO的物质的量,进而计算参加反应的CO的物质的量,再根据转化率定义计算;列式三段式计算平衡浓度,结合平衡常数概念计算得到;
(5)该反应正反应为放热反应,应选择催化活性高、速度快、反应温度较低;
(1)从反应开始到12s时,A的浓度变化量△c=0.8mol/L-0.2mol/L=0.6mol/L,时间为12s,故![]() =0.05mol/(Ls),故答案为:0.05 mol·L-1·s-1;
=0.05mol/(Ls),故答案为:0.05 mol·L-1·s-1;
(2)12s时,B的浓度变化量△c=0.5mol/L-0.3mol/L=0.2mol/L,故a:b=0.6:0.2=3:1,经测定前4s内v(C)=0.05molL-1s-1,此时A浓度变化为:0.8mol/L-0.5mol/L=0.3mol/L,此时v(A)=![]() =0.075mol/(Ls),即v(A):v(C)=0.075:0.05=3:2,故a:b:c=3:1:2,故化学反应方程式为:3A(g)+B(g)2C(g);
=0.075mol/(Ls),即v(A):v(C)=0.075:0.05=3:2,故a:b:c=3:1:2,故化学反应方程式为:3A(g)+B(g)2C(g);
故答案为:3A(g)+B(g)2C(g);
(3)确定A的速率为:甲:v(A)=0.3molL-1s-1;乙:v(B)=0.12molL-1s-1,故v(A)=3×0.12molL-1s-1=0.36molL-1s-1;丙:v(C)=9.6molL-1min-1==0.16molL-1s-1,故v(A)=![]() ×0.16molL-1min-1=0.24molL-1s-1,故最快的是乙,最慢的是丙,故答案为:乙>甲>丙;
×0.16molL-1min-1=0.24molL-1s-1,故最快的是乙,最慢的是丙,故答案为:乙>甲>丙;
(4))①由表中数据可知,温度越高平衡常数越小,说明升高温度平衡向逆反应方向移动,正反应为放热反应,即△H1<0;
故答案为:<;
②某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L;达到平衡后,测得c(CO)=0.2mol/L,则参加反应的CO的物质的量=2mol-0.2mol/L×2L=1.6mol,故CO转化率=![]() ×100%=80%,依据化学平衡三段式列式计算得到平衡浓度:
×100%=80%,依据化学平衡三段式列式计算得到平衡浓度:

K=![]() ,对照图表数据判断温度为250°C;
,对照图表数据判断温度为250°C;
故答案为:80%;250°C;
(5)该反应正反应为放热反应,应选择催化活性高、速度快、反应温度较低,故选择Z;
故答案为:Z;催化效率高且活性温度低。


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
【题目】下列有关醛的说法正确的是
A.分子通式为CnH2nO的有机物与乙醛一定互为同系物
B.用溴水可以检验CH2=CHCHO中含有的碳碳双键
C.对甲基苯甲醛(![]() )可使酸性KMnO4溶液褪色,说明醛基具有还原性
)可使酸性KMnO4溶液褪色,说明醛基具有还原性
D.能发生银镜反应的有机物不一定是醛类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化石燃料开采、加工过程产生的H2S 废气制取氢气,既价廉又环保。
(1)工业上可用组成为K2O·M2O3·2RO2·nH2O的无机材料纯化制取的氢气。
①已知元素M、R均位于元素周期表中第3周期,两种元素原子的质子数之和为27,则R的原子结构示意图为____________;
②常温下,不能与M单质发生反应的是____________(填序号);
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)利用H2S废气制取氢气的方法有多种。
①高温热分解法已知:H2S(g)![]() H2(g)+1/2S2(g)
H2(g)+1/2S2(g)
在恒容密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol·L-1测定H2S的转化率,结果见图。曲线a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。根据图像回答下列问题:

i 计算 985 ℃时H2S按上述反应分解的平衡常数 K=________;
ii 说明随温度的升高,曲线b向曲线a逼近的原因:________________________________;
②电化学法

i该法制氢过程如图。反应池中反应物的流向采用气、液逆流方式,其目的是____________;
ii反应池中发生反应的化学方程式为____________;
iii反应后的溶液进入电解池,电解总反应的离子方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。该温度下,下列说法正确的是

A. 含有大量SO42-的溶液中肯定不存在Ag+
B. Ag2SO4的溶度积常数(Ksp)为1×10-3
C. 0.02 mol·L-1的AgNO3溶液与0.02 mol·L-1的Na2SO4溶液等体积混合不会生成沉淀
D. a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
(实验原理)2KMnO4 + 5H2C2O4 + 3H2SO4 = K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
(实验内容及记录)
实验编号 | 室温下,试管中所加试剂及其用量 / mL | 室温下溶液颜色褪至无色所需时间 / min | |||
0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05mol/L KMnO4溶液 | ||
1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
请回答:
(1)根据上表中的实验数据,可以得到的结论是___________________________________。
(2)利用实验1中数据计算,若用KMnO4的浓度变化表示的反应速率为:υ(KMnO4)= ________。
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
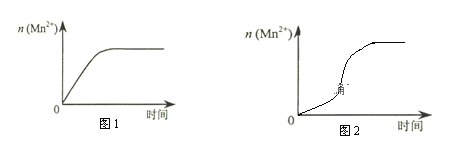
①该小组同学提出的假设是___________________________________________________。
②请你帮助该小组同学完成实验方案,并填写表中空白。
实验编号 | 室温下,试管中所加试剂及其用量 / mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间 / min | |||
0.6mol/L H2C2O4溶液 | H2O | 3mol/L稀硫酸 | 0.05mol/L KMnO4溶液 | |||
4 | 3.0 | 2.0 | 2.0 | 3.0 | _______ | t |
③若该小组同学提出的假设成立,应观察到的现象是_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是4种短周期主族元素,在周期表中的相对位置如表,已知四种元素的原子最外层电子数之和为18,则以下说法中正确的是( )
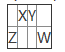
A.Y的最高正化合价与最低负化合价的代数和为2
B.X、Y、Z、W四种原子中,X的原子半径最小
C.Y的氢化物的沸点一定高于X的氢化物的沸点
D.X、Y、W三种元素氧化物对应的水化物的酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒容密闭容器中充满NO2,常温下建立下列平衡:2NO2(g)![]() N2O4(g)ΔH < 0,将容器置于100 ℃的水浴中,则下列性质不改变的是
N2O4(g)ΔH < 0,将容器置于100 ℃的水浴中,则下列性质不改变的是
A.颜色B.压强C.质量D.平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向HCl、AlCl3混合溶液中逐滴加入NaOH溶液,生成沉淀的量随NaOH溶液加入量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是( )

A. M点对应的溶液中:K+、Fe2+、SO42-、NO3-
B. N点对应的溶液中:K+、NH4+、Cl-、CO32-
C. S点对应的溶液中:Na+、SO42-、HCO3-、NO3-
D. R点对应的溶液中:Na+、SO42-、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究![]() 、
、![]() 、CO等大气污染气体测量及处理具有重要意义,目前,消除污染有多种方法.
、CO等大气污染气体测量及处理具有重要意义,目前,消除污染有多种方法.
(1)用活性炭还原法处理氮氧化物.有关反应为:![]() 某研究小组向某密闭容器中加人一定量的活性炭和NO,恒温
某研究小组向某密闭容器中加人一定量的活性炭和NO,恒温![]() 条件下反应,反应进行到不同时间测得各物质的浓度如下.
条件下反应,反应进行到不同时间测得各物质的浓度如下.
| NO |
|
|
0 |
| 0 | 0 |
10 |
|
|
|
20 |
|
|
|
30 |
|
|
|
40 |
|
|
|
50 |
|
|
|
①![]() 时,该反应的平衡常数
时,该反应的平衡常数![]() ______
______ ![]() 保留两位小数
保留两位小数![]() .
.
②![]() 后,改变某一条件,反应重新达到平衡,则改变的条件可能是 ______ ;
后,改变某一条件,反应重新达到平衡,则改变的条件可能是 ______ ;
③若30min后升高温度至![]() ,达到平衡时,容器中NO、
,达到平衡时,容器中NO、![]() 、
、![]() 的浓度之比为5:3:3,则该反应的
的浓度之比为5:3:3,则该反应的![]() ______
______ ![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]()
(2)用![]() 催化还原氮氧化物可以消除氮氧化物的污染.已知:
催化还原氮氧化物可以消除氮氧化物的污染.已知:
①![]()
②![]()
③![]()
写出![]() 与
与![]() 反应生成
反应生成![]() 、
、![]() 和
和![]() 的热化学方程式 ______
的热化学方程式 ______
(3)新型氨法烟气脱硫技术化学原理是采用氨水吸收烟气中的![]() ,再用一定量磷酸与上述吸收产物反应.该技术优点除了能回收利用
,再用一定量磷酸与上述吸收产物反应.该技术优点除了能回收利用![]() 外,还能得到一种复合肥料.
外,还能得到一种复合肥料.
①该复合肥料可能的化学式为 ______ ![]() 写出一种即可
写出一种即可![]() .
.
②若氨水与![]() 恰好完全反应生成正盐,则此时溶液呈 ______ 性
恰好完全反应生成正盐,则此时溶液呈 ______ 性![]() 填“酸”或“碱”
填“酸”或“碱”![]() .
.![]() 已知常温下:氨水
已知常温下:氨水![]() ,
,![]()
![]() ,
,![]() .
.![]()
(4)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的.如图是通过人工光合作用,以![]() 和
和![]() 为原料制备HCOOH和
为原料制备HCOOH和![]() 的原理示意图.催化剂b表面发生的电极反应式为 ______
的原理示意图.催化剂b表面发生的电极反应式为 ______ ![]() 常温下,
常温下,![]() 的HCOONa溶液pH为10,则HCOOH的电离常数
的HCOONa溶液pH为10,则HCOOH的电离常数![]() ______ .
______ .

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com