
【题目】用如图所示装置研究原电池原理。下列叙述错误的是
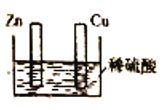
A.Cu棒和Zn棒用导线连接时,铜片上有气泡逸出
B.Cu棒和Zn棒不连接时,锌片上有气泡逸出
C.无论Cu棒和Zn棒是否用导线连接,装置中所涉及的总反应都相同
D.无论Cu棒和Zn棒是否用导线连接,装置都是把化学能转化为电能
【答案】D
【解析】
不连接时,锌发生化学腐蚀,锌和氢离子发生置换反应;两个电极用导线连接时,该装置构成原电池,Zn作负极、Cu作正极,电子从负极沿导线流向正极,据此分析解答。
A. Zn与Cu用导线连接时,该装置构成原电池,由于金属活动性Zn>Cu,Zn易失电子作负极、Cu作正极,电子从锌片流向铜片,H+从铜片上获得锌失去的电子,A正确;
B.Zn与Cu不连接时,由于金属活动性Zn>H>Cu,锌和氢离子发生置换反应,所以锌片上会有气泡逸出,锌片逐渐溶解,B正确;
C.无论Zn与Cu是否用导线连接,锌片均会溶解,发生反应Zn+2H+=Zn2++H2↑,C正确;
D.只有Zn、Cu用导线连接,才能构成原电池,化学能才转变为电能,D错误;
故合理选项是D。


科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素在周期表中的位置如图所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物。
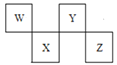
请回答下列问题。
(1)H2Y2的电子式为___________,Z在周期表中的位置___________。
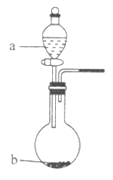
(2)在图中,b的pH约为7,且含有Fe2+和淀粉KI的水溶液,a为H2Y2的水溶液,旋开分液漏斗旋钮,观察到烧瓶中溶液呈蓝色并有红褐色沉淀生成。当消耗2molI-时,共转移3mol电子,该反应的离子方程式是_________________________。
(3)已知:298K时,金属钠与Y2气体反应,若生成1molNa2Y固体时,放出热量414kJ;若生成1molNa2Y2固体时,放出热量511kJ。则由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为_____________。
(4)有人设想利用原电池原理以气体Z2和氢气制备一种重要的化工原料,同时获取电能。假设这种想法可行,用石墨作电极材料,用稀盐酸作电解溶液,则通入Z2的电极为原电池的___________极,其电极反应式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1830年,瑞典化学家塞弗斯托姆从一种铁矿石中得到了一种新元素,并以凡娜迪丝女神(![]() )之名命名为“钒”。钒(
)之名命名为“钒”。钒(![]() )的用途很广,在冶金行业有“第一金属”的美誉。
)的用途很广,在冶金行业有“第一金属”的美誉。
(1)基态钒原子能量最高的电子占据的能级符号为_________。
(2)依据价电子互斥理论推测![]() 的立体构型是______________。
的立体构型是______________。
(3)①化合物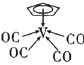 中,中心原子V的价电子与配体提供的电子数之和为18,配体
中,中心原子V的价电子与配体提供的电子数之和为18,配体![]() 不带电荷,且其提供的是大π键的电子,则配体“
不带电荷,且其提供的是大π键的电子,则配体“![]() ”中的大π键可表示为_______。(例如苯中大π键可表示为
”中的大π键可表示为_______。(例如苯中大π键可表示为![]() )
)
②从电负性角度解释![]() 作配体时,配位原子是C而不是O的原因是___________________。
作配体时,配位原子是C而不是O的原因是___________________。
(4)2-巯基烟酸氧钒配合物(如图甲)是有效调节血糖的新型药物的主要成分。
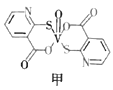
①2-巯基烟酸氧钒配合物中![]() 键长_________(填“大于”“等于”或“小于”)V—O键长,该物质中氮原子的杂化方式是_________________。
键长_________(填“大于”“等于”或“小于”)V—O键长,该物质中氮原子的杂化方式是_________________。
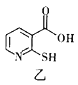
②相同条件下,2-巯基烟酸(如图乙)在水中溶解性好于2-巯基烟酸氧钒配合物的原因是____。
(5)某钒的氧化物的晶胞如图。
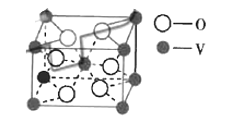
①氧的配位数为_____________。
②已知上述晶胞为立方晶胞,距离最近的钒原子和氧原子间的核间距为![]() ,晶体密度为
,晶体密度为![]() ,则晶胞中底面上的两个氧原子的核间距为__________cm.
,则晶胞中底面上的两个氧原子的核间距为__________cm.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】β一l,3一葡聚糖具有明显的抗肿瘤功效,受到日益广泛的关注。β-l,3一葡聚糖的结构简式如图,下列说法正确的是

A.分子式为(C6Hl2O6)nB.与葡萄糖互为同系物
C.可以发生氧化反应D.葡萄糖发生加聚反应可生成β-l,3一葡聚糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某班学生通过分组实验测定酸碱滴定曲线。
实验用品:0.1 mol·L-1HCl溶液、0.1 mol·L-1NaOH溶液、蒸馏水、pH计、酸式滴定管、碱式滴定管、铁架台(带滴定管夹)、锥形瓶。甲、乙、丙三组同学锥形瓶中的溶液所取体积均为20.00 mL,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示,其中乙和丙两组同学的操作上都存在着不足或失误。
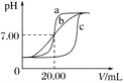
请回答下列问题:
(1)实验前pH计应用标准溶液进行校准,若将pH计放入c(H+)=0.0001 mol·L-1的标准溶液中校准,则pH计的读数应为________。
(2)甲组同学滴定时选用的滴定管为________(填“酸式”或“碱式”)滴定管,最后一次润洗滴定管应选用实验用品中的________进行润洗。
(3)乙组同学操作上的不足之处是________________________________________。
(4)造成丙组同学的曲线与甲组同学不同的原因可能是________(填字母)。
A.用待装液润洗锥形瓶
B.滴定使用的滴定管的尖嘴部分在滴定前有气泡未排出,滴定后气泡消失
C.滴定前后对滴定管进行读数的视线分别如图所示

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列6种有机物: ①CH3CH2CH2CH3②![]() ③
③![]() ④
④![]() ⑤
⑤![]() ⑥
⑥![]() 请回答:
请回答:
(1)属于醇类的是_________(填序号).
(2)与①互为同分异构体的是________(填序号).
(3)与④互为同系物的是_________(填序号).
(4)用系统命名法给③命名,其名称为__________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于氧化还原反应,且氧化剂和还原剂为同一种物质的是
A.MgO+2HCl=MgCl2+H2OB.C+H2O(g)![]() CO+H2
CO+H2
C.8NH3+6NO2![]() 7N2+12H2OD.2Na2O2+2H2O=4NaOH+O2↑
7N2+12H2OD.2Na2O2+2H2O=4NaOH+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,将20mL某气态烃与过量的氧气混合,充分燃烧后冷却至室温,发现混合气体的体积减少60mL,将所得混合气体通过氢氧化钠溶液后,体积又减少80mL。
(1)通过计算确定气态烃分子式_____________________
(2)若该烃能使溴水和高锰酸钾褪色,且该烃与H2加成后的产物有三个甲基,请写出该烃的结构简式____________。又知该烃在一定的温度、压强和催化剂的作用下,生成一种高聚物,写出其方程式________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A.常温下,23g NO2和N2O4的混合气体含有NA个氧原子
B.1L0.1molL-1的氨水含有0.1NA个OH―
C.标准状况下,NO和O2各11.2L混合,所得混合气体的分子总数为0.75NA
D.1molFe与1molCl2充分反应,转移3NA个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com