
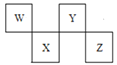
【题目】W、X、Y、Z四种短周期元素在周期表中的位置如图所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物。
请回答下列问题。
(1)H2Y2的电子式为___________,Z在周期表中的位置___________。
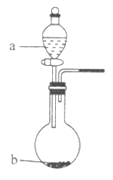
(2)在图中,b的pH约为7,且含有Fe2+和淀粉KI的水溶液,a为H2Y2的水溶液,旋开分液漏斗旋钮,观察到烧瓶中溶液呈蓝色并有红褐色沉淀生成。当消耗2molI-时,共转移3mol电子,该反应的离子方程式是_________________________。
(3)已知:298K时,金属钠与Y2气体反应,若生成1molNa2Y固体时,放出热量414kJ;若生成1molNa2Y2固体时,放出热量511kJ。则由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为_____________。
(4)有人设想利用原电池原理以气体Z2和氢气制备一种重要的化工原料,同时获取电能。假设这种想法可行,用石墨作电极材料,用稀盐酸作电解溶液,则通入Z2的电极为原电池的___________极,其电极反应式为____________________。
【答案】![]() 第三周期ⅦA族 2Fe2++3H2O2+4I-=2Fe(OH)3+2I2 Na2O(s)+1/2O2(g)=Na2O2(s)△H=-97kJ/mol 正极 Cl2+2e-=2Cl-
第三周期ⅦA族 2Fe2++3H2O2+4I-=2Fe(OH)3+2I2 Na2O(s)+1/2O2(g)=Na2O2(s)△H=-97kJ/mol 正极 Cl2+2e-=2Cl-
【解析】
W、X、Y、Z四种短周期元素,由元素在元素周期表中的位置,可知W、Y处于第二周期,X、Z处于第三周期,其中Y与钠元素和氢元素均可形成原子个数l:1和1:2的化合物,则Y为O元素,可推知W为C元素、X为P、Z为Cl。
(1)H2O2分子中O原子之间形成1对共用电子对、H原子与O原子之间形成1对共用电子对,其电子式为![]() ;Z为Cl元素,处于第三周期ⅦA族,故答案为
;Z为Cl元素,处于第三周期ⅦA族,故答案为![]() ;第三周期ⅦA族;
;第三周期ⅦA族;
(2)在图2中,将H2O2的水溶液滴入含有Fe2+和淀粉KI的水溶液,观察到烧瓶中溶液呈蓝色并有红褐色沉淀生成,说明反应生成氢氧化铁与碘单质.当消耗2molI-时,共转移3mol电子,则参加反应的Fe2+物质的量为![]() =1mol,参加反应H2O2的物质的量=
=1mol,参加反应H2O2的物质的量=![]() =1.5mol,故Fe2+、H2O2、I-的化学计量数之比=2:3:4,该反应离子方程式为:2Fe2++3H2O2+4I-=2Fe(OH)3↓+2I2,故答案为2Fe2++3H2O2+4I-=2Fe(OH)3↓+2I2;
=1.5mol,故Fe2+、H2O2、I-的化学计量数之比=2:3:4,该反应离子方程式为:2Fe2++3H2O2+4I-=2Fe(OH)3↓+2I2,故答案为2Fe2++3H2O2+4I-=2Fe(OH)3↓+2I2;
(3)根据题意可知:①2Na(s)+![]() O2(g)=Na2O(s)△H=-414kJ/mol,②2Na(s)+O2(g)=Na2O2(s)△H=-511kJ/mol根据盖斯定律,②-①得Na2O(s)+
O2(g)=Na2O(s)△H=-414kJ/mol,②2Na(s)+O2(g)=Na2O2(s)△H=-511kJ/mol根据盖斯定律,②-①得Na2O(s)+![]() O2(g)=Na2O2(s)△H=-97kJ/mol,故答案为Na2O(s)+
O2(g)=Na2O2(s)△H=-97kJ/mol,故答案为Na2O(s)+![]() O2(g)=Na2O2(s)△H=-97kJ/mol;
O2(g)=Na2O2(s)△H=-97kJ/mol;
(4)氯气获得电子生成Cl-,发生还原反应,应在原电池正极通入,电极反应式为:Cl2+2e-=2Cl-,故答案为正;Cl2+2e-=2Cl-。


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
【题目】已知NA为阿伏加德罗常数的值,下列说法正确的是
A.3g由CO2和SO2组成的混合气体中含有的质子数为1.5NA
B.1L0.1molL-1 Na2SiO3溶液中含有的SiO32-数目为0.1NA
C.0.1molH2O2分解产生O2时,转移的电子数为0.2NA
D.2.8g聚乙烯中含有的碳碳双键数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
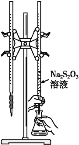
【题目】H2S2O3是一种弱酸,实验室欲用0.01mol·L-1的Na2S2O3溶液滴定I2溶液,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,下列说法合理的是( )
A.该滴定可用甲基橙作指示剂
B.Na2S2O3是该反应的还原剂
C.该滴定可选用如图所示装置
D.该反应中每生成1molNaI,电子转移数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于消去反应的是
A.CH2=CH2+HCl 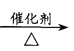 CH3CH2Cl
CH3CH2Cl
B.CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
C.![]() +Br2
+Br2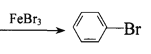 +HBr
+HBr
D.CH3CH2Br+NaOH![]() CH2=CH2+NaBr+H2O
CH2=CH2+NaBr+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是
A.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
B.0.5molC3H8分子中所含C-H共价键数为2NA
C.标准状况下,22.4 L CHCl3中含有的氯原子数目为3NA
D.标准状况下,22.4L乙醇完全燃烧所耗的氧气分子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素的原子序数依次增大,W的某种原子无中子,X、Y可形成原子个数比为1∶1的具有漂白性的物质,工业上常用电解饱和YZ溶液来获得Z的单质及其他产品。下列说法正确的是
A. W和X、Y、Z均能形成18电子的分子
B. 上述四种元素的原子半径大小顺序为r(Z)>r(Y)>r(X)>r(W)
C. X、Y之间形成的化合物可能同时含有离子键和非极性共价健
D. W、X、Z三种元素形成的化合物一定是弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有机物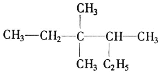 的名称为___________________ 。
的名称为___________________ 。
(2)肉桂酸甲酯是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。它的分子式为C10H10O2,分子中只含有1个苯环,且苯环上只有一个取代基。它的核磁共振氢谱图上有6个信号峰,峰面积之比为1︰2︰2︰1︰1︰3。它的红外光谱图如下。
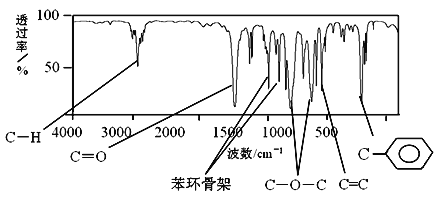
请写出肉桂酸甲酯的结构简式是________________________。
(3)芳香烃A中C、H原子数之比是4∶5,1 mol A在氧气中完全燃烧生成8 mol CO2,A分子中只有7个碳原子一定共平面,A的结构简式是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯苯在染料、医药工业中有广泛的应用,某实验小组利用如下装置合成氯苯(支撑用的铁架台部分省略)并通过一定操作提纯氯苯。
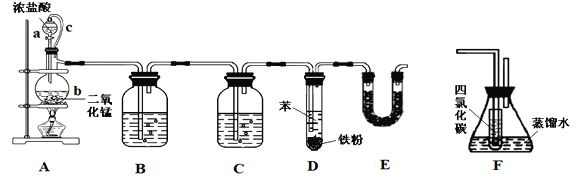
反应物和产物的相关数据列表如下:
密度/g·cm-3 | 沸点/℃ | 水中溶解性 | |
苯 | 0.879 | 80.1 | 微溶 |
氯苯 | 1.11 | 131.7 | 不溶 |
请按要求回答下列问题。
(1)装置A中橡胶管c的作用是______________,装置E的作用是__________________。
(2)实验时;使a中的浓盐酸缓缓滴下,可观察到仪器b内的现象是________________,写出反应的离子方程式______________________________________。
(3)为证明氯气和苯发生的是取代而不是加成反应,该小组用装置F说明,则装置F置于________之间(填字母),F中小试管内CCl4的作用是___________________,还需使用的试剂是______________。
(4)已知D中加入5 mL苯,经过提纯后收集到氯苯3.0 g,则氯苯的产率为_________%(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置研究原电池原理。下列叙述错误的是
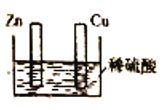
A.Cu棒和Zn棒用导线连接时,铜片上有气泡逸出
B.Cu棒和Zn棒不连接时,锌片上有气泡逸出
C.无论Cu棒和Zn棒是否用导线连接,装置中所涉及的总反应都相同
D.无论Cu棒和Zn棒是否用导线连接,装置都是把化学能转化为电能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com