
【题目】H2S2O3是一种弱酸,实验室欲用0.01mol·L-1的Na2S2O3溶液滴定I2溶液,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,下列说法合理的是( )
A.该滴定可用甲基橙作指示剂
B.Na2S2O3是该反应的还原剂
C.该滴定可选用如图所示装置
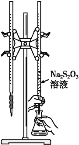
D.该反应中每生成1molNaI,电子转移数为2NA
科目:高中化学 来源: 题型:
【题目】有机物A为烃类化合物,质谱图表明其相对分子质量为70,其相关反应如图所示,其中B、D、E的结构中均含有2个—CH3,它们的核磁共振氢谱中均出现4个峰。请回答:
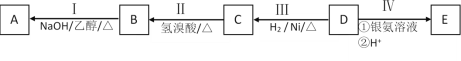
(1)A中所含官能团的名称为___;
(2)Ⅰ的反应类型为___(填字母序号),Ⅲ的反应类型为___;
a.取代反应 b.加成反应 c.氧化反应 d.消去反应
(3)D的分子式为___;
(4)写出下列反应的化学方程式:
Ⅰ:___;
Ⅱ:___;
III:C和E可在一定条件下反应生成F,F为有香味的有机化合物,该反应的化学方程式为___;
(5)A的同分异构体中有一对互为顺反异构,且结构中有2个—CH3,写出其顺式结构的结构简式___;
(6)E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】席夫碱类化合物G在催化、药物、新材料等方面有广泛应用。合成G的一种路线如下:

已知以下信息:
①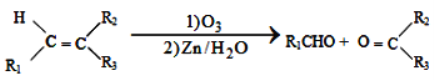
②1molB经上述反应可生成2molC,且C不能发生银镜反应。
③D属于单取代芳香烃,其相对分子质量为106。
④核磁共振氢谱显示F苯环上有两种化学环境的氢。
⑤
回答下列问题:
(1)由A生成B的化学方程式为_______________________。
(2)D的化学名称是______________________。
(3)G的结构简式为_______________________。
(4)F的同分异构体中含有苯环的还有____种(不考虑立体异构)。
(5)由苯和化合物C经如下步骤可合成N-异丙基苯胺。
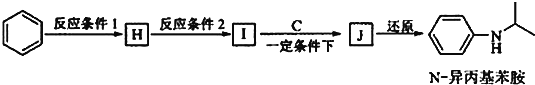
反应条件2所选用的试剂是_____________________, I的结构简式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Prolitane是一种抗抑郁药物,以芳香烃A为原料的合成路线如下:

请回答以下问题:
(1)D的化学名称为______,H→Prolitane的反应类型为______。
(2)E的官能团名称分别为______和______。
(3)B的结构简式为______。
(4)F→G的化学方程式为______。
(5)C的同分异构体中能同时满足下列条件的共有______种(不含立体异构);
①属于芳香化合物 ②能发生银镜反应 ③能发生水解反应
其中核磁共振氢谱显示为4组峰,其峰面积比为3∶2∶2∶1,写出符合要求的该同分异构体的结构简式______。
(6)参照Prolitane的合成路线,设计一条由苯和乙醇为原料制备苯甲酸乙酯的合成路线_____________(其他无机试剂和溶剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学设计实验制备并探究SO2的性质。回答下列问题:
(1)实验室用废铜屑制备SO2的化学方程式为______。
(2)将SO2通入NaHS溶液,溶液中有淡黄色沉淀,说明SO2具有______性。
(3)将SO2通过品红溶液,溶液红色逐渐褪去,将褪色后的溶液微热,又显浅红色,这现象可解释为______。
(4)将SO2通入橙黄色酸性K2Cr2O7溶液,溶液逐渐变为浅绿色,该反应中氧化剂与还原剂的物质的量之比为______。(Cr2O72-被还原为Cr3+)
(5)常温下,改变0.1molL-1H2SO3溶液(SO2水溶液)的pH,溶液中的H2SO3、HSO3-、SO32-的物质的量分数δ(X)[δ(X)= 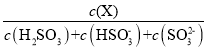 ]随pH的变化如图所示:
]随pH的变化如图所示:
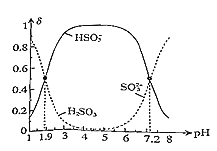
H2SO3的lgKa1=______;反应HSO3-+OH-![]() SO32-+H2O的lgK=______;用0.100molL-1NaOH溶液滴入0.100molL-1H2SO3溶液(甲基橙作指示剂)中,溶液由红色变为橙色时,发生的主要反应的离子方程式为______。
SO32-+H2O的lgK=______;用0.100molL-1NaOH溶液滴入0.100molL-1H2SO3溶液(甲基橙作指示剂)中,溶液由红色变为橙色时,发生的主要反应的离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10mL浓度为0.1mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
A.水的电离程度始终增大
B.![]() 先增大再减小
先增大再减小
C.c(CH3COOH)与c(CH3COO-)之和始终保持不变
D.当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
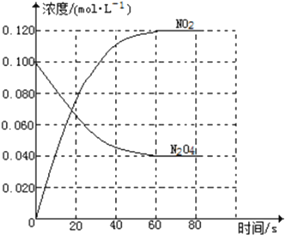
回答下列问题:
(1)反应的△H______0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60s时段,反应速率v(N2O4)为___________molL-1s-1反应的平衡常数K1为___________。
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 molL-1s-1的平均速率降低,经10s又达到平衡。
①T_______100℃(填“大于”“小于”),判断理由是_____。
②列式计算温度T是反应的平衡常数K2___________
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向___________(填“正反应”或“逆反应”)方向移动,判断理由是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素在周期表中的位置如图所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物。
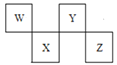
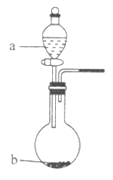
请回答下列问题。
(1)H2Y2的电子式为___________,Z在周期表中的位置___________。
(2)在图中,b的pH约为7,且含有Fe2+和淀粉KI的水溶液,a为H2Y2的水溶液,旋开分液漏斗旋钮,观察到烧瓶中溶液呈蓝色并有红褐色沉淀生成。当消耗2molI-时,共转移3mol电子,该反应的离子方程式是_________________________。
(3)已知:298K时,金属钠与Y2气体反应,若生成1molNa2Y固体时,放出热量414kJ;若生成1molNa2Y2固体时,放出热量511kJ。则由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为_____________。
(4)有人设想利用原电池原理以气体Z2和氢气制备一种重要的化工原料,同时获取电能。假设这种想法可行,用石墨作电极材料,用稀盐酸作电解溶液,则通入Z2的电极为原电池的___________极,其电极反应式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1830年,瑞典化学家塞弗斯托姆从一种铁矿石中得到了一种新元素,并以凡娜迪丝女神(![]() )之名命名为“钒”。钒(
)之名命名为“钒”。钒(![]() )的用途很广,在冶金行业有“第一金属”的美誉。
)的用途很广,在冶金行业有“第一金属”的美誉。
(1)基态钒原子能量最高的电子占据的能级符号为_________。
(2)依据价电子互斥理论推测![]() 的立体构型是______________。
的立体构型是______________。
(3)①化合物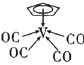 中,中心原子V的价电子与配体提供的电子数之和为18,配体
中,中心原子V的价电子与配体提供的电子数之和为18,配体![]() 不带电荷,且其提供的是大π键的电子,则配体“
不带电荷,且其提供的是大π键的电子,则配体“![]() ”中的大π键可表示为_______。(例如苯中大π键可表示为
”中的大π键可表示为_______。(例如苯中大π键可表示为![]() )
)
②从电负性角度解释![]() 作配体时,配位原子是C而不是O的原因是___________________。
作配体时,配位原子是C而不是O的原因是___________________。
(4)2-巯基烟酸氧钒配合物(如图甲)是有效调节血糖的新型药物的主要成分。
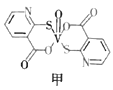
①2-巯基烟酸氧钒配合物中![]() 键长_________(填“大于”“等于”或“小于”)V—O键长,该物质中氮原子的杂化方式是_________________。
键长_________(填“大于”“等于”或“小于”)V—O键长,该物质中氮原子的杂化方式是_________________。
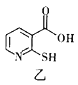
②相同条件下,2-巯基烟酸(如图乙)在水中溶解性好于2-巯基烟酸氧钒配合物的原因是____。
(5)某钒的氧化物的晶胞如图。
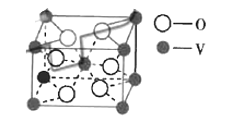
①氧的配位数为_____________。
②已知上述晶胞为立方晶胞,距离最近的钒原子和氧原子间的核间距为![]() ,晶体密度为
,晶体密度为![]() ,则晶胞中底面上的两个氧原子的核间距为__________cm.
,则晶胞中底面上的两个氧原子的核间距为__________cm.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com