
【题目】下列水溶液一定呈中性的是
A. c(H+)=c(OH-)=10-6 mol·L-1的溶液 B. c(H+)=1×10-7mol·L-1的溶液
C. pH=7的溶液 D. 酸与碱恰好完全反应生成正盐的溶液
【答案】A
【解析】
任何温度下中性溶液的本质是c(H+)=c(OH-),据此分析。
A.任何温度下中性溶液的本质是c(H+)=c(OH-),A项正确;
B.已知c(H+)=1×10-7mol/L,题目未给出溶液的温度,无法确定Kw的值,根据c(OH-)=![]() 无法计算c(OH-),不能确定c(H+)与c(OH-)是否一定相等,B项错误;
无法计算c(OH-),不能确定c(H+)与c(OH-)是否一定相等,B项错误;
C.由pH=7可知溶液中c(H+)=10-7mol/L,题目未给出溶液的温度,无法确定Kw的值,根据c(OH-)=![]() 无法计算c(OH-),不能确定c(H+)与c(OH-)是否一定相等,C项错误;
无法计算c(OH-),不能确定c(H+)与c(OH-)是否一定相等,C项错误;
D.强酸与弱碱恰好完全反应所得的正盐属于强酸弱碱盐,在溶液中因水解使溶液显酸性;弱酸与强碱恰好完全反应所得的正盐属于强碱弱酸盐,在溶液中因水解使溶液显碱性,所以酸与碱完全反应生成的正盐溶液不一定显中性,D项错误;答案选A。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】现有前四周期A,B,C,D,E、X六种元素,已知B,C,D,E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题:
(1)写出C,D,E三种原子第一电离能由大到小的顺序为__。
(2)A原子与B,C,D原子形成最简单化合物的稳定性由强到弱的顺序为__,根据价层电子对互斥理论预测BA2D的分子构型为__。
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个BC﹣.与A同族且相差两个周期的元素R的离子位于立方体的恰当位置上,根据其结构特点可知该晶体的化学式为____(用最简正整数表示)。
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如右图所示),其中3种离子晶体的晶格能数据如下表:

根据表格中的数据:判断KCl、MgO、TiN 三种离子晶体熔点从高到低的顺序是__,MgO晶体中一个Mg2+周围和它最邻近且等距离的O2﹣有__个。
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好,离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是__。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
①NaHCO3溶液加水稀释,c(Na+)/ c(HCO3-)的比值保持增大
②浓度均为0.1 mol·L1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)]
③在0.1 mol·L1氨水中滴加0.lmol·L1盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH-)=l0-amol·L-1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32-)均增大
⑤浓度相等的a、NH4HSO4溶液、b、NH4HCO3溶液、c、NH4Cl溶液中的c(NH4+):a >b>c
⑥NaHSO3溶液显酸性,c(Na+)>c(HSO3-)>c(H+)>c(OH-)>c(SO32-)
⑦常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1 mol·L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
⑧pH=3.6的0.1mol/L HX与0.1mol/L NaX的混合溶液中,c(H+)-c(OH-)=c(X-)-c(HX)
A. ②④⑥⑦ B. ②⑤⑦⑧ C. ①③⑤⑥ D. ②⑤⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温条件下,可逆反应:2NO(g)+O2(g)![]() 2NO2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
2NO2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
①单位时间内生成n mol O2的同时生成2n mol NO2②单位时间内生成n mol O2的同时生成2n mol NO③用NO2、NO、O2表示的反应速率的比为2:2:1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态⑥混合气体的压强不再改变的状态⑦混合气体的平均相对分子质量不再改变的状态.
A. ①④⑥⑦ B. ②③⑤⑦ C. ①③④⑤ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A. N2(g)![]() NH3(g)
NH3(g)![]() NH4Cl(aq)
NH4Cl(aq)
B. Fe(s)![]() FeCl2(s)
FeCl2(s)![]() Fe(OH)2(s)
Fe(OH)2(s)
C. MgO(s)![]() MgSO4(aq)
MgSO4(aq)![]() Mg(s)
Mg(s)
D. S(s)![]() SO2(g)
SO2(g)![]() BaSO3(s)
BaSO3(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇: CO(g)+2H2(g) ![]() CH3OH(g),现在实验室模拟该反应并进行分析。
CH3OH(g),现在实验室模拟该反应并进行分析。
(1)下图是该反应在不同温度下CO的转化率随时间变化的曲线。

①该反应的焓变ΔH__________0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数大小关系是K1_______K2 (填 “>”、“<”或“=”)。
③若容器容积不变,下列措施可增加甲醇产率的是______________。
A.升高温度 B.将CH3OH(g)从体系中分离
C.使用合适的催化剂 D.充入He,使体系总压强增大
(2)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响,如图所示
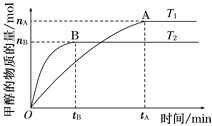
下列说法正确的是________(填序号);
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=nA/tAmol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
(3)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为α,则容器内的压强与起始压强之比为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关事实,与水解反应无关的是
A. 热的纯碱溶液用于清洗油污
B. 氯化铁溶液腐蚀铜板
C. 加热蒸干氯化铁溶液,不能得到氯化铁晶体
D. 用TiCl4和大量水反应,同时加热制备TiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用废弃旧电池的铜帽(主要成分为Zn和Cu)回收Cu并制备ZnO的部分实验过程如图所示:

下列叙述错误的是( )
A. “溶解”操作中可用酸性条件下不断鼓入O2代替H2O2
B. 铜帽溶解后,将溶液加热至沸腾以除去溶液中过量的H2O2
C. 与加入锌粉反应的离子为Cu2+、H+
D. “过滤”操作后,将滤液蒸干、高温灼烧即可制取纯净的ZnO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,改变0.1mol/L弱酸RCOOH溶液的pH,溶液中RCOOH分子的物质的量分数δ(RCOOH)随之改变[已知![]() ,甲酸(HCOOH)]与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是
,甲酸(HCOOH)]与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是

A. 图中M、N两点对应溶液中的c(OH-)比较:前者>后者
B. 丙酸的电离常数K=10-4.88
C. 等浓度的HCOONa和CH3CH2COONa两种溶液的pH比较:前者>后者
D. 将0.1 mol/L的HCOOH溶液与0.1 mol/L的HCOONa溶液等体积混合,所得溶液中:c(Na+)>c(HCOOH)>c(HCOO-)>c(OH-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com