
【题目】对于氨气的催化氧化反应:4NH3 +5O2 =4NO + 6H2O
(1)该反应中的还原剂是________,被还原的元素是_________ ;
(2)用单线桥标出该反应中电子转移的方向和数目;4NH3 +5O2 =4NO + 6H2O_________
(3)若反应转移了2mol电子,则产生的气体在标准状态下体积约为_______。
【答案】NH3(氨气) O(氧或氧元素) 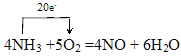 8. 96L
8. 96L
【解析】
在反应4NH3 +5O2 =4NO + 6H2O中,NH3 中的N元素由-3价升高到+2价,O2中的O元素由0价降低到-2价。
(1)该反应中,还原剂是含有化合价降低元素的反应物,被还原的元素是反应物中化合价降低的元素;
(2)用单线桥标出该反应中的电子转移方向,是从反应物中化合价升高元素指向化合价降低元素,数目是得电子总数或失电子总数;
(3)确定本反应的电子转移数目,然后建立NO与电子转移数目关系式,利用反应转移的2mol电子,算出生成NO的物质的量,从而算出其在标准状态下体积。
(1)该反应中,还原剂是含有化合价降低元素的反应物,则还原剂是NH3(氨气),被还原的元素是反应物中化合价降低的O(氧或氧元素)素;答案为:NH3(氨气);O(氧或氧元素);
(2)用单线桥标出该反应中的电子转移和数目为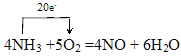 ;答案为:
;答案为: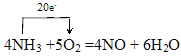 ;
;
(3)由单线桥表示的电子转移方向和数目的反应,可得出如下关系式:NO——5e-,现反应中转移2mol电子,则n(NO)=![]() =0.4mol,V(NO)=0.4mol×22.4L/mol=8. 96L。答案为:8. 96L。
=0.4mol,V(NO)=0.4mol×22.4L/mol=8. 96L。答案为:8. 96L。


科目:高中化学 来源: 题型:
【题目】某化学实验小组用酸性KMnO4溶液和草酸(H2C2O4)溶液反应,研究外界条件反应速率的影响,实验操作及现象如下:
编号 | 实验操作 | 实验现象 |
I | 向一支试管中先加入1mL 0.01 mol/L酸性 KMnO4溶液,再加入1滴3mol/L硫酸和9滴蒸馏水,最后加入1mL 0.1mol/L草酸溶液 | 前10min内溶液紫色无明显变化,后颜色逐渐变浅, 30 in后几乎变为无色 |
II | 向另一支试管中先加入1mL 0.01mol/L酸性 KMnO4溶液,再加入10滴3mol/L硫酸,最后加入1mL 0.1mol/L草酸溶液 | 80s内溶液紫色无明显变化,后颜色迅速变浅,约150s后几乎变为无色 |
(1)高锰酸钾与草酸反应的离子方程式:______________________________________
(2)由实验I、II可得出的结论是____________________________。
(3)关于实验II中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的Mn2+对反应有催化作用。利用提供的试剂设计实验III,验证猜想。
提供的试剂:0.01mol/L酸性 KMnO4溶液,0.1mol/L草酸溶液,3mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水
① 补全实验III的操作:向试管中先加入1mL 0.01mol/L酸性 KMnO4溶液,______,最后加入1mL 0.1mol/L草酸溶液。
② 若猜想成立,应观察到的实验现象是______。
(4)该小组拟采用如图所示的实验方案继续探究外界条件对反应速率的影响。
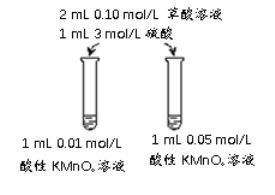
① 他们拟研究的影响因素是______。
② 你认为他们的实验方案______(填“合理”或“不合理”),理由是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室药品必须按规定存放,下列对错误存放后出现现象的解释合理的是( )
A.石灰水敞口存放,出现白色固体:![]()
B.浓硝酸存放于无色细口瓶中,颜色变黄:![]()
C.酸化的硫酸亚铁溶液长时间存放,溶液变黄:![]()
D.将氨水和浓盐酸存放在同一个药品柜中,柜壁出现白色固体:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某工业废水中含有大量FeSO4,较多的CuSO4, 以及部分污泥,通过下列流程可从该废水中回收FeSO4·7H2O晶体及金属Cu。
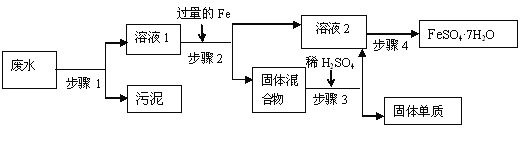
(1)步骤1的主要操作是______,(填操作名称)需用到的玻璃仪器除烧杯外还有_______。
(2)步骤2中发生反应的化学方程式为___________
(3)步骤3中发生反应的化学方程式为_______
(4)步骤4中涉及的操作是:蒸发浓缩、________、过滤、洗涤、烘干。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S是一种大气污染物。工业尾气中含有H2S,会造成严重的环境污染;未脱除H2S的煤气,运输过程中还会腐蚀管道。
(1)干法氧化铁脱硫是目前除去煤气中H2S的常用方法,其原理如图所示。
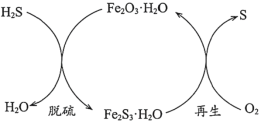
①下列说法正确的是____________(填序号)。
a.单质硫为淡黄色固体
b.脱硫反应为3H2S+Fe2O3·H2O=3H2O+Fe2S3·H2O
c.再生过程中,硫元素被还原
d.脱硫过程中,增大反应物的接触面积可提高脱硫效率
②从安全环保的角度考虑,再生过程需控制反应温度不能过高的原因是_______。
(2)电化学溶解一沉淀法是一种回收利用H2S的新方法,其工艺原理如下图所示。
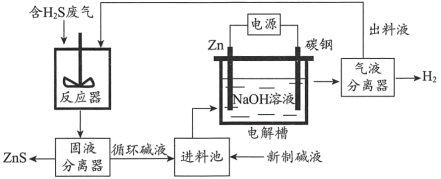
已知: Zn与强酸、强碱都能反应生成H2;Zn(II)在过量的强碱溶液中以[Zn(OH)4]2-形式存在。
①锌棒连接直流电源的____________(填“正极”或“负极”)。
②反应器中反应的离子方程式为____________。
③电解槽中,没接通电源时已经有H2产生,用化学用语解释原因:___________。
(3)常用碘量法测定煤气中H2S的含量,其实验过程如下:
i.将10L煤气通入盛有100mL锌氨络合液的洗气瓶中,将其中的H2S全部转化为ZnS沉淀,过滤;
ii.将带有沉淀的滤纸加入盛有15mL 0.1mol/L碘标准液、200mL水和10mL盐酸的碘量瓶中,盖上瓶塞,摇动碘量瓶至瓶内滤纸摇碎,置于暗处反应10 min后,用少量水冲洗瓶壁和瓶塞。(已知:ZnS+I2=ZnI2+S)
iii.用0.1mol/L Na2S2O3标准液滴定,待溶液呈淡黄色时,加入1mL淀粉指示剂,继续滴定至终点。(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
①i中,将煤气中的H2S转化为ZnS的目的是____________。
②滴定终点的现象是__________________。
③若消耗Na2S2O3标准液的体积为20mL,则煤气中![]() 的含量为_______________mg/m3。
的含量为_______________mg/m3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关硫及其化合物的说法中正确的是
A.浓硫酸具有吸水性,可做干燥剂,如可干燥氯气、二氧化硫、氨气等
B.浓硫酸与炭共热反应,仅体现了浓硫酸的强氧化性
C.SO2 和 Cl2 均可使品红溶液褪色,但溶有 SO2 的品红溶液加热后恢复红色,说明 SO2 的氧化性没有 Cl2强
D.以 FeS2 为原料生产硫酸过程中,要用到沸腾炉、接触室、吸收塔等设备,所涉及的反应均为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应2A(s)+3B(g)![]() C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列叙述正确的是
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列叙述正确的是
①增加A的量,平衡向逆反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
A.①②B.④C.③D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:H2(g)+![]() O2(g)=H2O(g) ΔH1
O2(g)=H2O(g) ΔH1
![]() N2(g)+O2(g)=NO2(g) ΔH2
N2(g)+O2(g)=NO2(g) ΔH2
![]() N2(g)+3/2H2(g)=NH3(g) ΔH3
N2(g)+3/2H2(g)=NH3(g) ΔH3
则反应2NH3(g)+![]() O2(g)=2NO2(g)+3H2O(g)的ΔH为( )
O2(g)=2NO2(g)+3H2O(g)的ΔH为( )
A. 2ΔH1+2ΔH2-2ΔH3B. ΔH1+ΔH2-ΔH3
C. 3ΔH1+2ΔH2+2ΔH3D. 3ΔH1+2ΔH2-2ΔH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有以下物质:①石墨;②氯化氢气体;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;⑦氯化铁溶液;⑧纯醋酸;⑨氧化钠固体;⑩铝。
(1)属于非电解质的是______________;属于强电解质的是__________;属于弱电解质的是___________。(用序号填空)
(2)写出物质⑥溶于水溶液显碱性的原因_______(用离子方程式和简要文字说明作答)
(3)写出物质⑥和⑧在水中反应的离子方程式:_____________。
(4)配制溶液⑦时通常将⑦先溶于___________,然后再加水稀释,通过增加溶液中_______的浓度以防止其发生水解。
(5)浓度、体积相同的②和⑧的溶液,加入相同形状且足量的Zn粒,反应速率快的是___(用序号填空);pH值、体积相同的②和⑧的溶液时,产生气体的量多的是________。(用序号填空)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com