
【题目】对可逆反应2A(s)+3B(g)![]() C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列叙述正确的是
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列叙述正确的是
①增加A的量,平衡向逆反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
A.①②B.④C.③D.④⑤
【答案】B
【解析】
①A为固体不影响化学平衡;
②反应是放热反应,升温平衡逆向进行,反应速率增大;
③反应前后气体体积不变,改变压强,平衡不动,正逆反应速率增大;
④增加B,平衡正向进行,反应速率增大;
⑤加入催化剂改变反应速率不改变化学平衡。
①A为固体不影响化学平衡,增加A的量,平衡不移动,故①错误;
②反应是放热反应,升温平衡逆向进行,反应速率增大,正逆反应速率都增大,故②错误;
③反应前后气体体积不变,压强增大一倍,平衡不移动,v(正)、v(逆)增大,故③错误;
④增加B,平衡正向进行,反应速率增大,v(正)>v(逆),故④正确;
⑤加入催化剂改变反应速率不改变化学平衡,B的转化率不变,故⑤错误;
故选B。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.稀醋酸中加入少量醋酸钠能增大醋酸的电离程度
B.25 ℃时0.1 mol/L的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱
C.NaHCO3溶液中溶质的电离方程式为NaHCO3===Na++H++CO![]()
D.室温下,对于0.10 mol·L-1的氨水,加水稀释后,溶液中c(NH![]() )·c(OH-)变大
)·c(OH-)变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.NaCl溶液中混有Na2CO3、Na2SO4,为检验两种物质的存在,请你根据所选择的试剂,按实验步骤的先后顺序写出相应的化学方程式:
①______________________________;
②______________________________;
③________________________________。
II.取100.0 mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到16.84g沉淀,用过量稀硝酸处理后沉淀质量减少至6.99g,同时溶液中有气泡产生。试求:原混合液中Na2SO4的物质的量浓度为________________;(写出计算列式的过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于氨气的催化氧化反应:4NH3 +5O2 =4NO + 6H2O
(1)该反应中的还原剂是________,被还原的元素是_________ ;
(2)用单线桥标出该反应中电子转移的方向和数目;4NH3 +5O2 =4NO + 6H2O_________
(3)若反应转移了2mol电子,则产生的气体在标准状态下体积约为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池能将污水中的乙二胺(H2NCH2CH2NH2)氧化成环境友好的物质,示意图如图所示,a、b均为石墨电极。下列说法错误的是
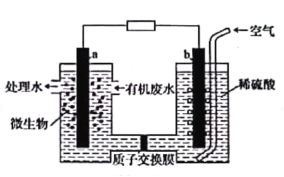
A.a电极的电极反应为H2NCH2CH2NH2-16e-+4H2O=2CO2↑+N2↑+16H+
B.电池工作时质子通过交换膜由负极区向正极区移动
C.a电极上的电势比b电极上的电势低
D.电池工作时b电极附近溶液的pH保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学原理在防止金属腐蚀、能量转换、物质制备等方面应用广泛。
(1)钢闸门在海水中易被腐蚀,常用以下两种方法减少其腐蚀:
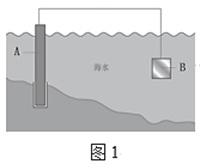
①图1中,A为钢闸门,材料B可以选择___(填字母序号)。
a.碳棒 b.铜板 c.锌板
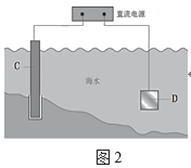
②图2中,钢闸门C做___极。用氯化钠溶液模拟海水进行实验,D为石墨块,则D电极反应式为___,检验该电极反应产物的方法___。
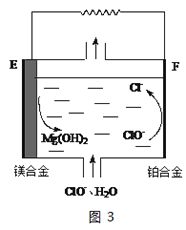
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。E为该燃料电池的___极(填“正”或“负”)。F电极上的电极反应式为___。
(3)利用电化学法生产硫酸,可使绝大多数单质硫直接转化为SO3,在生产硫酸的同时还能化学发电。图4为电化学法生产硫酸的工艺示意图,电池以固体金属氧化物作电解质,该电解质能传导O2-离子。
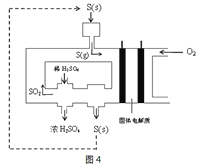
①正极每消耗4.48LO2(标准状况下),电路中转移电子的数目为___。
②S(g)在负极生成SO3的电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,2.24LCH3OH分子中共价键的数目为0.5NA
B.100g46%的甲酸(HCOOH)水溶液中所含的氧原子数目为5NA
C.lmol铁粉高温下与足量水蒸气反应,转移电子数为3NA
D.2molSO2和lmolO2在催化剂作用下充分反应所得分子总数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com