
һ�������£�ͨ�����з�Ӧ��ʵ��ȼú��������Ļ��գ�
2CO(g)+SO2(g)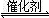 2CO2(g)+S(l) ��H
2CO2(g)+S(l) ��H
��1����֪2CO(g)+O2(g)= 2CO2(g) ��H1=��566kJ?mol��1
S(l) +O2(g)= SO2(g) ��H2=��296kJ?mol��1
��Ӧ�Ȧ�H= kJ?mol��1��
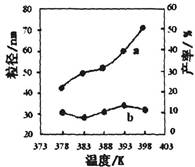
��2������������ͬ��������ͬʱ��SO2��ת�����淴Ӧ�¶ȵı仯��ͼa��260��ʱ ����Fe2O3��NiO��Cr2O3����������Ӧ������졣Fe2O3��NiO����������ʹSO2��ת���ʴﵽ��ߣ������Ǽ۸����أ�ѡ��Fe2O3����Ҫ�ŵ��� ��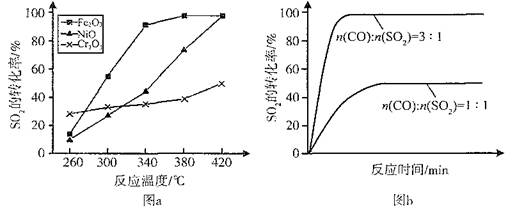
��3������С����380�桢Fe2O3������ʱ���о��˲�ͬͶ�ϱ�[n(CO)��n(SO2)]��SO2ת���ʵ�Ӱ�죬�����ͼb�����ڴ������ͼ�л���n(CO)��n(SO2)="2��1" ʱ��SO2ת���ʵ�Ԥ�ڱ仯���ߡ�
��4����ҵ�ϻ�����Na2SO3��Һ���������е�SO2��Na2SO3+SO2+H2O=2NaHSO3��ij�¶�����1.0mol?L��1 Na2SO3��Һ���մ�����SO2������Һ��c(SO32��)����0.2mol?L��1ʱ���������������½���Ӧ�������ռ���
�ٴ�ʱ��Һ��c(HSO3��)ԼΪ______mol?L��1��
�ڴ�ʱ��ҺpH=______������֪���¶���SO32��+H+ HSO3����ƽ�ⳣ��K="8.0" �� 106 L?mol��1������ʱSO2��H2SO3��Ũ�Ⱥ��Բ��ƣ�
HSO3����ƽ�ⳣ��K="8.0" �� 106 L?mol��1������ʱSO2��H2SO3��Ũ�Ⱥ��Բ��ƣ�
��16�֣�
��1����270 ��3�֣�
��2��Cr2O3 ��3�֣� Fe2O3������ʱ������Խϵ��¶ȿɻ�ýϸ�SO2��ת���ʣ��Ӷ���Լ������Դ��3�֣�
��3������ͼ ��3�֣�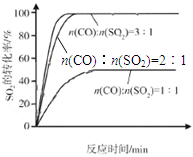
��4����1.6 ��2�֣� ��6 ��2�֣�
���������������1���۲��Ȼ�ѧ����ʽ֮��Ĺ�ϵ��������֪��1���Ȼ�ѧ����ʽ��ȥ��2���Ȼ�ѧ����ʽʱ���ܹ�ԼȥO2(g)�õ�2CO(g)+SO2(g)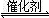 2CO2(g)+S(l)�����ݸ�˹���ɣ��÷�Ӧ�Ȧ�H=��H1����H2=��270kJ?mol��1����2����ͼa��֪��260��ʱƽ��ת���ʣ�Cr2O3> Fe2O3>NiO���ɴ��ƶ�Cr2O3������ʱ��Ӧ������죻��ͼ��֪��Fe2O3��NiO����������ʹSO2��ת���ʴﵽ��ߣ���SO2��ת������ͬʱ����Ӧ�¶ȣ�Fe2O3<NiO������Fe2O3������ʱ����Ҫ�ŵ�������Խϵ��¶ȿɻ�ýϸ�SO2��ת���ʣ��Ӷ���Լ������Դ����3����ͼb��֪������������ͬʱ������n(CO)��n(SO2)�ı�ֵ����������CO��Ӧ��Ũ�ȣ���������Ӧ���ʣ����̴ﵽƽ���ʱ�䣬��ʹƽ��������Ӧ��Ӧ�����ƶ���ʹSO2��ת������������ͼa��380��ʱSO2��ת������ߣ�����n(CO)��n(SO2)�ı�ֵΪ2��1��Ϊ3��1ʱ��SO2��ƽ��ת���ʻ�������ȫ��ͬ��ֻ�Ǵﵽƽ���ʱ�����̣��ɴ˿�����ͼb�л����й��¶ȶԷ�Ӧ���ʺ�ƽ���ƶ���Ӱ��ͼ��4�������⣬Na2SO3��NaHSO3����ǿ����ʣ������ƶϷ�Ӧ������������ʼŨ�ȡ��仯Ũ�ȡ������Լ�ʱŨ�ȣ���
2CO2(g)+S(l)�����ݸ�˹���ɣ��÷�Ӧ�Ȧ�H=��H1����H2=��270kJ?mol��1����2����ͼa��֪��260��ʱƽ��ת���ʣ�Cr2O3> Fe2O3>NiO���ɴ��ƶ�Cr2O3������ʱ��Ӧ������죻��ͼ��֪��Fe2O3��NiO����������ʹSO2��ת���ʴﵽ��ߣ���SO2��ת������ͬʱ����Ӧ�¶ȣ�Fe2O3<NiO������Fe2O3������ʱ����Ҫ�ŵ�������Խϵ��¶ȿɻ�ýϸ�SO2��ת���ʣ��Ӷ���Լ������Դ����3����ͼb��֪������������ͬʱ������n(CO)��n(SO2)�ı�ֵ����������CO��Ӧ��Ũ�ȣ���������Ӧ���ʣ����̴ﵽƽ���ʱ�䣬��ʹƽ��������Ӧ��Ӧ�����ƶ���ʹSO2��ת������������ͼa��380��ʱSO2��ת������ߣ�����n(CO)��n(SO2)�ı�ֵΪ2��1��Ϊ3��1ʱ��SO2��ƽ��ת���ʻ�������ȫ��ͬ��ֻ�Ǵﵽƽ���ʱ�����̣��ɴ˿�����ͼb�л����й��¶ȶԷ�Ӧ���ʺ�ƽ���ƶ���Ӱ��ͼ��4�������⣬Na2SO3��NaHSO3����ǿ����ʣ������ƶϷ�Ӧ������������ʼŨ�ȡ��仯Ũ�ȡ������Լ�ʱŨ�ȣ���
SO32��+SO2+H2O=2HSO3��
��ʼŨ�ȣ�mol/L�� 1.0 0
�仯Ũ�ȣ�mol/L�� 0.8 1.6
�����Լ�ʱŨ�ȣ�mol/L�� 0.2 1.6
������Լ�ʱ��c(HSO3��)=1.6mol/L
����SO32��+H+ HSO3����ƽ�ⳣ��K= c(HSO3��)/[ c(SO32��)? c(H+)]����c(H+)= c(HSO3��)/[ c(SO32��)?K)]������c(HSO3��)=1.6mol/L��c(SO32��)=0.2mol/L�����¶���K="8.0" �� 106 L?mol��1����c(H+)=1.6/(0.2��8.0 �� 106) mol/L=10��6 mol/L��������Һ��pH="��lg" c(H+)=������6��=6��
HSO3����ƽ�ⳣ��K= c(HSO3��)/[ c(SO32��)? c(H+)]����c(H+)= c(HSO3��)/[ c(SO32��)?K)]������c(HSO3��)=1.6mol/L��c(SO32��)=0.2mol/L�����¶���K="8.0" �� 106 L?mol��1����c(H+)=1.6/(0.2��8.0 �� 106) mol/L=10��6 mol/L��������Һ��pH="��lg" c(H+)=������6��=6��
���㣺���黯ѧ��Ӧԭ�����漰��˹���ɡ����ͼ������������¶ȶԷ�Ӧ���ʼ���Ӧ��ת���ʵ�Ӱ����ɡ�����ѡ��������ŵ㡢�����ض��¶��·�Ӧ����ȶԷ�Ӧ���ʺ�ƽ���ƶ���Ӱ��ͼ�����ʵ�������Ũ�ȣ������ӷ���ʽ�����е�Ӧ�á����ݷ�Ӧ��仯Ũ�ȼ���������ı仯Ũ�ȡ��������ݷ����йؼ��㡢����ƽ�ⳣ�����йؼ��㡢��ҺpH�ļ���ȡ�


 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ϳɰ���ҵ�Թ���������Ҫ���壬�������ᡢ�ϳ���ά�Լ�Ⱦ�ϵ�
��1����֪ijЩ��ѧ���ļ����������±���
| ��ѧ�� | N��N | H��H | N��H |
| ����kJ��mol��1 | 946 | 436 | 390 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ʴ���
������ʵ��д�����з�Ӧ���Ȼ�ѧ����ʽ��
��1��1molC2H4(g)������O2(g)��Ӧ����CO2��g����H2O(l)���ų�1411kJ������
��2��1molC2H5OH(l)������O2(g)��Ӧ����CO2��g����H2O(l)���ų�1366��8kJ������
��3��2molAl��s��������O2(g)��Ӧ����Al2O3��s�����ų�1669��8kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�ྦྷ�裨�赥�ʵ�һ�֣�����Ϊ�����Ӵ��õĻ�ʯ�����Ʊ��и�������SiCl4Ϊ������������Ⱦ�ܴ�����ˮǿ��ˮ�⣬�ų��������ȡ��о���Ա����SiCl4ˮ�����ɵ�����ͱ���ۣ���Ҫ�ɷ�ΪBaCO3���Һ�������þ�����ӣ��Ʊ�BaCl2��2H2O�������������£�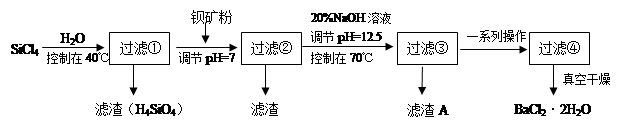
��֪��
�ٳ�����Fe3+��Mg2+��ȫ������pH�ֱ���3.4��12.4
��BaCO3����Է���������197��BaCl2��2H2O����Է���������244
�ش��������⣺
��1��SiCl4����ˮ�ⷴӦ�Ļ�ѧ����ʽΪ_______________________________________
��2����H2��ԭSiCl4��������ȡ���ȺܸߵĹ裬����Ӧ����1mol����ת��ʱ����59KJ��������÷� Ӧ���Ȼ�ѧ����ʽΪ_____________________________________________
��3���ӱ���۲�����pH=7��Ŀ���Ǣ� ����
��4�����ˢں����Һ��Fe3+Ũ��Ϊ ����Һ�¶�25�棬Ksp[Fe(OH)3]=2.2��10-38��
��5����������A�����ӷ���ʽ__________________________________________
��6����ʽ�����10�ֺ�78.8% BaCO3�ı�������������������BaCl2��2H2O������Ϊ���ٶ֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
I����¯������ұ��������Ҫ��������������Ҫ��ӦΪ��
Fe2O3(s) + 3CO(g) 2Fe(s)+3CO2(g) ��H
2Fe(s)+3CO2(g) ��H
��1����֪����Fe2O3(s) + 3C(ʯī)="2Fe(s)" + 3CO(g) ��H1
��C(ʯī��+ CO2(g) = 2CO(g) ��H2
���H___________________(�ú���H1 ����H2�Ĵ���ʽ��ʾ)��
��2����¯������Ӧ��ƽ�ⳣ������ʽK=____________________________��
��3����ij�¶�ʱ���÷�Ӧ��ƽ�ⳣ��K=64����2L�����ܱ����������У��ֱ��±���ʾ�������ʣ���Ӧ����һ��ʱ���ﵽƽ�⡣
| | Fe2O3 | CO | Fe | CO2 |
| ��/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| ��/mol | 1.0 | 1.5 | 1.0 | 1.0 |
| ��� | �¶�/K | ��Ӧʱ��/h | ��Ӧ�����ʵ������ | ʵ��Ŀ�� |
| �� | 378 | 4 | 3��1 | ʵ��ں͢�̽��________ ______________________ ʵ��ں�__________̽�� ��Ӧʱ��Բ��ʵ�Ӱ�졣 |
| �� | 378 | 4 | 4��1 | |
| �� | 378 | 3 | _______ | |
| �� | 398 | 4 | 4��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�Ҵ������DZ��㷺ʹ�õ��������ȼ�ϣ���ҵ�����Ҵ���һ�ַ�Ӧԭ��Ϊ��
2CO(g) + 4H2(g) CH3CH2OH(g) + H2O(g) ��H =" ��256.1" kJ��mol��1
CH3CH2OH(g) + H2O(g) ��H =" ��256.1" kJ��mol��1
��֪��CO(g) + H2O(g) CO2(g)+H2(g) ��H=" ��41.2" kJ��mol��1
CO2(g)+H2(g) ��H=" ��41.2" kJ��mol��1
��1����CO2(g)��H2(g)Ϊԭ��Ҳ�ɺϳ��Ҵ������Ȼ�ѧ����ʽ���£�
2CO2(g) +6H2(g) CH3CH2OH(g) +3H2O(g) ��H = ��
CH3CH2OH(g) +3H2O(g) ��H = ��
��2������ʹ���Ҵ����Ͳ����ܼ���NOx���ŷţ���ʹNOx����Ч������Ϊ�����������Ҫ���⡣
��ij�о�С����ʵ������Ag�C ZSM�C 5Ϊ���������NOת��ΪN2��ת�������¶ȱ仯�������ͼ������ʹ��CO���¶ȳ���800�棬����NO��ת���ʽ��ͣ�����ܵ�ԭ��Ϊ ����n(NO)/n(C O)=1�������£�Ӧ���Ƶ�����¶��� ���ҡ�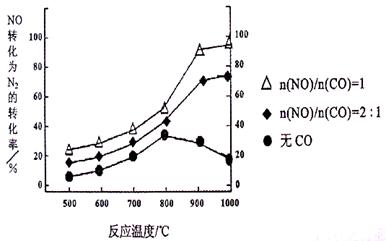
���û���̿��ԭ��������������йط�ӦΪ��C (s) +2NO2(g) N2 (g) + CO2 (g)��ij�о�С����ij�ܱ������м��������Ļ���̿��NO������( T1��)�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
N2 (g) + CO2 (g)��ij�о�С����ij�ܱ������м��������Ļ���̿��NO������( T1��)�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
| �� Ũ��/mol?L��1 ʱ��/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
50 mL 0��50 mol��L��1������50 mL 0��55 mol��L��1NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����кͷ�Ӧ�ķ�Ӧ�ȡ�
�ش��������⣺
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ��������� ��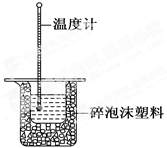
��2���ձ�����������ĭ���ϵ������� ��
��3�����ձ����粻��Ӳֽ�壬��õ��кͷ�Ӧ�ķ�Ӧ�ȵ���ֵ (�ƫ�� ��ƫС������Ӱ�족)��
��4��ʵ���и���55 mL 0��50 mol��L��1�����50 mL 0��55 mol��L��1NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų������� (���ȡ�����ȡ�)��
��5������ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ��������ʵ�飬��õ��кͷ�Ӧ�ķ�Ӧ����ֵ�� (�ƫ��ƫС������Ӱ�족)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����β���е��ж�����NO��CO����һ�������¿ɷ�����Ӧ����N2��CO2�����й��ڴ˷�Ӧ��˵���У���ȷ����
| A����Сѹǿ������Ӧ���� | B������ѹǿ�ܼ�С��Ӧ���� |
| C��ʹ���ʵ��Ĵ���������Ӧ���� | D�������¶ȶԷ�Ӧ������Ӱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����¡����ݣ�2L�����ܱ������г���2molX��һ������Y��������Ӧ��2X(g)��Y(g)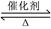 2Z(g)
2Z(g)
��H��0��4min��ﵽƽ��c(X)��0.2mol��L-1����X��Y��ת������ȡ�����˵���в���ȷ���ǣ� ��
| A���ﵽƽ��ʱ���ٳ���1molX����Ӧ���ʱ䱣�ֲ��� |
| B����Y��ʾ4min�ڵķ�Ӧ����Ϊ0.1 mol��L-1��min-1 |
| C�����������г���1molZ���ﵽ��ƽ�⣬c(X)��c(Y)��2��1 |
| D��4min���������¶ȣ�ƽ�ⳣ��K���� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com