
����Ŀ����֪ijNaOH�����к���NaCl���ʣ�Ϊ�ⶨ������NaOH�������������������²���ʵ�飺
�� ����1.000 g��Ʒ����ˮ�����250 mL��Һ��
�� ȷ��ȡ25.00 mL������Һ����ƿ�У�
�� �μӼ��η�̪��Һ��
�� ��0.1000 mol/L �ı�����ζ����Σ�ÿ����������������¼���£�
�ζ���� | ����Һ�����mL�� | �����������Һ�������mL�� | |
�ζ�ǰ���� | �ζ������ | ||
1 | 25.00 | 0.50 | 20.60 |
2 | 25.00 | 6.00 | 26.00 |
3 | 25.00 | 1.10 | 21.00 |
��ش�
��1����_______�ζ��ܣ�������ʽ��������ʽ����ʢװ0.1000 mol/L�������Һ��
��2���жϵζ��յ㵽��ʱ������_________��
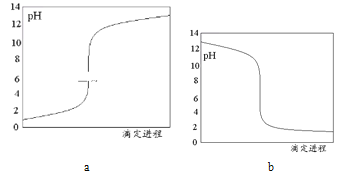
��3���õζ����̵ĵζ����������е�______��ѡ����a������b������
��4������������������ⶨ���ƫ�ߵ���__________��
a �ζ�ǰ������ˮ��ϴ��ƿ
b ������ƿʱ������ƿ����Һ����
c ���ڵζ������в�����������Һ������ƿ��
��5��ͨ�������֪���ռ���Ʒ�Ĵ���Ϊ______________��
���𰸡���ʽ ��ƿ�е���Һ�ɺ��Ϊ��ɫ b c 80.0%
��������
(1)���������ԣ�Ӧ�ü�ʽ�ζ���ʢװ0.10mol/L�������Һ��
(2)�μӼ��η�̪��NaOH��Һ�Ժ�ɫ�����ζ����յ�ʱ����Һ�����ԣ���Һ��Ϊ��ɫ��
(3)��ƿ��ʢ�ŵ���NaOH��Һ�����Եζ�ʱ��Һ��pH��С��
(4)����c(NaOH)=![]() ������������
������������
(5)���ݵζ�ԭ�����з�����
(1)���������ԣ�Ӧ����ʽ�ζ���ʢװ0.10mol/L�������Һ��
(2)�μӼ��η�̪��NaOH��Һ�Ժ�ɫ�����ζ����յ�ʱ����Һ�����ԣ���Һ��Ϊ��ɫ����ζ��յ㵽��ʱ����������ƿ�е���Һ�ɺ��Ϊ��ɫ��
(3)��ƿ��ʢ�ŵ���NaOH��Һ�����Եζ�ʱ��Һ��pH��С����ͼ��֪b���߷��ϣ�
(4)����c(NaOH)=![]() �������
�������
a���ζ�ǰ������ˮ��ϴ��ƿ�������Ӱ�죬��a����
b��������ƿʱ������ƿ����Һ���������ƫ�ͣ���b����
c�����ڵζ������в�����������Һ������ƿ�⣬��Ҫ��������ᣬ���ƫ�ߣ���c��ȷ��
�ʴ�Ϊc��
(5)ͼ�����ݷ�����֪���ζ�ǰ�����ı���Һ����ֱ�Ϊ��20.60mL-0.50mL=20.10mL��26.00mL-6.00mL=20.00mL��21.00mL-1.10mL=19.90mL��ƽ���������=![]() =20.
=20.![]() 00mL���������ƺ��Ȼ������ʵ�����ͬ����250mL��Һ�����������������ʵ���=0.0200L��0.10mol/L��
00mL���������ƺ��Ȼ������ʵ�����ͬ����250mL��Һ�����������������ʵ���=0.0200L��0.10mol/L��![]() =0.020mol��
=0.020mol��
����������������=![]() ��100%=80%��
��100%=80%��


 ������������ϵ�д�
������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ���ѧ��������һ�����͵ĸ߱�����п-����Һ����أ��乤��ԭ��ʾ��ͼ���¡�ͼ����Һ���ɴ���������Һ����ߵ�ص�������������������ȷ����
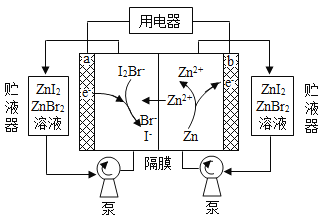
A. �ŵ�ʱ��a�缫��ӦΪ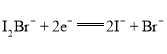
B. �ŵ�ʱ����Һ�����ӵ���Ŀ����
C. ���ʱ��b�缫ÿ����![]() ����Һ����
����Һ����![]() ������
������
D. ���ʱ��a�缫�����Դ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���һ��2 L���ܱ������У�����4 mol A��2 mol B������Ӧ��
3A(g)��2B(g)![]() 4C(s)��2D(g)��5min��ﵽƽ�⣬�������1.6 mol C��������˵����ȷ����
4C(s)��2D(g)��5min��ﵽƽ�⣬�������1.6 mol C��������˵����ȷ����
A. �÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ��K��![]()
B. ��ʱ��B��ƽ��ת������40%
C. �������ϵ��ѹǿ��ƽ�������ƶ�����ѧƽ�ⳣ������
D. ����ƽ����ϵ�м�������C���������淴Ӧ���ʾ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��������£���һ����![]() ��
��![]() �Ļ������ͨ��һ�ݻ�Ϊ2L���ܱ������У���ø����ʵ�Ũ����ʱ��仯��ϵ��ͼ��ʾ������˵����ȷ����
�Ļ������ͨ��һ�ݻ�Ϊ2L���ܱ������У���ø����ʵ�Ũ����ʱ��仯��ϵ��ͼ��ʾ������˵����ȷ����![]()
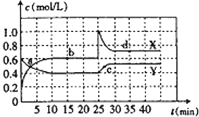
A.ͼ�е����������У�Y�DZ�ʾ![]() Ũ����ʱ��ı仯����
Ũ����ʱ��ı仯����
B.ǰ10min�ڣ���![]() ��ʾ�Ļ�ѧ��Ӧ����Ϊ
��ʾ�Ļ�ѧ��Ӧ����Ϊ![]()
C.��25minʱ����Ӧ�ı��������������![]() ��Ũ��
��Ũ��
D.a��b��c��d�ĸ����У���a��b��d��Ļ�ѧ��Ӧ����ƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��pH=2��A��B��������Һ��1mL���ֱ��ˮϡ�͵�1000mL�� ��pHֵ����Һ���V�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�
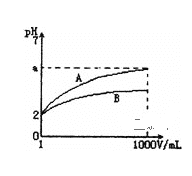
A.A��B������Һ�����ʵ���Ũ��һ�����
B.ϡ�ͺ�A��Һ�����Ա�B��Һǿ
C.a=5ʱ��A��ǿ�ᣬB������
D.��A��B�������ᣬ�����ԣ�A��B
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ���������ȷ����
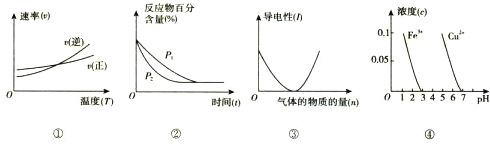
A. ����ͼ���жϷ�ӦA2(g)+3B2(g) ![]() 2AB3(g)�� ��H>0
2AB3(g)�� ��H>0
B. ͼ���ɱ�ʾѹǿ(P)�Է�Ӧ2A(g)+2B(g) ![]() 3C(g)+D(s)��Ӱ��
3C(g)+D(s)��Ӱ��
C. ͼ���ɱ�ʾ�������Һͨ�백��ʱ����Һ�������氱�����ı仯
D. ����ͼ�ܣ���ȥCuSO4��Һ�е�Fe3+���ɼ���CuO����pH��3��5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�з�������ͼ�����( )

A. N2(g)+3H2(g)![]() 2NH3(g) ��H=-Q1kJ��mol-1(Q1>0)
2NH3(g) ��H=-Q1kJ��mol-1(Q1>0)
B. 2SO3(g)![]() 2SO2(g)+O2(g) ��H=+Q2kJ��mol-1(Q2>0)
2SO2(g)+O2(g) ��H=+Q2kJ��mol-1(Q2>0)
C. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ��H=-Q3kJ��mol-1(Q3>0)
4NO(g)+6H2O(g) ��H=-Q3kJ��mol-1(Q3>0)
D. H2(g)+CO(g)![]() C(s)+H2O(g) ��H=+Q4kJ��mol-1(Q4>0)
C(s)+H2O(g) ��H=+Q4kJ��mol-1(Q4>0)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2C2O4ˮ��Һ�в������ķֲ���������pH��ϵ��ͼ��ʾ������˵����ȷ����

A.��H2C2O4��Һ�еμ�NaOH��Һ��pH��2.5��c(H2C2O4)��c(C2O42��)>c(HC2O4��)
B.��ͼ��֪��H2C2O4��Ka2��10��4.2
C.��H2C2O4��Һ�еμ�NaOH��Һ��pH��7������Һ�У�2c(C2O42��)>c(Na��)
D.��0.01 mol��L��1��H2C2O4��Һ��0.02 mol��L��1 NaOH��Һ�������Ϻ����Һ�У�c(OH��)��c(H��)��c(HC2O4��)��2c(H2C2O4)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���һ���������ܱ������г���1molN2��3molH2���������з�Ӧ��N2(g)+3H2(g)2NH3(g)����Ӧ�ﵽƽ��ı�����������NH3����ƽ��Ũ�Ȳ��ı���ǣ� ��
A.�����¶Ⱥ�����ѹǿ���䣬����1molNH3(g)
B.�����¶Ⱥ�����������䣬����1molNH3(g)
C.�����¶Ⱥ�����ѹǿ���䣬����1molN2(g)
D.�����¶Ⱥ�����ѹǿ���䣬����1molAr(g)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com