
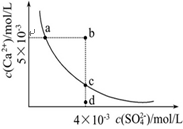


科目:高中化学 来源:不详 题型:单选题
| A.稀释前,溶液 pH:①>② = ③ |
| B.稀释前,溶液中溶质的物质的量浓度:③>① =② |
| C.稀释后,溶液 pH:①>② = ③ |
| D.稀释后,溶液中溶质的物质的量浓度:③>① =② |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.40 mL 1 mol/L的BaCl2溶液 |
| B.30 mL 2 mol/L的Ba(OH)2溶液 |
| C.10 mL纯水 |
| D.50 mL 0.1 mol/L的H2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
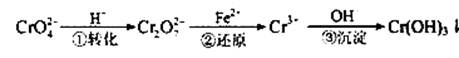
 Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O Cr3+(aq)+3OH—(aq)
Cr3+(aq)+3OH—(aq)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
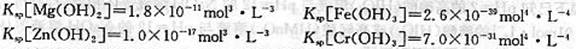
| A.Cr3+ | B.Fe3+ | C.Zn2+ | D.Mg2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
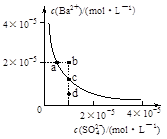
| A.加入Na2SO4可以使溶液由a点变到b点 |
| B.通过蒸发可以使溶液由d点变到c点 |
| C.d点无BaSO4沉淀生成 |
| D.a点对应的BaSO4的Ksp大于c点对应的Ksp |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 mAn+(aq)+nBm-(aq) [An+]m·[Bm-]n=Ksp
mAn+(aq)+nBm-(aq) [An+]m·[Bm-]n=Ksp查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
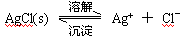
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com