
分析 根据常见的黑色粉末有:氧化铜、碳、二氧化锰等,红色物质有氧化铁、铜、红磷等,使石灰水变浑浊的气体是二氧化碳,黑色粉末混合物加热会生成红色的物质和二氧化碳,所以红色物质是铜,黑色物质是碳和氧化铜,无色气体A通过炽热的焦炭后转化为气体D,则A应为CO2,D为CO,黑色粉末B在加热条件下与D反应,生成红色固体E,同时放出无色气体A,该反应为氧化铜与一氧化碳的反应,所以B为CuO,E为Cu,A与石灰沙浆中的F反应,能够生成白色坚固的固体G,则F为Ca(OH)2,G为CaCO3,根据元素守恒,可知M中有铜元素,M分解生成氧化铜和二氧化碳,根据绿色粉末状的这一特征,可推出M为Cu2(OH)2CO3,据此答题.
解答 解:根据常见的黑色粉末有:氧化铜、碳、二氧化锰等,红色物质有氧化铁、铜、红磷等,使石灰水变浑浊的气体是二氧化碳,黑色粉末混合物加热会生成红色的物质和二氧化碳,所以红色物质是铜,黑色物质是碳和氧化铜,无色气体A通过炽热的焦炭后转化为气体D,则A应为CO2,D为CO,黑色粉末B在加热条件下与D反应,生成红色固体E,同时放出无色气体A,该反应为氧化铜与一氧化碳的反应,所以B为CuO,E为Cu,A与石灰沙浆中的F反应,能够生成白色坚固的固体G,则F为Ca(OH)2,G为CaCO3,根据元素守恒,可知M中有铜元素,M分解生成氧化铜和二氧化碳,根据绿色粉末状的这一特征,可推出M为Cu2(OH)2CO3,
(1)由上面的分析可知,M为Cu2(OH)2CO3,故答案为:Cu2(OH)2CO3;
(2)①二氧化碳和碳反应生成一氧化碳,反应的化学方程式为:CO2+C$\frac{\underline{\;高温\;}}{\;}$ 2CO;
②氧化铜和一氧化碳反应生成铜和二氧化碳,反应的化学方程式为:CuO+CO $\frac{\underline{\;高温\;}}{\;}$Cu+CO2;
③二氧化碳和氢氧化钙反应生成碳酸钙和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O,
故答案为:CO2+C$\frac{\underline{\;高温\;}}{\;}$ 2CO;CuO+CO $\frac{\underline{\;高温\;}}{\;}$Cu+CO2;CO2+Ca(OH)2=CaCO3↓+H2O.
点评 在解此类方程式的书写题时,首先确定反应原理,然后再依据原理找出反应物、生成物和反应条件,根据方程式的书写规则书写方程式.


科目:高中化学 来源: 题型:选择题
| A. | 镁条作负极,电极反应:Mg-2e-=Mg2+ | |
| B. | 铝片作负极,电极反应:Al+4OH--3e--=[Al(OH)4]- | |
| C. | 电流从Al电极沿导线流向Mg电极 | |
| D. | 铝片上有气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
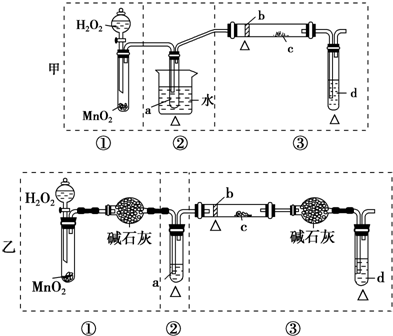
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



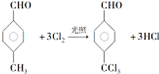 ,反应类型为取代反应
,反应类型为取代反应 +n
+n $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ +(2n-1)H2O
+(2n-1)H2O 的路线流程图:
的路线流程图: 合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验组 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | 达到平衡所需的时间/min | ||||
| CO | H2 | CH3OH | CO | H2 | CH3OH | |||
| 1 | 650℃ | 2.0 | 6.0 | 0 | 1.0 | 5 | ||
| 2 | 900℃ | 2.0 | 6.0 | 0 | 1.2 | 2 | ||
| 3 | 650℃ | 1.0 | 4.0 | 2.0 | a | b | c | t |
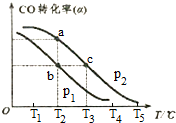
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.
肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.
| 苯甲醛 | 乙酸酐 | 肉桂酸 | 乙酸 | |
| 溶解度(25℃,g/100g水) | 0.3 | 遇热水水解 | 0.04 | 互溶 |
| 沸点(℃) | 179.6 | 138.6 | 300 | 118 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制备Fe(OH)3胶体,通常是将FeCl3固体溶于热 NaOH溶液中 | |
| B. | 为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量 | |
| C. | 除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 | |
| D. | 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com