
【题目】下列说法中正确的是( )
A. s电子云是在空间各个方向上伸展程度相同的对称形状
B. p电子云的形状是对顶双球
C. L电子层有d轨道
D. 2p轨道有一个未成对电子的基态原子和价电子排布为2s22p5的原子是同种元素的原子
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列物质的变化过程中有共价键明显被破坏的是( )
①I2升华 ②氯化钠溶于水 ③氯化氢溶于水 ④碳酸氢铵中闻到了刺激性气味
A. ①② B. ①③ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲乙两同学分别对含+4价硫元素的物质性质进行了探究。
(1)甲用下图装置进行实验(气密性已检验,加热和夹持装置已略去)。实验进行一段时间后,C、D中都出现明显的白色沉淀,经检验均为BaSO4。
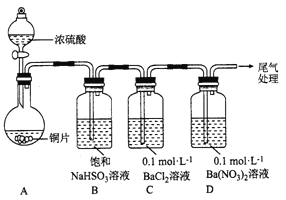
① A中反应的化学方程式是______________。
②为探究SO2在D中所发生的反应,甲进一步实验发现,出现由色沉淀的过程中,D溶液中NO3-浓度几乎不变。甲据此得出结论:D中出现白色沉淀的主要原因是__________________。
(2)乙用如下实验对含+4价疏元素的物质性质继续进行探究。
序兮 | 实验搡作 | 实聆现象 |
1 | 取0.3g纯净Na2SO3固体,向其中加人10mL 2 mol/L盐酸,再滴入4滴BaCl2溶液 | 产生无色气泡,滴入BaCl2溶液后,开始无现象,4 min后,溶液变浑浊 |
2 | 取0.3g纯净Na2SO3固体,向其中加入10mL 2 mol/L HNO3,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,2 h后,溶液变浑浊 |
3 | 取0.3g纯净Na2SO3固体,向其中加入10mL 浓HNO3,再滴入4滴BaCl2溶液 | 产生红棕色气体;滴入BaCl2溶液后,溶液立即产生大量白色沉淀 |
①用离子方程式解释实验1中产生现象的原因:________________。
② 由实验1、2、3对比,可以得到推论:________________。
③乙通过査阅资料发现.Na+对实验1和2中出现浑浊的时间无影响,于是进一步探究Cl-和 NO3-对其的影响:
序号 | 实验操作 | 实验现象 |
4 | 取____固体混合物,向其中加入10mL2 mol /LHNO3,再滴入4滴BaCl2溶液 | 产生无色气泡;:滴入BaCl2溶液后,开始无现象,20 min后,溶液变浑浊 |
i.实验2和4对比,乙获得推论:C1-的存在可以加快溶液中+4价硫元索的氧化;
ii.实验I和4对比,乙获得推论: ______________。
④通过以上实验,乙同学认为,确定某溶液中含有SO42-的实验方案:取待测液,向其中先滴加____________ (填字母序号)。
a.2 mol/L盐酸,再滴加BaCl2溶液,一段时间后出现白色沉淀
B.2 mol/L盐酸,再滴加BaCl2溶液,立即出现白色沉淀
C.2 mol/L硝酸,再滴加BaCl2溶液,一段时间后出现白色沉淀
D.2 mol/L硝酸,再滴加BaCl2溶液,立即出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一碘水和Fe(OH)3胶体的颜色极为相似。不用化学方法将它们区别开来,这样的方法有( )
①丁达尔效应 ②加热法 ③电泳实验法 ④加电解质法
A. ②④ B. ③④ C. ②③④ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CO2制备甲醇过程可能涉及反应如下:
反应Ⅰ:CO2(g)+3H2(g) ![]() CH3OH(g) +H2O(g) △H1=-49.58 kJmol-1
CH3OH(g) +H2O(g) △H1=-49.58 kJmol-1
反应Ⅱ:CO2(g)+ H2(g) ![]() CO (g)+H2O(g) △H2
CO (g)+H2O(g) △H2
反应Ⅲ:CO(g)+2 H2(g) ![]() CH3OH(g) △H 3=-90.77 kJmol-1
CH3OH(g) △H 3=-90.77 kJmol-1
回答下列问题:
(1)反应Ⅱ的△H2= ,反应Ⅲ自发进行条件是 (填“低温”、“高温”或“任何温度”)。
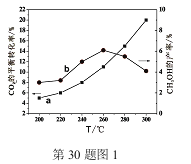
(2)某研究小组将一定量的H2和CO2充入恒容密闭容器中,在合适的催化剂条件下发生了反应I、Ⅱ、Ⅲ,不同温度下体系达到平衡时测得CO2的转化率(a)及CH3OH的产率(b)变化如图1所示。
①该反应达到平衡后,为再提高反应速率同时提高甲醇的生成量,可采取的措施有 。
A改用高效催化剂 B升高温度 C缩小容器体积 D分离出甲醇 E增加CO2的浓度
②据图1,当温度高于260℃时,CO2的平衡转化率随温度的升高继续增加,而CH3OH的产率却反而下降,请说明理由 。
(3)已知:在2L恒容密闭容器中充入3mol H2和1.5mol CO2(一定条件下,仅考虑发生反应Ⅰ),实验测得在不同温度下,反应体系中CO2的平衡转化率与温度的关系曲线如图2所示。实验测得:在500K时,反应Ⅰ经10min时达到平衡,假如其他条件不变,当反应时间进行到3min时,迅速将反应温度升至600K进行实验,请在图3中画出3~10min内容器中CH3OH浓度的后续变化总趋势图。
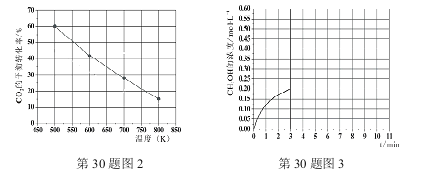
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于等质量的SO2和SO3的比较,正确的是
A.所含氧原子的个数比为2:3 B.所含硫原子的个数比为1:1
C.所含硫元素的质量比为5:4 D.所含原子个数比为3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列原子构成的单质中既能与稀硫酸反应,又能与烧碱溶液反应,且都产生H2的是( )
A. 核内无中子的原子
B. 外围电子排布为3s23p2
C. 最外层电子数等于倒数第三层上的电子数的原子
D. N层上无电子,最外层上的电子数等于电子层数的原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4溶液常用作氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液很容易被空气中或水中某些少量还原性物质还原,生成难溶性物质MnO (OH)2,因此配制KMnO4标准溶液的操作是: (1)称取稍多于所需量的KMnO4固体溶于水,将溶液加热并保持微沸1h; (2)用微孔玻璃漏斗过滤除去难溶的MnO (OH)2; (3)过滤得到的KMnO4溶液贮存于棕色试剂瓶放在暗处; (4)利用氧化还原滴定方法,在700C-800C条件下用基准试剂 (纯度高、式量较大、稳定性较好的物质)溶液标定其浓度。请回答下列问题:
(1)将溶液加热并保持微沸1h的目的是 。
(2)如何保证在700C~800C条件下进行滴定操作: 。
(3)准确量取一定体积的KMnO4溶液用 (填仪器名称)。
(4)在下列物质中,用于标定KMnO4溶液的基准试剂最好选用 (填序号)。
A.H2C2O4·2H2O | B.FeSO4 | C.浓盐酸 | D.Na2SO3 |
(5)若准确称取Wg你选的基准试剂溶于水配成500mL水溶液,取25.00mL置于锥形瓶中,用高锰酸钾溶液滴定至终点,消耗高锰酸钾溶液VmL。问:
①滴定终点标志是 ;
②所配制KMnO4标准溶液的物质的量浓度为 ;
(6)若用放置两周的KMnO4标准溶液去滴定水样中Fe2+含量,测得的浓度值将 (填“偏高”或“偏低”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com