
【题目】从海水中提取的粗盐含有Ca2+、Mg2+、SO42-等离子,为除去杂质离子可使用以下四种试剂:①Na2CO3溶液②BaCl2溶液③NaOH溶液④盐酸(用于沉淀的试剂均稍过量)。
![]()
(1)请在操作流程中填入合适的试剂编号_______、_______、______。
(2)加入过量NaOH溶液的目的是除去_______(填离子符号)。
(3)写出加入盐酸后溶液中发生主要反应的离子方程式_________、___________。
【答案】② ① ④ Mg2+ OH-+H+=H2O CO32-+2H+=CO2+H2O
【解析】
SO42-、Ca2+、Mg2+分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,再通过过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,所以应先加BaCl2溶液再加Na2CO3溶液,最后加入盐酸,以此解答该题。
(1)SO42-、Ca2+、Mg2+等分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,盐酸能除去过量的Na2CO3溶液和NaOH溶液,所以应先加BaCl2溶液再加Na2CO3溶液,最后加入盐酸,所以正确顺序为③②①④;
(2)加入过量NaOH溶液的目的是除去Mg2+;
(3)滤液中含有过量的碳酸钠和氢氧化钠。加入的盐酸可与碳酸钠、氢氧化钠反应,反应的离子方程式为OH-+H+=H2O、CO32-+2H+=CO2+H2O。


科目:高中化学 来源: 题型:
【题目】(1)系统命名: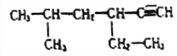 的名称为:_______________________。
的名称为:_______________________。
(2)![]() 的键线式:_____________________________。
的键线式:_____________________________。
(3)下列关于糖类的说法正确的是_______。(填标号)
a.糖类都有甜味,具有CnH2mOm的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类正确的是
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
B | NaOH | HCl | NaCl | Na2O | CO |
C | NaOH | CH3COOH | CaF2 | CO | SO2 |
D | KOH | HNO3 | CaCO3 | CaO | SO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯的同系物中,有的侧链能被KMnO4酸性溶液氧化,生成芳香酸,反应如下:
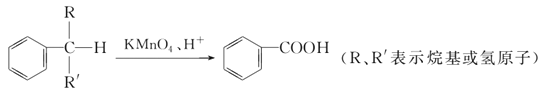
(1)现有苯的同系物甲、乙,分子式都是C10H14,甲不能被KMnO4酸性溶液氧化为芳香酸,它的结构简式是______________;乙能被KMnO4酸性溶液氧化为分子式为C8H6O4的芳香酸,则乙可能的结构有________种。
(2)有机物丙也是苯的同系物,分子式也是C10H14,它的苯环上的一溴代物只有一种,试写出丙所有可能的结构简式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学进行下列实验:在加热条件下将24g CuO、Fe2O3的混合物与充足的CO完全反应,并将反应后的气体全部通入到足量的澄清石灰水中,得到白色沉淀40g。下列有关叙述中不正确的是( )
A. 原混合物中CuO与Fe2O3物质的量比为1:1
B. 反应后所得CO2的物质的量为0.4mol
C. 实验过程中需要的CO 质量为11.2g
D. 原混合物中CuO与Fe2O3的质量比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图。根据图示判断,下列结论中不正确的是

A. N点时溶液中的溶质只有NaCl
B. M点之前加入的是NaOH溶液,M点之后加入的是盐酸
C. c(NaOH)=c(HCl)
D. 原混合溶液中c(MgCl2)∶c(AlCl3)=1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。

实验操作 | 实验现象 |
i.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
ii.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
iii.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(1)C中产生的白色沉淀是______。
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2。
①乙同学认为不能得出此结论,对实验进行了改进:
打开弹簧夹,通入N2,待排净装置内空气后,关闭弹簧夹,再打开A中分液漏斗活塞,此操作的目的是_________________
②丙同学进行了进一步的改进:
在B和C之间增加盛放CCl4的洗气瓶D,丙同学的目的是______
③将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:
氧化性H2O2>SO2。试写出两者反应的化学方程式________________
(3)iii中滴入少量H2O2没有明显变化。提出假设:
观点1:H2O2的量少不能氧化Br-
观点2:B中有未反应H2SO3(或SO2)
为验证观点2,应进行的实验操作及现象是______。
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期主族元素,它们的原子序数依次增大,其中A元素原子核外电子仅有一种原子轨道,也是宇宙中最丰富的元素,B元素原子核外p电子数比s电子数少1,C为金属元素且原子核外p电子数和s电子数相等,D元素的原子核外所有p轨道全充满或半充满。
(1)写出A、B元素的元素符号:A________,B________。
(2)写出C元素基态原子核外电子排布式:C______________________________。
(3)写出D元素基态原子核外电子轨道表示式:D_____________________________。
(4)写出B、C两种元素单质在一定条件下反应的化学方程式:___________________。
(5)写出B元素单质和氢化物的电子式:单质________,氢化物__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com