
【题目】下列有机反应的化学方程式正确的是( )
A.CH2=CH2+Br2→CH3—CHBr2
B.C2H4+3O2![]() 2CO2+2H2O
2CO2+2H2O
C.CH3CH2OH+Na→CH3CH2Na+H2O
D.CH3CH2OH+CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
科目:高中化学 来源: 题型:
【题目】某课外活动小组用如图装置进行实验,试回答下列问题:
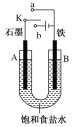
(1)若开始时开关K与a连接,则B极的Fe发生___腐蚀(填“析氢”或“吸氧”),B极的电极反应式为___。
(2)若开始时开关K与b连接,下列说法正确的是___(填序号);
a.溶液中Na+向A极移动
b.从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
c.反应一段时间后加入适量稀盐酸可使电解质溶液恢复到电解前的浓度
d.若标准状况下B极产生2.24L气体,则溶液中转移0.2mol电子
此时装置内总反应的离子方程式为___。
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
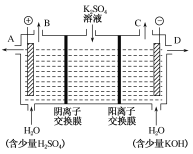
①该电解槽的阳极反应式为___,此时通过阴离子交换膜的离子数___(填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口___(填“A”“B”“C”或“D”)导出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料均为石墨)。

(1)图中a极要连接电源的________(填“正”或“负”)极,C口流出的物质是________。
(2)SO32-放电的电极反应式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是铜-锌原电池示意图。下列有关该原电池的描述中正确的是( )

A.锌片作正极,不断溶解
B.铜片作负极,有气泡产生
C.负极反应:Zn2++2e-=Zn
D.正极反应:2H++2e-=H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列常用物质:A.碳酸氢钠 B.阿斯匹林 C.葡萄糖 D.苯甲酸钠 E.柠檬黄
请用字母填空:
①具有解热镇痛疗效的是__,②可直接进入人体血液补充能量的是__,③可用作食品防腐剂的是___,④常用作食品着色剂的是__,⑤常用作治疗胃酸过多的抗酸剂的是__。
(2)保护环境,人人有责。①空气质量监测中,不需要监测的指标是__。
A.可吸入颗粒物的含量 B.NO2浓度 C.SO2浓度 D.CO2浓度
②在处理产生的废水时,需先加入明矾,其作用是__;后通入氯气或二氧化氯,其作用是___。
③对垃圾需要分类处理。如图所示的垃圾分类标志的含义是__。

(3)化学与材料密切关联。
①石墨烯(如图)可用作太阳能电池的电极,这里主要利用了石墨烯的__性。

②钢铁在酸雨中会发生吸氧腐蚀,其正极反应为:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇(CH3CH2OH)既是生活中常见的有机物,又是重要的化工原料。
(1)工业上可用乙烯制备乙醇,其反应的化学方程式为:CH2 = CH2+H2O![]() CH3CH2OH,该反应属于__反应(填“加成”或“取代”)。
CH3CH2OH,该反应属于__反应(填“加成”或“取代”)。
(2)官能团决定有机物的性质。乙醇中含有的官能团名称是__。
(3)为探究乙醇的性质,某学生向试管中加入3mL乙醇,将下端绕成螺旋状的铜丝在酒精灯火焰上灼烧至红热后,迅速插入乙醇中,可观察到铜丝表面由黑色变成红色,说明乙醇具有__性。
(4)萃取是物质分离的一种方法。某学生拟用乙醇萃取溴水中的Br2,判断该方法是否可行:__(填“是”或“否”),判断的理由是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁、铝、硅、银、铁的单质及其化合物在建筑业、飞机制造业、电子工业和石油化工等方面应用广泛。回答下列问题:
(1)Fe3+价层电子的轨道表达式(电子排布图)为__。
(2)硅能形成多种化合物(如SiH4、Si2H4等),SiH4的中心原子的杂化轨道类型为__,其分子的立体构型为__,键角为__;Si2H4分子中含有的σ键和π键的数目之比为__。
(3)Mg、Al的第一电离能:Mg__Al(填“>”或“<”)。
(4)Ca和Fe属于同一周期,且核外最外层电子构型相同,但金属Ca的熔点、沸点等都比金属Fe低,原因是__。
(5)Ag晶体的堆积方式为面心立方最密堆积(如图所示),晶胞中Ag原子的配位数为__;设Ag原子半径为rcm,阿伏加德罗常数的值用NA表示,则Ag晶体的密度为__g·cm-3(写出表达式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究NO2与过氧化钠反应的情况,甲、乙两位同学设计了如下实验,其装置如图。

已知:2NO2+2NaOH==NaNO3+NaNO2+H2O
试回答下列问题:
(1)仪器A的名称是________________,仪器B的作用是________________________。
(2)装入药品前必须检查装置的气密性,具体操作方法是________________________。
(3)试管中生成NO2反应的离子方程式是________________________________________。
(4)实验过程中,两位同学通过检验得知气体产物中含有较多氧气。该同学通过查阅资料了解NO2具有氧化性,据此甲同学判断NO2与过氧化钠反应可得到氧气,而乙同学认为该结论不合理,理由是__________。为验证自己的想法,乙同学对上述装置进行了改进,具体做法是________________。
(5)改进装置后,再进行实验,两位同学发现过氧化钠的颜色由淡黄色逐渐变成白色,且检验不出氧气的生成,该反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝试剂的结构简式如图所示,下列有关铝试剂的说法错误的是
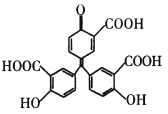
A.铝试剂分子中氢原子数目为16
B.1 mol铝试剂最多消耗3 mo1NaHCO3
C.铝试剂分子中所有碳原子可能在同一平面上
D.铝试剂能与FeCl3溶液发生显色反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com