
| 8g |
| 6.2g+93.8g |
| 8g |
| 4.6g+95.6g-0.2g |
| 8g |
| 7.8g+93.8g-1.6g |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
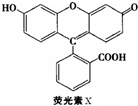
| A、荧光素的分子式为C20H14O5 |
| B、1molX最多能与9mol氢气反应 |
| C、1molX与足量的浓溴水反应,最多消耗4molBr2 |
| D、X能与甲醛发生缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| [H+]?[CH3COO-] |
| [CH3COOH] |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol葡萄糖可与5mol乙醇发生酯化反应 |
| B、油脂氢化、氨基酸形成多肽、蛋白质水解都属于取代反应 |
| C、可用碘水和银氨溶液鉴别葡萄糖、麦芽糖和淀粉三种物质 |
| D、乙二醇、甲醛、α-羟基丙酸(CH3-CHOH-COOH)都可发生缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、③④⑤ |
| C、①②③④ | D、①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质的量相同的两种盐NaX、NaY的溶液,pH依次为9、10,则HX的酸性比HY弱 |
| B、相同体积、相同物质的量浓度的盐酸与醋酸溶液,分别与同浓度的氢氧化钠溶液恰好完全反应时,醋酸消耗的氢氧化钠溶液体积多 |
| C、pH=11的NaOH溶液和pH=11的氨水分别稀释100倍,前者pH一定小于后者 |
| D、分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、温度、压强一定时,熵减小的放热反应一定能自发进行 |
| B、温度、压强一定时,焓判据共同决定一个化学反应自发进行的方向 |
| C、反应焓变是决定反应能否自发进行的唯一因素 |
| D、固体的溶解过程与熵变无关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com