
【题目】100ml0.25molL﹣1 AlCl3溶液中,Cl﹣的物质的量浓度为molL﹣1;若将上述溶液加水稀释到500ml,Cl﹣的物质的量浓度为molL﹣1 .
科目:高中化学 来源: 题型:
【题目】碲(Te)广泛用于彩色玻璃和陶瓷。工业上用精炼钢的阳极泥(主要含有TeO2、少量Ag、 Au)为原料制备单质碲的一种工艺流程如下:

已知Te02微溶于水,易溶于较浓的强酸和强碱。
(1)“碱浸”时所用的试剂是 ___(填化学式)。
(2)碱浸后的“滤渣”可用于____。
(3)“沉碲”时,缓慢加入H2SO4,并不断搅拌。为生成TeO2沉淀需控制溶液的pH为4.5—5.0,其原因是____。
(4)“酸溶”后,将SO2通入TeC14酸性溶液中进行“还原”得到碲,该反应的化学方程式是____。
(5) 25℃时,亚碲酸(H2Te03)的Kal=lxl0-3,Ka2=2×l0-8
①0.lmol/L的NaHTe03的溶液中c(TeO32-) - c(H2TeO3)= ____(填离子浓度表达式)。
②0.lmol.L-1的NaHTe03溶液呈__________填“酸性”,“碱性”,“中性”)理由是____(写出利用平衡常数汁算及推理过程).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属加工后的废切削液中含有2%~5%的NaNO2,它是一种环境污染物。人们用NH4Cl溶液来处理此废切削液,使亚硝酸钠转化为无毒物质。该反应分两步进行:
第一步:NaNO2+NH4Cl=NaCl+NH4NO2
第二步:NH4NO2![]() N2↑+2H2O
N2↑+2H2O
下列对第二步反应的叙述中正确的是
①NH4NO2仅是氧化剂
②NH4NO2仅是还原剂
③NH4NO2发生了分解反应
④只有氮元素的化合价发生了变化
⑤NH4NO2既是氧化剂又是还原剂
A. ①③ B. ①④
C. ②③④ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤水中蕴含着丰富的镁资源,就MgCl2粗产品的提纯、镁的冶炼过程回答下列问题:已知MgCl2粗产品的溶液中含有Fe2+、Fe3+和Al3+. 表是生成氢氧化物沉淀的pH:
物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 8.1 | 3.8 | 9.5 |
完全沉淀pH | 3.7 | 9.6 | 4.8 | 11.0 |
(1)把MgCl2粗产品的溶液中的Fe2+转化为Fe3+,最适宜选用的物质是____(填序号,下同),加入______调节溶液的pH,充分反应后过滤,可得MgCl2溶液.
a.KMnO4 b.H2O2 c.MgO d.NaOH
(2)若除去溶液中的杂质离子,调节溶液的pH范围为:___________。
(3)由MgCl2溶液获得MgCl2固体的操作是:__________________。
(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的Na2SO3溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-6mol·L-1],此时溶液中c(SO32-)≤__________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式表达正确的是
A. 用惰性电极电解氯化镁溶液:2Cl-+2H2O![]() Cl2↑+H2↑+OH-
Cl2↑+H2↑+OH-
B. 碳酸氢钠溶液与过量澄清石灰反应:HCO3-+Ca2++OH-= CaCO3↓+ H2O
C. NaHS04溶液中滴入Ba(OH)2溶液至S042-完全沉淀:2H++S042-+Ba2++ OH-= BaS04↓+2 H2O
D. 向明矾溶液中滴加过量氨水:Al3++4NH3![]() H2O=Al02-+4NH4++2H2O
H2O=Al02-+4NH4++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(CH3COOH)2(g)![]() 2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量随温度(T)的变化曲线如图所示,下列说法正确的是( )
2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量随温度(T)的变化曲线如图所示,下列说法正确的是( )
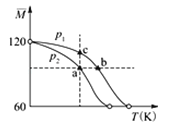
A. 该过程的△H<0
B. 气体压强:p(a)<p(b)= p(c)
C. 平衡常数:K(a)= K(b)< K(c)
D. 测定乙酸的相对分子质量要在高压、低温条件
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度时,将n mol/L氨水滴入10mL 1.0mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,有关说法正确的是( )
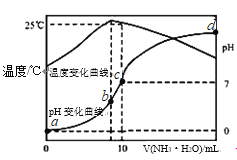
A. a点Kw=1.0×10﹣14 mol 2![]() L﹣2
L﹣2
B. 水的电离程度:b>c>a>d
C. b点:c(NH4+)>c(Cl﹣)>c(H+)>c(OH﹣)
D. 25℃ 时NH3·H2O的电离常数为![]() mol
mol![]() L-1(用n表示)
L-1(用n表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种,现利用另一种溶液X,用如图所示的方法可将它们依次确定。

试确定A、B、C、D、X各代表何种溶液。
A:________,B:__________,C:_________,D:_________,X:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)49 g H2SO4的物质的量是________;1.5 mol H2SO4的质量是_______,其中含有_______ mol H,含有_______g O。
(2)摩尔质量是指单位物质的量的物质所具有的质量。
①已知NH3的相对分子质量为17,则NH3的摩尔质量为________。
②NA为阿伏加德罗常数,已知a g某气体中含分子数为b,则该气体的摩尔质量为________。
③已知一个铁原子的质量为b g,则铁原子摩尔质量为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com