
【题目】A、B两种有机化合物,分子式都是C9H11O2N。
(1)化合物A是天然蛋白质的水解产物,光谱测定显示,分子结构中不存在甲基(—CH3),化合物A的结构简式是________。
(2)化合物B是某种分子式为C9H12的芳香烃一硝化后的唯一产物(硝基连在苯环上)。化合物B的结构简式是________。
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
【题目】把400 mL NH4HCO3和Na2CO3的混合溶液分成两等份,取一份加入含a mol NaOH的溶液恰好反应完全;取另一份加入含b mol HCl的溶液恰好反应完全。该混合溶液中c(Na+)为( )
A. (10b-5a) mol·L-1 B. (b-0.5a) mol·L-1
C. (![]() -
-![]() ) mol·L-1 D. (5b-
) mol·L-1 D. (5b-![]() ) mol·L-1
) mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前36号元素中的A、B、C、D、E、F的原子序数依次增大,只有前四种为短周期元素。A、B的原子核外s电子总数与p电子总数相等: C原子核外所有p轨道全满或半满: D元素的族序数与周期数的差为4;E是前四周期中电负性最小的元素:F在周期表的第七列。请根据以上相关信息,回答下列问题.
(1)A离子的电子共占据_____个轨道,A元素在自然界中的存在形态_____(a 只有化合态、b只有游离态、c都可能)。
(2)某人画的B的电子排布图如图![]() ,违背了________原理。
,违背了________原理。
(3)F位于______族,其基态原子的电子有_____种运动状态。
(4)CD3中心原子的杂化方式为____,用价层电子对互斥理论推测其分子空间构型为____,检验E元素的方法是___________。
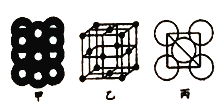
(5)若某金属单质晶体中原子的堆积方式如图甲所示,其品胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.则晶胞中该原子的配位数为______,该单质晶体中原子的堆积方式为四种基本堆积方式中的________,若已知该金属的原子半径为dcm,NA代表阿伏加德罗常数,金属的相对原子质量为M,则该晶体的密度为________g/cm3(用字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校课外活动小组的同学在完成课本乙醇氧化制乙醛的实验后,改进了实验方案(如图),进行如下实验操作(顺序已打乱):
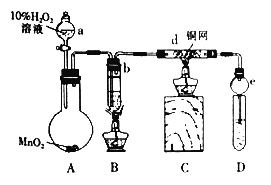
①点燃B装置中的酒精灯加热无水乙醇至沸腾并持续加热;
②向圆底烧瓶中滴加10%过氧化氢溶液;
③连接好仪器,检验装置的气密性;
④正确添加试剂;
⑤点燃C装置中的酒精灯
根据以上实验内容回答下列问题:
(1)实验操作顺序是 _____________________(填序号).
(2)装置e的作用是_____________________________________;
(3)写出d中发生反应的化学方程式____________________________________________;
(4)为检验D中收集的产物中是否含有乙醛,甲同学利用银氨溶液检验,请写出化学方程式_________________________________________________________;
(5)乙同学在一支试管中先加入2mL5%的CuSO4,滴加4﹣5滴NaOH溶液,再滴加几滴D中溶液,在酒精灯上加热,未出现砖红色沉淀,从而断定无乙醛生成.请你判断乙同学的说法是否合理,并说明理由___________________________________________________;
(6)若试管中收集到的液体用紫色石蕊试液检验,溶液显红色,说明液体中还含有____,要除去该物质,可先在混合液中加入_____(填写下列选项中的字母),然后再通过_____(填操作名称)即可除去.
A.饱和NaCl溶液 B.C2H5OH C.NaHCO3溶液 D.CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A、C、D、F具有下列性质:
物质 | 性质 |
A | 属于酯类化合物 |
C | 含有4类氢原子 |
D | 只含有一个氧原子,与Na反应放出H2 |
F | 属于烃 |
转化关系如图所示:
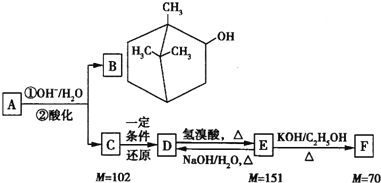
请回答下列问题:
(1)B的分子式为 ____________。
(2)B不能发生的反应是 (_______)(填序号)。
a.氧化反应 b.聚合反应 c.消去反应 d.取代反应 e.与Br2加成反应
(3)写出D→E、E→F的反应:
D→E ____________________________ ;
E→F______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),其过程如下:
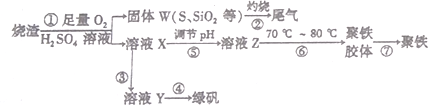
(1)过程③中,需要加入的物质名称是____________________。
(2)过程②中产生的尾气会对大气造成污染,可选用下列试剂中的___________吸收。
a.浓硫酸 b.蒸馏水 c.NaOH溶液 d.浓硝酸
(3)过程①中,FeS和O2、H2SO4反应的化学方程式为____________________。
(4)过程④的实验操作是____________________。
(5)过程⑥中,将溶液Z加热到70℃~80℃,目的是 ___________________。
(6)某种脱硫脱硝工艺中将废气经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥。设废气中的SO2、NO2的物质的量之比为1:1,则该反应的化学方程式为__________________。
(7)实验室为测定所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取样品2.700 g;②将样品溶于足量盐酸后,加入足量的氯化钡溶液:③过滤、洗涤、干燥、称量,得固体质量为3.495g,若该聚铁主要成分为[Fe(OH)SO4]a,则该聚铁中铁元素的质量分数为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组混合液:①汽油和水;②75%的酒精溶液;③碘的水溶液,分离以上各混合液的正确方法依次是
A. 分液、萃取、蒸馏 B. 分液、蒸馏、萃取
C. 萃取、蒸馏、分液 D. 蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解在化工生产、金属冶炼及科学研究等方面有重要应用。
(1)工业上用电解熔融氧化铝的方法来制取金属铝。纯净氧化铝的熔点很高(约2045℃),在实际生产中,通过加入助熔剂冰晶石Na3AlF6) 在1000℃左右就可以得到熔融体。
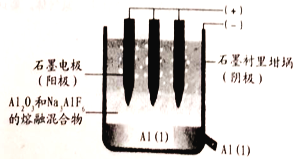
①写出电解时阳极的电极反应式:___________。
②电解过程中作阳极的石墨易消耗,原因是___________。
(2) 电解食盐水是氯破工业的基础。
①电解所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为____、_____。电解时,阴极反应的主要产物是___________。
②电解时用盐酸控制阳极区的pH在2~3,用必要的文字和反应方程式说明原因: ___________。
(3)Cu2O是半导体材料,工业上常用电解法制取。电解装置如下图所示。
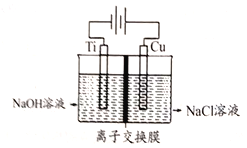
电解装置中采用离了交换膜控制阳极区OH-的浓度而制备纳米Cu2O。该离子交换膜是____(填“阴”或“阳”)离子交换膜,阳极生成Cu2O的电极反应式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com