
A.0.045mol/L B.0.035mol/L C.0.055mol/L D.0.040mol/L
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:013
常温下,将硫酸钾、硫酸铝、硫酸铝钾3种盐溶于硫酸酸化过的水中,测得溶液中![]() 、c(Al3+)=0.055mol/L,同时测得溶液的pH=1.0(假设溶液中硫酸完全电离为H+和
、c(Al3+)=0.055mol/L,同时测得溶液的pH=1.0(假设溶液中硫酸完全电离为H+和![]() ),则c(K+)为( )
),则c(K+)为( )
A.0.045mol/L B.0.035mol/L C.0.055mol/L D.0.040mol/L
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省攀枝花市高三第二次统考化学试卷(解析版) 题型:计算题
硫酸的工业制备是一个重要的化工生产过程,但同时在生产过程中会产生大量SO2等污染物。
(1)将SO2通入Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时若滴入BaCl2溶液,则会产生白色沉淀。溶液由棕黄色变为浅绿色用离子方程式表示为_____,后又由浅绿色变为棕黄色的离子方程式为_____。
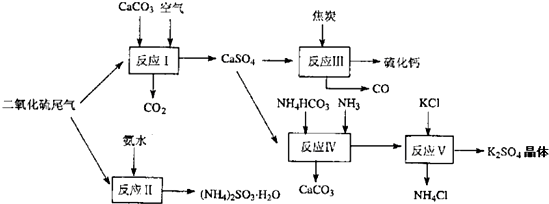
(2)以硫酸工业的尾气、氨水、石灰石、焦炭及碳酸氢铵和KCI为原料可以合成有重要用途的硫化钙、硫酸钾、亚硫酸氢铵等物质。合成路线如下:
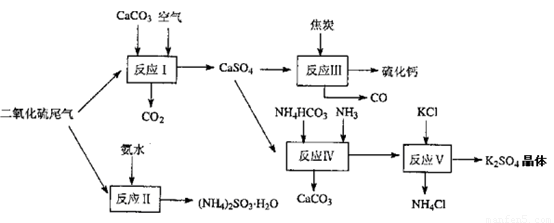
写出反应反应Ⅳ的化学方程式 ;
反应III中氧化剂与还原剂的物质的量之比为__ __;
反应V在25'C、40%乙二醇溶液中进行,该复分解反应能顺利进行的原因是 。
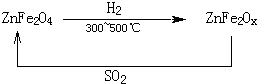
(3)新型纳米材料氧缺位铁酸锌(ZnFe2Ox),常温下能使SO2分解,减小工业废气对环境的影响,它由铁酸锌(ZnFe2O4)经高温还原制得,转化流程如下图所示:
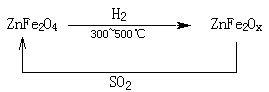
若2molZnFe2Ox与SO2反应可生成 0.75molS,x= ,写出铁酸锌高温下被还原生成氧缺位铁酸锌的化学方程式
(4)石灰石-石膏湿法烟气脱硫工艺技术的原理是烟气中的二氧化硫与浆液中的碳酸钙以及空气反应生成石膏(CaSO4.2H2O),写出该反应的化学方程式 。某电厂用煤300t(煤中含硫的质量分数为2.5%),若燃烧时煤中的硫全部转化为二氧化硫,用该方法脱硫时有96%的硫转化为石膏,则可生产石膏 t。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com