
【题目】有关氧化还原反应的叙述正确的是( )
A.氧化还原反应的实质是电子的转移(得失或偏移)
B.氧化还原反应的实质是元素化合价的升降
C.氧化还原反应的实质是有氧元素的得失
D.物质所含元素化合价升高的反应是还原反应
科目:高中化学 来源: 题型:
【题目】已知20°C时AgBr的溶解度为8.4×10﹣6AgCl的溶解度为1.5×10﹣4将AgCl与AgBr的饱和溶液等体积混合,再加入足量浓硝酸银,发生的反应为( )
A.AgCl沉淀多于AgBr沉淀
B.AgCl和AgBr沉淀等量生成
C.AgCl沉淀少于AgBr沉淀
D.只有AgBr沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁矿石中含铁量的测定,按以下步骤进行:铁矿石中含铁量的测定
下列说法不正确的是( )
A.步骤④中煮沸的作用是为了除去残留的氯气
B.步骤⑤中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、250mL容量瓶
C.铁矿石中铁的百分含量为56%
D.该铁矿石中若含氧为24% ,则铁的氧化物的化学式为Fe2O3·3FeO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两种溶液中分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-这6种离子中的3种(两种溶液中的离子不重复),已知甲溶液呈蓝色,则乙溶液中大量存在的离子是
A. K+、OH-、CO32-B. Cu2+、H+、Cl-
C. K+、H+、Cl-D. CO32-、OH-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,浓度均为1.0molL﹣1的NH3H2O和NH4Cl混合溶液10mL,测得其pH为9.3.下列有关叙述正确的是( )
A.加入适量的NaCl,可使c(NH4+)=c(Cl﹣)
B.滴加几滴浓氨水,c(NH4+)减小
C.滴加几滴浓盐酸, ![]() 的值减小
的值减小
D.1.0 molL﹣1的NH4Cl溶液中c(NH4+)比该混合溶液大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯。
已知: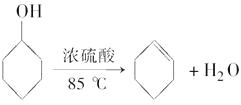
密度/g·cm-3 | 熔点/℃ | 沸点/℃ | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
(1)A中碎瓷片的作用是 , 导管B除了导气外还具有的作用是。
(2)试管C置于冰水浴中的目的是。
(3)环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在层(填“上”或“下”),分液后用(填入编号)洗涤。
a.KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
(4)再将环己烯进行蒸馏,可得环己烯精品。蒸馏时要加入生石灰,目的是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将绿矾(FeSO4·7H2O)、硫酸铵以相等物质的量混合可制得莫尔盐晶体。(NH4)2SO4+FeSO4+6H2O= (NH4)2SO4·FeSO4·6H2O↓,根据下图回答: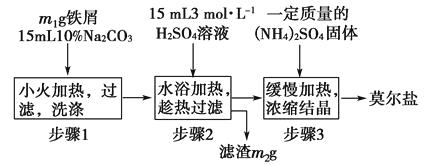
(1)步骤2中铁屑过量的目的是。
(2)步骤3中,加入(NH4)2SO4固体后,要得到莫尔盐晶体,需经过的实验操作包括:加热蒸发、、。浓缩时能否蒸发至干,为什么?。
(3)步骤3中制得的晶体过滤后用无水乙醇洗涤的目的是;
不用蒸馏水洗涤,理由是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( ) 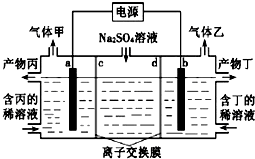
A.a极与电源的正极相连
B.产物丙为硫酸溶液
C.离子交换膜d为阳离子交换膜(允许阳离子通过)
D.a电极反应式为2H2O+2e﹣═2OH﹣+H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com