下列叙述中,不正确的是( )
A.0.1 mol?L-1CH3COOH溶液加水稀释,n(H+)增大
B.0.2 mol?L-1盐酸与等体积0.05 mol?L-1Ba(OH)2溶液混合后,溶液pH为1
C.向AgCl悬浊液中滴入KI溶液,生成AgI沉淀,说明AgCl的溶解度大于AgI
D.若NH4HCO3溶液、NH4HSO4溶液和NH4NO3溶液中c(NH4+)相等,则c(NH4HSO4)<c(NH4NO3)<c(NH4HCO3)
【答案】
分析:A、依据弱电解质存在电离平衡,稀释促进电离分析;
B、依据强酸强碱酸碱中和反应的实质分析计算;
C、依据沉淀溶解平衡中的沉淀转化的实质分析判断;
D、依据盐类水解的程度和其他影响离子对水解的影响分析.
解答:解:A、0.1 mol?L
-1CH
3COOH溶液加水稀释促进弱电解质醋酸的电离,离子浓度减少.n(H
+)物质的量增加,故A正确;
B、0.2 mol?L
-1盐酸中的氢离子浓度为0.2mol/L,0.05 mol?L
-1Ba(OH)
2溶液中氢氧根离子浓度为0.1mol/L,等体积混合按照H
++OH
-=H
2O反应后,剩余氢离子浓度=
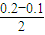
=0.05mol/L,pH>1,故B错误;
C、依据反应向更难的方向进行,向AgCl悬浊液中滴入KI溶液,生成AgI沉淀,说明AgCl的溶解度大于AgI,故C正确;
D、NH
4HCO
3溶液中的碳酸氢根离子水解促进铵根水解、NH
4HSO
4溶液中的氢离子抑制铵根离子的水解,NH
4NO
3溶液中只存在铵根离子的水解,若NH
4HCO
3溶液、NH
4HSO
4溶液和NH
4NO
3溶液中c(NH
4+)相等,则需要溶质的浓度为c(NH
4HSO
4)<c(NH
4NO
3)<c(NH
4HCO
3),故D正确;
故选B.
点评:本题考查了弱电解质的电离平衡移动,酸碱中和反应后的溶液pH计算,沉淀转化的本质,盐类水解的应用.

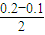 =0.05mol/L,pH>1,故B错误;
=0.05mol/L,pH>1,故B错误;
