
����Ŀ����ѧ�Һϳ���һ������ҩ��(G)�������Ӳ����պ����������ڴ�������������������Ӷ�ʹ�Ӳݳ�����������ϳ�·�����£�
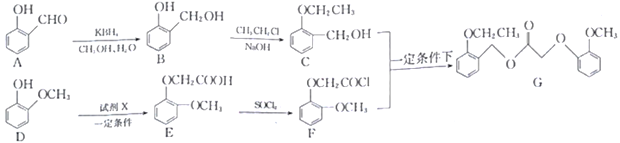
��1���м���E�к��������ŵ�����_________________��
��2��A��B��Ӧ������_______________________��
��3����֪D��Eת������һ������HBr�����Լ�X�Ľṹ��ʽΪ_________________��
��4��д��C+F��G�Ļ�ѧ����ʽ��__________________________________��
��5��д��ͬʱ��������������E��ͬ���칹��Ľṹ��ʽ________________ (д��һ�ּ���)��
�����ڷ����廯���
�ڴŹ�������������壬�������Ϊ1��1��2��6��
���ܷ���������Ӧ��ˮ�����֮һ�ܺ�FeCl3��Һ������ɫ��Ӧ��
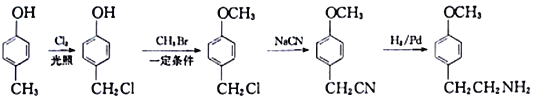
��6��������H(H2NCH2CH2![]() OCH3)�Ǻϳ����о�����Ҫ�м��壬д���Զ�-�����Ӻ� CH3Br Ϊ��Ҫԭ�Ϻϳɻ�����H��·�ߣ�_____________________________________________(�������Լ���ѡ)��
OCH3)�Ǻϳ����о�����Ҫ�м��壬д���Զ�-�����Ӻ� CH3Br Ϊ��Ҫԭ�Ϻϳɻ�����H��·�ߣ�_____________________________________________(�������Լ���ѡ)��
��ʾ��R��Cl![]() R��CN
R��CN![]() RCH2NH2
RCH2NH2
���𰸡� �Ѽ����Ȼ� ��ԭ��Ӧ BrCH2COOH 
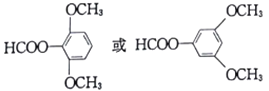
����������1���м���E�Ľṹ��ʽΪ��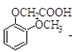 ������������Ϊ�Ѽ����Ȼ�����Ϊ���Ѽ����Ȼ�
������������Ϊ�Ѽ����Ȼ�����Ϊ���Ѽ����Ȼ�
��2��A��B ��A�е�ȩ��������ԭ��Ӧת��Ϊ�ǻ�����Ϊ����ԭ��Ӧ
��3��D��E����һ������HBr���÷�ӦΪȡ����Ӧ�����Լ�X�Ľṹ��ʽΪBrCH2COOH
����BrCH2COOH
��4����ӦC+F��GΪȡ����Ӧ,����л���ṹ��ʽ����֪��������HCl������C+F��G�Ļ�ѧ����ʽΪ�� 
��5��E��ͬ���칹�������������������ڷ����廯������˵�����б������ܷ���������Ӧ��ˮ�����֮һ�ܺ�FeCl3��Һ������ɫ��Ӧ��˵������������ˮ������з��ǻ�����ϴŹ�������������壬�������Ϊ1��1��2��6����֪����������ͬ���칹��Ľṹ��ʽ��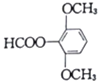 ��
��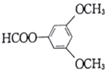 ����
���� 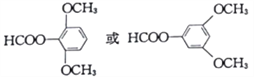
��6��![]() ���������յ�����������
���������յ�����������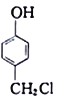 ��������ҩ��(G)�ĺϳ�·�߿���֪��,
��������ҩ��(G)�ĺϳ�·�߿���֪��,  ��CH3Br��һ������������
��CH3Br��һ������������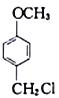 ��������ʾ��R��Cl
��������ʾ��R��Cl![]() R��CN
R��CN![]() RCH2NH2 ��
RCH2NH2 �� ��NaCN����
��NaCN����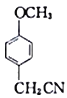 ��
�� ��
��![]() ������������
������������ �����������ϳɻ�����H��·�ߣ�
�����������ϳɻ�����H��·�ߣ�


 ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л��������{���ӻ��������
A. ˮ���к��е�ά����C B. ʯ���к��е�C16H34
C. �۲��к��е���ά�� D. ֲ�����к��е���֬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ĺ̶��Թ�ũҵ��������������ش����塣
��.�ϳɰ�������Ҫ���˹��̵���N2(g)+3H2(g)![]() 2NH3(g)��
2NH3(g)��
��1�����й��ڸ÷�Ӧ��˵���У���ȷ���� ��
A����H��0,��S��0 B����H��0����S��0
C����H��0,��S��0 D����H��0,��S��0
��2�� �����¶��£����ݻ�Ϊ1L���ܱ������У�����ImolN2��3molH2����Ӧ�ﵽƽ��ʱH2��ת����Ϊ60%����������·�Ӧ��ƽ�ⳣ��K= (�˴���Ҫ��д��λ)����������������䣬���������м���lmolN2��3molH2��Ӧ�ﵽƽ��ʱ��������ת���ʽ� (���������С�����䡱)
��3����״���£�����22.4mL�İ���ͨ��100mLpHΪ2��������.����Һ�и�����Ũ�ȵ�˳���ɴ�СΪ ��
��4��������ͨ��ʢ��CaSO4����Һ�ij������У���ͨ��������CO2���壬��ַ�Ӧ����������ҺΪ(NH4)2SO4��Һ���ù��̵Ļ�ѧ����ʽΪ ��
II.�����о��IJ������룬��ѧ�ҷ�����Խ��Խ���йص��Ĺ̶�������
��5��20����ĩ����ѧ�Ҳ��ø����ӵ����Ե�SCY�մ�(�ܴ���H+)Ϊ���ʣ�������������������ϵĽ����ٶྦྷ��Ĥ���缫��ʵ�ֳ�ѹ��570�����µĵ�ⷨ�ϳɰ�������˷�Ӧ���ת���ʣ���ʵ���ͼ���£������ĵ缫��ӦʽΪ ��

��6�����꣬���п�ѧ������ڳ��¡���ѹ�������������ºϳɰ�������˼·����Ӧԭ��Ϊ��
2N2(g)+6H2O(I) ![]() 4NH3(g)+3O2(g)�����䷴Ӧ����H= ��(��֪��N2(g)+3H2(g)
4NH3(g)+3O2(g)�����䷴Ӧ����H= ��(��֪��N2(g)+3H2(g) ![]() 2NH3(g) ��H=-92.4kJ��mol-1��2H2(g)+O2(g)
2NH3(g) ��H=-92.4kJ��mol-1��2H2(g)+O2(g) ![]() 2H2O(I) ��H=-571.6kJ��mol-1)
2H2O(I) ��H=-571.6kJ��mol-1)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʣ�����������ʡ������˳�����е��ǣ� ��
A.�ռҺ̬�������
B.��ʯ�ҡ����ס���ʯ��
C.�ɱ��������Ȼ���
D.����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ƿ�����õ��һ��ΪǦ���أ�����һ�ֵ��͵Ŀɳ���أ�����ܷ�ӦʽΪ��Pb+PbO2+4H++2SO42��![]() 2PbSO4+2H2O������˵����ȷ���ǣ�������
2PbSO4+2H2O������˵����ȷ���ǣ�������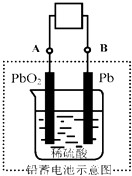
A.�ŵ�ʱ����������������A����������B
B.�ŵ�ʱ��������Ӧ��Pb��2e��+SO42�� ![]() PbSO4
PbSO4
C.���ʱ��Ǧ���صĸ���Ӧ��������Դ����������
D.���ʱ��������Ӧ��PbSO4��2e��+2H2O=PbO2+SO42��+4H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Li2CO3��K2CO3Ϊ����ʣ���Ȼ���������������ṩ��Ӧ����ȼ�ϵ������ͼ������˵����ȷ����
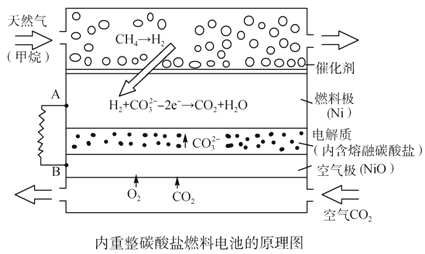
A. �Դ˵��Ϊ��Դ��⾫��ͭ������0.1 mol e�� ת��ʱ����3.2 gͭ�ܽ�
B. ���Լ���Ϊȼ����ʱ�����缫��Ӧʽ��CH4+5O2����8e��=CO32-+2H2O
C. �õ��ʹ�ù������貹��Li2CO3��K2CO3
D. �����������ĵ缫��ӦʽΪO2��4e����2CO2===2CO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ǽ�������A����ͼ��ʾ�Ĺ���ת��Ϊ������D����֪DΪǿ�ᣬ��ش��������⡣
![]()
(1)��DΪ���ᣬ��B�Ļ�ѧʽ��______��
(2)��DΪ���ᣬ��C����ɫΪ______��Cת��ΪB�ķ�Ӧ����ʽΪ____________��
(3)���������������Ļ����Һ���ɲ�ȡ�ķ��뷽����______��
(4)��һ���������Ļ����Һ��ȡ��100mL��������BaCl2��Һ�����ˣ�ϴ�ӣ���ɺ�õ�93.2g��������Һ��4mol/LNaOH��Һ��Ӧ������400mLNaOH��Һʱǡ����ȫ�к͡�����ɵã�
�ٻ����Һ����������ʵ���Ũ��Ϊ______��
����ȡ100mLԭ�����Һϡ����200mL����Ϊϡ�ᣬ����44.8gͭ�۹��ȣ��ռ����������ڱ�״���µ����Ϊ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ�ÿ������ռ�SO2����֤��ijЩ��ѧ����,����˵����ȷ����
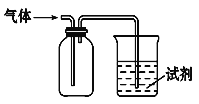
ѡ�� | �Լ� | ���� | ���� |
A | ��ˮ | ��Һ��ɫ | SO2�������� |
B | H2S��Һ | ����ɫ���� | SO2�������� |
C | NaOH��Һ | ���������� | SO2��NaOH��Һ����Ӧ |
D | ��ɫʯ����Һ | ��Һ���ɫ����ɫ | SO2�����ԡ�û��Ư���� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�������SOCl2����һ��Һ̬������е�Ϊ 77������ũҩ����ҩ��ҵ����;�㷺��SOCl2��ˮ���ҷ�Ӧ��Һ���ϲ��������������д̼�����ζ�����������ʵ���Һϳ�ԭ����SO2+Cl2+SCl2�T2SOCl2������װ����ͼ��ʾ��(��֪ SCl2�ķе�Ϊ 50��).
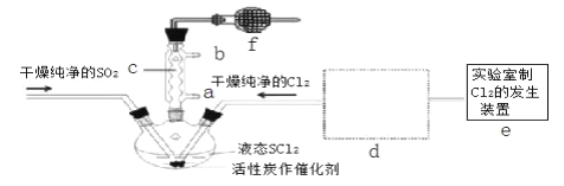
�ش��������⣺
��1�����������Ʊ� SO2�ķ��������ѡ����____________________________
���� | A | B | C | D |
����װ�� |
|
|
|
|
��ѡ�Լ� | 70%H2SO4+K2SO3 | 18.4mol/LH2SO4+Cu | 4mol/LHNO3+Na2SO3 | NaHCO3���� |
��2���� MnO2��Ũ����Ϊԭ���Ʊ� Cl2�����ӷ���ʽΪ___________________________
��3������ f ��������_________________________________________________
��4��d �����߿�����������װ�ã�����������˳��������װ�õ�ҩƷ�ֱ���_______________��
��5��ʵ�������,��������ƿ������в�Ʒ��������ķ����� _________________________
��6������ SOCl2�� FeCl36H2O ����ˮ�������ʵ��֤����ˮʱ������������ԭ��Ӧ��ȡ���� FeCl36H2O ���Թ��У�������� SOCl2�������Թ��м�ˮ�ܽ⣬�μ�____________��________��Һ��֤����ˮ���̷�����������ԭ��Ӧ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com