
分析 (1)n(H2SO4.SO3)=$\frac{445g}{178g/mol}$=2.5mol,每个焦硫酸分子可以吸水后成为2个硫酸分子,所以C=$\frac{n({H}_{2}S{O}_{4}.S{O}_{3})×2}{V}$;
(2)根据浓硫酸吸水后生成H2SO4•H2O计算,硫酸与水的物质的是为1:1;
(3)设Fe3O4与Fe2O3物质的量分别为amol,bmol然后铁守恒和消耗氧气的量列方程组解;
(4)根据2H2S+3O2$\frac{\underline{\;点燃\;}}{\;}$2SO2+2H2O,设混合所体为1体积,则硫化氢为0.84体积,然后关系式来求解.
解答 解:(1)n(H2SO4.SO3)=$\frac{445g}{178g/mol}$=2.5mol,每个焦硫酸分子可以吸水后成为2个硫酸分子,所以C=$\frac{n({H}_{2}S{O}_{4}.S{O}_{3})×2}{V}$=$\frac{2.5mol×2}{4L}$=1.25mol/L,
故答案为:1.25;
(2)n(H2SO4•H2O)=n(H2SO4)=$\frac{250g×98%}{98g/mol}$=2.5mol,所以吸收水的质量为:2.5mol×116g/mol-250g=40g,
答:250g质量分数为98%的硫酸能吸收40g水;
(3)2934.4L氧气的物质的量为$\frac{2934.4L}{22.4L/mol}$=131mol,设Fe3O4与Fe2O3物质的量分别为amol,bmol,则$\left\{\begin{array}{l}{3a+2b=48}\\{8a+5.5b=131}\end{array}\right.$,解得:$\left\{\begin{array}{l}{a=4}\\{b=18}\end{array}\right.$,所以Fe3O4与Fe2O3物质的量之比4:18=2:9,
答:反应产物中Fe3O4与Fe2O3物质的量之比2:9;
(4)设混合所体为1体积,则硫化氢为0.84体积,
由2H2S+3O2$\frac{\underline{\;点燃\;}}{\;}$2SO2+2H2O,
2 3 2 2
0.84 1.26 0.84 0.84
所以反应消耗的空气为:$\frac{1.26}{21%}$=6,而空气过量77%,所以一共所需空气为:6×1.77=10.62体积,所以φ(SO2)=$\frac{0.84}{10.62-1.26+1+0.84}$=0.075,
答:产物气体中SO2体积分数为0.075.
点评 本题考查化学方程式的有关计算,为高频考点,侧重考查学生分析计算能力,明确各个物理量关系是解本题关键,注意原子守恒的灵活运用,题目难度中等.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:解答题
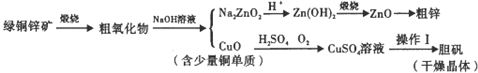

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 分子式/结构式 | NO/N≡O | CO/C≡O | CO2/O=C=O | N2/N≡N |
| 化学键 | N≡O | C≡O | C=O | N≡N |
| 键能(KJ/mol) | 632 | 1072 | 750 | 946 |
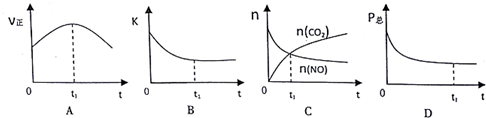
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/×10-2mol | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| n(CO)/×10-1mol | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
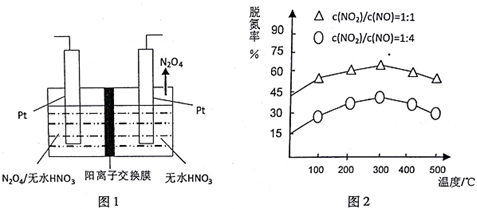
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1010的溶液中:Na+ ${NH}_{4}^{+}$ HCO${\;}_{3}^{-}$ Cl- | |
| B. | 含有大量ClO-的溶液中:K+ OH- Na+ ${SO}_{3}^{2-}$ | |
| C. | c(Al3+)=0.1 mol?L-1的溶液中:Na+ NO${\;}_{3}^{-}$ AlO${\;}_{2}^{-}$ ${SO}_{4}^{2-}$ | |
| D. | 澄清透明的溶液中:Cu2+ Fe3+ NO${\;}_{3}^{-}$ Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
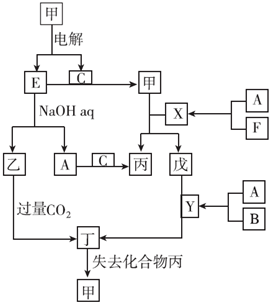
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使广泛pH试纸显蓝色的溶液:K+、Na+、CH3COO-、Br- | |
| B. | 甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- | |
| C. | 0.1 mol?L-1 FeCl3溶液:K+、NH4+、I-、SCN- | |
| D. | 由水电离的c (H+)=1×10-14 mol?L-1的溶液中:Ca2+、K+、Cl-、HCO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤ | B. | ①②③⑤ | C. | ③④⑤ | D. | ②④⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com