


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
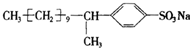 ,其结构中与肥皂(C17H35COONa)的憎水基团-C17H35相当的基团为
,其结构中与肥皂(C17H35COONa)的憎水基团-C17H35相当的基团为查看答案和解析>>
科目:高中化学 来源: 题型:
| 步骤 | 实验操作 | 实验现象 |
| Ⅰ | 向X的粉末中加入过量盐酸 | 产生气体A,得到无色溶液 |
| Ⅱ | 向Ⅰ所得的溶液中滴加氨水,调节pH至5~6,过滤 | 生成白色沉淀B |
| Ⅲ | 向沉淀B中加过量NaOH溶液 | 沉淀全部溶解 |
| Ⅳ | 向Ⅱ得到的滤液中滴加NaOH溶液,调节pH至12 | 生成白色沉淀C |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸发 | B、萃取 | C、过滤 | D、蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
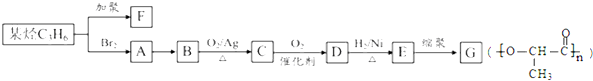
查看答案和解析>>
科目:高中化学 来源: 题型:
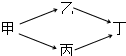 甲、乙、丙、丁四种烃的含氧衍生物,其分子中都含有一个或一个以上的官能团,通过下列转化关系可由甲制取丁:若丁的相对分子质量总为甲的两倍,乙的相对分子质量总大于丙.回答下列问题:
甲、乙、丙、丁四种烃的含氧衍生物,其分子中都含有一个或一个以上的官能团,通过下列转化关系可由甲制取丁:若丁的相对分子质量总为甲的两倍,乙的相对分子质量总大于丙.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | A | B | C | D |
| 实验目的 | 食盐水与泥沙分离 | 制取蒸馏水 | 分离水和植物油 | 从浓食盐水中 得到氯化钠晶体 |
| 分离方法 | 萃取 | 蒸馏 | 分液 | 蒸发 |
| 选用仪器 | 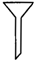 | 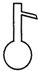 | 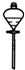 |  |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液的酸性增强 | ||
B、c(Na+)与c(CO
| ||
| C、溶液浓度变大,有晶体析出 | ||
| D、溶液浓度不变,有晶体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温 | B、较高温度 |
| C、较低温度 | D、无法判断温度高低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com