
| A. | 可溶性铜盐有毒,故人体内不存在铜元素 | |
| B. | 硅胶可用作食品干燥剂 | |
| C. | 宇航服主要成分是由碳化硅陶瓷和碳纤维复合而成,是一种新型无机非金属材料 | |
| D. | 中秋佳节月饼中用小袋包装的铁粉来防止月饼氧化变质 |
分析 A.铜是一种不可缺少的微量元素;
B.硅胶具有吸水性,且无毒;
C.碳化硅、陶瓷和碳纤维复合而成的是复合材料,是一种新型无机非金属材料分析;
D.铁粉具有还原性,能够防止食品氧化变质;
解答 解:A.铜是一种不可缺少的微量元素,人体内含有一定量的铜元素,故A错误;
B.硅胶具有吸水性,且无毒,可以做食品干燥剂,故B正确;
C.航天服主要成分是由碳化硅、陶瓷和碳纤维复合而成的,碳纤维复合材料是主要由碳单质做成,是一种复合材料,故C正确;
D.铁粉具有还原性,能够防止食品氧化变质,故D正确;
故选:A.
点评 本题考查常见的食品添加剂、材料的分类,熟悉相关物质和元素的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:推断题
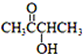 )有如下转化关系,且 1mol B反应生成了2mol C.
)有如下转化关系,且 1mol B反应生成了2mol C.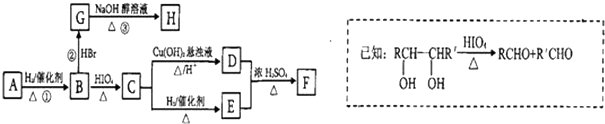
 .
.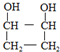 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
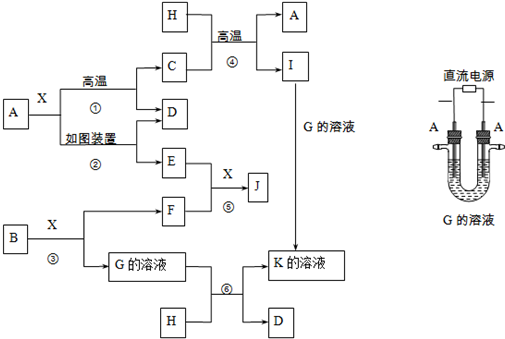
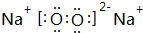 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol 钠与氧气反应生成 Na2O 或 Na2O2时,失电子数目均为 NA | |
| B. | 1 mol/L 的 NaOH 溶液中含 Na+数目为 NA | |
| C. | 标准状况下,2.24LC6H6 所含的分子数目为 0.1NA | |
| D. | 1 mol Na2O2 中含有的阴离子数目为 2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z的最高价氧化物的水化物能形成多种含Y元素的盐 | |
| B. | W的氧化物对应水化物的酸性一定强于Z | |
| C. | Y的单质应该保存在水中 | |
| D. | X的氢化物沸点比Z的氢化物沸点低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫元素既被氧化又被还原 | |
| B. | 氧化剂与还原剂的物质的量之比为1:2 | |
| C. | 每生成1molNa2S2O3,转移4mol电子 | |
| D. | 相同条件下,每吸收10m3SO2就会放出5m3CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ④ | C. | ②③ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
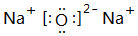 、
、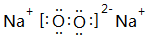 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L盐酸和0.1mol/L醋酸分别与0.2mol/L氢氧化钠溶液反应的速率相同 | |
| B. | 0.1mol/L盐酸和0.1mol/L硝酸分别与大小相同的大理石反应的速率相同 | |
| C. | 铝和铁分别与0.1mol/L硫酸的反应速率相同 | |
| D. | 大理石块与大理石粉末分别与0.1mol/L盐酸反应的速率相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com