
����Ŀ����A��B��C��D��E�������������������ʣ�
�ٸ�ȡ0.1mol�ֱ���ȼ�գ�����B��C��Eȼ�����õ�CO2��Ϊ4.48L(��״��)��A��Dȼ�����õ�CO2����ǰ���ߵ�3����
�������������£�A��B��C���ܸ����������ӳɷ�Ӧ������A����ת��ΪD��B����ת��ΪC��C����ת��ΪE��
��B��C����ʹ��ˮ������KMnO4��Һ��ɫ����A��D��E�����ʣ�
������м������ʱ��A�����巢��ȡ����Ӧ��
(1)�ж�A��B��D��E����ʲô���ʣ�д���������ʵĽṹ��ʽ��A_______B_______C_______D________E________��
(2)����E�����ȴ�����______�֡�
(3)д��C��������Ȼ�̼��Һ��Ӧ�Ļ�ѧ����ʽ��_______
(4)д�������漰�Ļ�ѧ����ʽ��__________
���𰸡�![]() CH��CH CH2=CH2
CH��CH CH2=CH2 ![]() CH3CH3 2 CH2=CH2+Br2��CH2BrCH2Br
CH3CH3 2 CH2=CH2+Br2��CH2BrCH2Br ![]() +Br2
+Br2![]()
![]() +HBr
+HBr
��������
ȡ0.1mol�������ֱ�ȼ�գ�����CO2�������ж�B��C��E��Cԭ�Ӹ���Ϊ2��A��D��Cԭ�Ӹ���Ϊ6���ٸ���A��B��C���ܸ����������ӳɷ�Ӧ������A����ת��ΪD��B����ת��ΪC��C����ת��ΪE��B��C����ʹ��ˮ������KMnO4��Һ��ɫ����A��D��E�����ʣ��Ϳ�һһ���
��ȡ0.1mol���������ֱ�ʹ֮���ȼ�գ�����B��C��Eȼ�����õ�CO2��Ϊ4.48L���������������̼�����ʵ���= ![]()
![]() =0.2mol������B��C��E�����к���2��̼ԭ�ӣ�A��Dȼ�����õ�CO2����B��C��E����������A��D�����к���6��̼ԭ�ӣ����ʵ��������£�A��B��C���ܸ����������ӳɷ�Ӧ��˵�����в����ͼ���������A��ֱ��ת��ΪD��B��ת��ΪC��C��ת��ΪE��B��C����ʹ��ˮ�����Ը��������Һ��ɫ����A��D��E�������ʣ�����֪B����̼̼������C�к���̼̼˫��������B����Ȳ��C����ϩ��E�����飻����м������ʱ��A����Һ̬�巢��ȡ����Ӧ��A����6��̼ԭ�ӣ���Ϊ������A�DZ���A��ת��ΪD����D�ǻ����飬
=0.2mol������B��C��E�����к���2��̼ԭ�ӣ�A��Dȼ�����õ�CO2����B��C��E����������A��D�����к���6��̼ԭ�ӣ����ʵ��������£�A��B��C���ܸ����������ӳɷ�Ӧ��˵�����в����ͼ���������A��ֱ��ת��ΪD��B��ת��ΪC��C��ת��ΪE��B��C����ʹ��ˮ�����Ը��������Һ��ɫ����A��D��E�������ʣ�����֪B����̼̼������C�к���̼̼˫��������B����Ȳ��C����ϩ��E�����飻����м������ʱ��A����Һ̬�巢��ȡ����Ӧ��A����6��̼ԭ�ӣ���Ϊ������A�DZ���A��ת��ΪD����D�ǻ����飬
(1)������������֪��AΪ![]() ��BΪCH��CH��CΪCH2=CH2��DΪ
��BΪCH��CH��CΪCH2=CH2��DΪ ![]() ��EΪCH3CH3 ��
��EΪCH3CH3 ��
�ʴ�Ϊ��AΪ![]() ��BΪCH��CH��CΪCH2=CH2��DΪ
��BΪCH��CH��CΪCH2=CH2��DΪ ![]() ��EΪCH3CH3 ��
��EΪCH3CH3 ��
(2) EΪCH3CH3�������ȴ���ΪCCl3CH2Cl��CHCl2CHCl2����2�ֽṹ��
�ʴ�Ϊ��2��
(3) C��������Ȼ�̼��Һ��Ӧ�Ļ�ѧ����ʽΪ��CH2=CH2+Br2��CH2BrCH2Br��
�ʴ�Ϊ��CH2=CH2+Br2��CH2BrCH2Br��
(4) �����漰�Ļ�ѧ����ʽΪ��![]() +Br2
+Br2![]()
![]() +HBr��
+HBr��
�ʴ�Ϊ��![]() +Br2
+Br2![]()
![]() +HBr��
+HBr��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ԭ��Ľṹ��ʽ��ͼ�������й���ԭ���˵��������ǣ�������
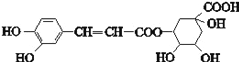
A. ����ʽΪC16H18O9 B. ����NaHCO3��Ӧ
C. �ܷ���ȡ����Ӧ��������Ӧ����ȥ��Ӧ D. 1 mol��ԭ�������6 mol Br2��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�ijͬѧ����CO2��Na2O2��Ӧ��̽��ʵ�飬�ش��������⡣
��1������ͼװ���Ʊ�������CO2
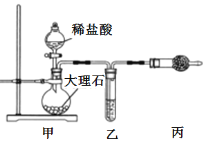
�ٱ�װ�õ�������___����װ����ʢװ���Լ���___��
����CO2 �л���HCl����HCl��Na2O2��Ӧ�Ļ�ѧ����ʽΪ____��
��2�����������װ��ͼ����ʵ�飨�г�װ���ԣ���
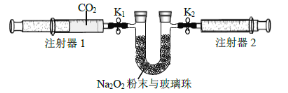
������װ������Ȼ��________������ע����1��ȡ100mL ������CO2������������K1 ����ע����2�Ļ����Ƶ���������K2 ������֧U �ι���װ��������Na2O2 ��ĩ�벣���顣
�ڴ�ֹˮ��K1��K2�������ƶ�ע����1�Ļ������ɹ۲쵽��������_____��
��ʵ������з�Ӧ�Ļ�ѧ����ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A ��һ���¶��·ֽ��������� B��C��D�� 2A B 2C 3D ����������ɻ�������������ͬ��ͬѹ����ͬ���H2 ������ 15 ��������� A ��Ħ�������ǣ� ��
A.30g / molB.60g / mol
C.90g / molD.120g / mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������450mL 0.2mol / L �� NaOH ��Һ��ʵ����������У�
A ��������ƽ��һ������ NaOH ���壬������������ˮʹ����ȫ�ܽ⣻
B ���ܽ�õ�����Һ����С�ĵ�ת�Ƶ�����ƿ�У�
C ����������ƿ�м�����ˮ��Һ���̶���1 ~ 2cm �������ý�ͷ�ι�С�ĵμ�����ˮ����Һ��Һ����ʹ���̶������У�
D ����������ˮϴ���ձ��Ͳ�����2~ 3 �Σ�ÿ�ε�ϴ��Һ��С��ע������ƿ����������
E ������ƿƿ���������������µߵ����ҡ�ȡ�����д���пհף�
��1�����������������ȷ˳��Ϊ������ţ�____________��
��2�������_____g �� NaOH ���壺�д���IJ���������_____������ţ���
��3�����������ʹ��ʵ��������ҺŨ��ƫ�ߵ���_____������ţ���
A ���ܽ����ʱ����Һ�彦����
B �� NaOH ����ֽ���ϳ�����
C NaOH ���ձ����ܽ������ת�Ƶ�����ƿ�У�
D �ô������������ƽ�� NaOH ʱ�������������������ķ�����
E ����ʱ���ӿ̶��ߣ�
F ����ƿδ���������ת����Һ��
G ҡ�Ⱥ���Һ���������ƿ�̶��ߣ�
H ������ˮʱ�����������˿̶��ߡ�
��4����ʵ����Ҫ�õ��Ķ��������������ձ���������ƽһ�ס��������⣬Ҫ��ɸ�ʵ�黹ȱ�ٵ�������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й���ͳ�Ļ������������Ĺ屦���Ŵ������м����˴����Ŵ���ѧ���о��ɹ����ش��������⣺
(1)�ҹ���ԭʼ���մ�Լ�����ھ��12000��ǰ�������������õ�ԭ���Ǹ���ʿ���侧�廯ѧʽ��Al4[Si4O10](OH)8�����������ʾ�����Ϊ______________��
(2)�����ݸ�Ŀ���м��أ���(��ҩ)������( KNO3)����ǡ�ɼľ̿���ϣ���Ϊ����糧���ҩ�ߡ�����Ӧԭ��Ϊ��S+2KNO3+3C![]() K2S+N2��+3CO2�����÷�Ӧ����������_________ ����Ӧת��4mol����ʱ����S������C��____________mol��
K2S+N2��+3CO2�����÷�Ӧ����������_________ ����Ӧת��4mol����ʱ����S������C��____________mol��
(3)�ҹ��Ŵ���ҩѧ���������ޱ��ݡ����ص�ҩ����844�֣������й����෯��������Ϊ����������ɫ���³���δ�����ߣ������������֮��ɫ�������ҹ����ڿƼ����顶����С��-��ʯ�ࡷ �����м����෯ʱ�ľ������෯����Ѭ�ˣ��·���֮���ã���ľ��ʢ�����෯�����̷�( FeSO4��7H2O)������������Ϣ��д�����෯�����ȷֽ�Ļ�ѧ����ʽ_____________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�����ֵ�������й�������ȷ����(����)
A. 14 g��ϩ�ͱ�ϩ��������е���ԭ����Ϊ2NA
B. 1 mol N2��4 mol H2��Ӧ���ɵ�NH3������Ϊ2NA
C. 1 mol Fe���ڹ������ᣬ����ת����Ϊ2NA
D. ��״���£�2.24 L CCl4���еĹ��ۼ���Ϊ0.4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��Q��T��XԪ��Ϊ����Ԫ�أ�Xԭ�ӵ�M����������δ�ɶԵ������չ����Yԭ�ӵļ۵����Ų�ʽΪ3d64s2��Zԭ�ӵ�![]() ���Ӳ��p�ܼ�����һ���չ����Qԭ�ӵ�L���Ӳ��p�ܼ���ֻ��һ�ԳɶԵ��ӣ�Tԭ�ӵ�M���Ӳ���p����������������������ȷ���ǣ� ��
���Ӳ��p�ܼ�����һ���չ����Qԭ�ӵ�L���Ӳ��p�ܼ���ֻ��һ�ԳɶԵ��ӣ�Tԭ�ӵ�M���Ӳ���p����������������������ȷ���ǣ� ��
A.Ԫ��Y��Q���γɻ�����Y2Q3
B.X��![]() ������������Ӧ��ˮ���ǰ�ߵ����ԱȺ���ǿ
������������Ӧ��ˮ���ǰ�ߵ����ԱȺ���ǿ
C.X��Q������ɵĻ�����Ϊ���ӻ�����
D.ZQ2���ɼ��Լ����ɵķǼ��Է���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(H2N��NH2)��ƫ������[H2N��N(CH3)2]�����������ȼ�ϡ��������ϵ�֪������һ�����õļ����ܼ������·������ģ�͵ĵ�����������۲죬������ƽ��ͼ����ͼ��ʾ������˵������ȷ����
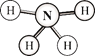
A.�·����еĵ�ԭ�Ӳ���sp3�ӻ�
B.�·����м��м��Լ����зǼ��Լ�
C.�·����ǷǼ��Է���
D.����ƫ�����»���ͬϵ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com