
【题目】研究性学习小组在辛集中学的玫瑰园与辛中公园附近分别采集一份土壤,分别配制成体积相同的两份营养液,其中两份各成分的含量如下:
含量 成分 | KCl | K2SO4 | ZnSO4 | ZnCl2 |
① | 0.3mol | 0.2mol | 0.1mol | ﹣ |
② | 0.1mol | 0.3mol | ﹣ | 0.1mol |
两份营养液的成分
A. 完全不同 B. 完全相同
C. 只有n(K+)相同 D. 只有 n(Cl﹣)相同
【答案】B
【解析】
第一份营养液中,0.3mol KCl里面有0.3mol 钾离子和0.3mol 氯离子, 0.2mol 硫酸钾里面有0.2mol![]() =0.4mol钾离子和0.2mol 硫酸根离子, 硫酸锌里面有0.1mol 锌离子和0.1mol 硫酸根离子,那么总共此营养液里面有:n(K)=0.3mol+0.4mol=0.7mol ,n(SO42-)=0.2mol+0.1mol=0.3mol n(Zn2+)=0.1mol, n(Cl-)=0.3mol 。第二份营养液中, 0.1mol KCl 里面有0.1mol 钾离子和0.1mol氯离子, 0.3mol硫酸钾里面有0.3mol
=0.4mol钾离子和0.2mol 硫酸根离子, 硫酸锌里面有0.1mol 锌离子和0.1mol 硫酸根离子,那么总共此营养液里面有:n(K)=0.3mol+0.4mol=0.7mol ,n(SO42-)=0.2mol+0.1mol=0.3mol n(Zn2+)=0.1mol, n(Cl-)=0.3mol 。第二份营养液中, 0.1mol KCl 里面有0.1mol 钾离子和0.1mol氯离子, 0.3mol硫酸钾里面有0.3mol![]() 2=0.6mol钾离子和0.3mol 硫酸根离子, 0.1mol 氯化锌里面0.1mol有0.1mol 锌离子和0.1mol
2=0.6mol钾离子和0.3mol 硫酸根离子, 0.1mol 氯化锌里面0.1mol有0.1mol 锌离子和0.1mol![]() 2=0.2mol 氯离子,则第二份营养液内有: :n(K)=0.1mol+0.6mol=0.7mo , n(SO42-)=0.3mol , n(Zn2+)=0.1mol , n(Cl-)=0.1mol +0.1mol =0.3mol ;对比以上可以知道:因体积相同,两种营养液相同离子的物质的量相同,则两种营养液离子浓度完全相同。A. 完全不同不符合题意,故A错误;B. 完全相同符合题意,故B正确;C. 只有n(K+)相同不符合题意,故C错误 ;D. 只有 n(Cl﹣)相同不符合题意,故D错误。答案:B。
2=0.2mol 氯离子,则第二份营养液内有: :n(K)=0.1mol+0.6mol=0.7mo , n(SO42-)=0.3mol , n(Zn2+)=0.1mol , n(Cl-)=0.1mol +0.1mol =0.3mol ;对比以上可以知道:因体积相同,两种营养液相同离子的物质的量相同,则两种营养液离子浓度完全相同。A. 完全不同不符合题意,故A错误;B. 完全相同符合题意,故B正确;C. 只有n(K+)相同不符合题意,故C错误 ;D. 只有 n(Cl﹣)相同不符合题意,故D错误。答案:B。


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】与醋酸有关的反应方程式正确的是
A. 与烧碱反应:OH-+CH3COOH → CH3COO-+H2O
B. 与CaCO3反应:CO32-+2CH3COOH → 2CH3COO-+CO2↑+H2O
C. 乙醛氧化:CH3CHO+O2 ![]() CH3COOH
CH3COOH
D. 制乙酸乙酯:CH3COOH+C2H518OH ![]() CH3COOC2H5+H218O
CH3COOC2H5+H218O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修5有机化合物】甲苯是有机化工生产的基本原料之一。利用乙醇和甲苯为原料,可按下列路线合成分子式均为C9H10O2的有机化工产品E和J。

已知:
请回答:
(1)写出下列反应方程式
①B+D→E______________________________________。
②G→H________________________________________。
(2)①的反应类型为__________;②的反应类型为__________;F的结构简式为__________。
(3)E、J有多种同分异构体,写出符合下列条件的4种同分异构体的结构简式。要求:①与E、J属同类物质②苯环上有两个取代基且苯环上的一氯代物只有两种。
__________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 铅蓄电池放电时的负极和正极的质量均增加
B. MgO(s)+C(s)![]() Mg(s)+CO(g)在室温下不能自发进行,说明该反应的△H <0
Mg(s)+CO(g)在室温下不能自发进行,说明该反应的△H <0
C. 对于发应2H2O2![]() 2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率
2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率
D. H2O与金属Na反应生成1molH2,反应中转移的电子数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应方程式,书写正确的是
A. 碳酸钠溶液中加入盐酸 CO32-+2H+=H2O+CO2↑
B. 稀硫酸中加入铁粉 2Fe+6H+=2Fe3++3H2↑
C. 碳酸钙中加入盐酸 CO32-+2H+=H2O+CO2↑
D. 氢氧化钡溶液中加入硫酸 H++OH-=H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,a、b、c……为部分元素。回答下列问题:

(1)请写出上述元素c原子基态核外电子排布式_______________; d+基态核外电子排布式_______________________________。
(2)请写出一个能比较f、h非金属性强弱的反应的化学方程式___________________。
(3)请比较f、h、i 三种元素的第一电离能由大到小的顺序________(写元素符号);b、e、j三种元素的电负性由大到小的顺序________(写元素符号)。i2-与b+两种微粒半径大小: i2-___b+ (填>、=或<)。
(4)请写出e 元素最高价氧化物对应的水化物与a、b、i三种元素形成的化合物反应 的离子方程式___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.lmol/L的K2CO3溶液中,由于CO32-的水解,使得c(CO32-)<0.lmol/L。如果要使c(CO32-)更接近于0.lmol/L,可以采取的措施是( )
A.加入少量盐酸 B.加入适量的水 C.加入适量的KOH D.加热
查看答案和解析>>
科目:高中化学 来源: 题型:
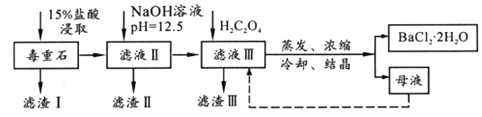
【题目】BaCl2可用于电子、仪表等工业。以毒重石(主要成分BaCO3,含少量CaCO3、MgSO4、Fe2O3、SiO2等杂质)为原料,模拟工业提取BaCl2·2H2O的流程如下:
已知:(1)Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(2)离子浓度小于至1×10-5认为沉淀完全。
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.0 | 3.7 |
(1)滤渣I的成分为________(填化学式),过滤所需玻璃仪器有______________。
(2)加入NaOH溶液后所得滤液III中,含有的Mg2+浓度为_____;加入H2C2O4时应避免过量,其原因是__________________________________。
(3)BaCl2母液中除了含有Ba+、Cl-外,还含有大量的______(填离子符号)。有人从“绿色化学”角度设想将“母液”沿虚线进行循环使用,请分析在实际工业生产中是否可行,_______(填“可行”或“不可行”),理由是_______________________。
(4)滤渣III是结石的主要成分,现将滤渣III 经过洗涤干燥后在有氧环境下进行热重分析,取146.0g灼烧,所得参数如下表。
溫度(℃) | 常温 | 190200 | 470480 |
质量(g) | 146.0 | 128.0 | 100.0 |
滤渣III 的成分是__________(填化学式);200~470℃时发生反应的化学方程式为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com