
����Ŀ�����ǻ��ʳ�εķ�ʽ�ж��֣�����Ҫ���Ǻ�ˮɹ�Ρ�ͨ����ˮ��ɹ�õ��Ĵ��γ�NaCl�⣬������MgCl2��CaCl2��Na2SO4�Լ���ɳ�����ʣ��������Ʊ����ε�ʵ�����̣��Լ��Ի�ѧʽ��ʾ��
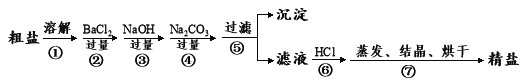
��1��BaCl2��NaOH��Na2CO3�ļ���˳���뱣֤___________��____________��
��2���ܽ⡢���ˡ����������ж�ʹ�õ��IJ���������_______ _________������ʱ��������������______________________
��3�������ݲ���֮��õ��ij����ijɷ�Ϊ��________________________
��4���Ƶõľ����в�С�Ļ���������ؾ��壬�õ�����ƽ��ȡ8.00g��Ʒ����ˮ������Һ�м���������������Һ���������ij������ˡ�ϴ�ӡ�������Ƶ�������Ϊ14.35g�������Ʒ���Ȼ��Ƶ���������Ϊ______________��
���𰸡���1��Na2CO3��1�֣���BaCl2��1�֣���
��2����������1�֣������裬��ֹ���Ȳ����ȵ���Һ��ɽ���1�֣���
��3��Mg��OH��2��CaCO3��BaSO4��BaCO3��4�֣�����4��73.125%��3�֣���
��������
�����������1�����ڳ�ȥNa2SO4����Ҫ���������BaCl2���������µ���������Ba2+��Ҫ��Na2CO3��Һ������������Na2CO3�ȳ�ȥ����CaCl2������BaCl2��Һ��ȥ���е�Na2SO4���ʣ�������BaCl2��Ҫ�ټ���Na2CO3 ��Һ���д�����ʹ�������跱�������Ӳ���Ҫ���鷳�����BaCl2��NaOH��Na2CO3�ļ���˳���뱣֤Na2CO3��BaCl2��μӣ�
��2���ܽ⡢���ˡ����������ж�ʹ�õ��IJ��������Dz�����������ʱ�������������ǽ��裬��ֹ���Ȳ����ȵ���Һ��ɽ���
��3���������ˮ�м���BaCl2��Һ��������Ӧ��BaCl2+ Na2SO4 =BaSO4 ��+2NaCl��Ȼ��������Һ�м���NaOH��Һ��������Ӧ��MgCl2+2NaOH=Mg(OH)2��+2NaCl���ټ���Na2CO3 ��Һ������Ӧ��Na2CO3 + CaCl2=CaCO3��+2NaCl��Na2CO3 + BaCl2=BaCO3��+2NaCl����˲���֮��õ��ij����ijɷ�Ϊ��Mg(OH)2��CaCO3��BaSO4��BaCO3��
��4���Ƶõľ����в�С�Ļ���������ؾ��壬�õ�����ƽ��ȡ8.00g��Ʒ����ˮ������Һ�м���������������Һ���������·�ӦAgNO3 +NaCl��+NaNO3 ���������ij������ˡ�ϴ�ӡ�������Ƶ�������Ϊ14.35g��n��AgCl��=14.35g��143.5g/mol=0.1mol�������ClԪ���غ㣬��֪n��NaCl��=0.1mol��m��NaCl��=0.1mol��58.5g/mol=5.85g�������Ʒ���Ȼ��Ƶ���������Ϊ��5.85g��8.00g����100% =73.125%��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����᳦��ҩ����Ч�ɷ�M�ĺϳ�·�����������ַ�Ӧ��ȥ�Լ���������:
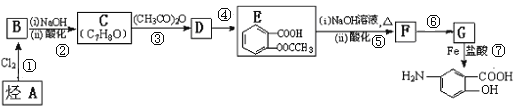
��֪����![]()
��![]()
��1����A��������______________��G�еĹ�����������_______________��
��2����Ӧ���ķ�Ӧ������__________����Ӧ���ķ�Ӧ������______________��
��3��E������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ��______________��
��4����������������D��ͬ���칹����___________�֡����к˴Ź���������4����ҷ����֮��Ϊ6:2:1:1�Ľṹ��ʽ��______________��
�����ڷ����廯�����ұ�������3��ȡ����
���ܺ�NaHCO3��Һ��Ӧ��������
��5����֪![]() �ױ��������������������ʱ������һ��ȡ��������ȡ����������ڶ�λ���������ϵĺϳ�·�ߣ����һ����AΪԭ�Ϻϳɻ�����
�ױ��������������������ʱ������һ��ȡ��������ȡ����������ڶ�λ���������ϵĺϳ�·�ߣ����һ����AΪԭ�Ϻϳɻ�����![]() �ĺϳ�·��______________��
�ĺϳ�·��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£����ڿ��淴ӦX��g��+3Y��g��![]() 2Z��g������X��Y��Z����ʼŨ�ȷֱ�Ϊ c1��c2��c3������Ϊ�㣩���ﵽƽ��ʱ��X��Y��Z��Ũ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.08mol/L���������ж���ȷ���ǣ� ��
2Z��g������X��Y��Z����ʼŨ�ȷֱ�Ϊ c1��c2��c3������Ϊ�㣩���ﵽƽ��ʱ��X��Y��Z��Ũ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.08mol/L���������ж���ȷ���ǣ� ��
A��c1��c2=3��1 B��ƽ��ʱ��Y��Z����������֮��Ϊ2��3
C��X��Y��ת������� D��c1��ȡֵ��ΧΪ0.04 mol/L��c1��0.14 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ڹ�ũҵ������������Ҫ����;�������Ҫ��������и��⡣
I.ij��ѧ��ȤС����������װ����ѡȡ��Ҫ��װ����ȡ��NH4��2SO4��Һ��

��1����װ��A�Ʊ�����ʱ������a���Ƿ��а��������ķ�����____________��
��2����ȡ��NH4��2SO4��Һʱ�������ӵ�˳�����ýӿ������ĸ��ʾ���ǣ�a �� _____________��
��3����װ��C������Һ���������IJ��������� ��
��.Ϊ����Ȼ�淋ľ��ü�ֵ���ҹ���ѧ�����������������þ�ȷֽ��Ȼ���ư������õ���ʽ�Ȼ�þ[Mg��OH��Cl]�Ĺ��ա�ijͬѧ���ݸ�ԭ����Ƶ�ʵ��װ����ͼ��
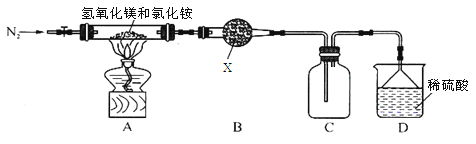
��4��װ��A�з�����Ӧ���ɼ�ʽ�Ȼ�þ�Ļ�ѧ����ʽΪ ��
��5��װ��B���Լ�XΪ________________��
��6������װ��ͼ�е�һ��������______________��
��7��MgCl2��6H2O�ڿ����м��ȣ�����Mg��OH��Cl������MgCl2��6H2O�Ʊ���ˮMgCl2��Ӧ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ��Һ���ܴ��������һ�������ǣ� ��
A��NH4+ ��Ba2+��Br-��CO32- B��Cl-��SO32-��Fe2+��H+
C��K+��Na+��SO42-��MnO4- D��Na+��H+��NO3-��HCO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��

��1����Ҫ��ȡŨ����_________mL��
��2�����Ƹ�ϡ����ʱʹ�õ���������Ͳ���ձ����������⣬ �������õ��������� �� ��
��3����ʵ���������������������Һ��Ũ�Ȼᣨ����ƫ��������ƫ����������������
A������ʱ���ӿ̶���_________��
B������ƿ�ڱڸ���ˮ���δ���ﴦ��______ ��
C���ܽ��û����ȴ����ж���_____ ��
��4���������Ƶ�ϡ���ᵹ��5.92g Na2CO3��NaHCO3�Ĺ��������У�ǡ����ȫ��Ӧ����ԭ�������Na2CO3����������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����������ʶ��ȷ���ǣ� ��
A. ���顢�������ܷ���������Ӧ
B. ��ϩ������ϩ��������ˮ�����ӳɷ�Ӧ
C. һ�ȱ��飨C3H7Cl����ͬ���칹�干��3��
D. ������������֬��NaOH��Һ��Ӧ���д�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȼ�ϵ��������������(Westinghouse)��˾���ƿ����ģ����Թ��������һ������Ϊ����ʣ����ֹ��������ڸ���������������(O2-)�����ͨ�����õ�صĹ���ԭ����ͼ��ʾ�����ж�缫a��b��������缫��Ӧ�������ж���ȷ����
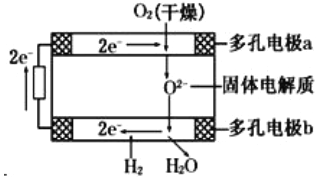
A����O2�ŵ��a��Ϊ��صĸ���
B��O2-�����ص�����
C��b����Ӧ�ĵ缫��ӦΪ2H2- 4e-+2O2-=2H2O
D��a����Ӧ�ĵ缫��ӦΪO2+2H2O+4e-=4OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������ƣ���������������������Һ�����ʷ�Ӧ������������Ӧ�������Ȼ���(BCl3�������ɵ����Ȼ�����ˮˮ���������(��֪��BCl3���۵�Ϊ��107.3 �棬�е�Ϊ12.5 �����������Ȼ���������ȡ������(B2H6����ij��ȤС�������ͼ��ʾװ���Ʊ����Ȼ���
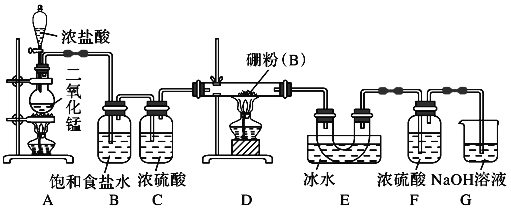
�ش��������⣺
��1�� װ��D�з�����Ӧ�Ļ�ѧ����ʽΪ_____________________��
��2��װ��B��E�����÷ֱ���_________________________��
��3��������ʢװ___________(���Լ��������ĸ���ܴ���װ��F��G��ʹʵ�����㡣
��4��Ϊ��˳�����ʵ�飬��ȼ�ƾ��Ƶ���ȷ������_________(����ĸ������������_________________��
a���ȵ�ȼA���ƾ��ƣ����ȼD���ƾ���
b���ȵ�ȼD���ƾ��ƣ����ȼA���ƾ���
c��ͬʱ��ȼA��D�����ƾ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com