
【题目】下列说法正确的是( )
A.PH=10的Mg(OH)2浊液C(Mg2+)=10﹣8 molL﹣1 (已知Mg(OH)2KSP=1×10﹣16)
B.已知AgClKSP=1.8×10﹣10;Ag2CrO4KSP=1.2×10﹣12则AgCl的溶解度一定比Ag2CrO4大
C.在饱和AgCl溶液中加入NaI固体不会发生变化
D.Fe3+在酸性溶液中一定不会生成Fe(OH)3沉淀
【答案】A
【解析】解:A、PH=10的Mg(OH)2浊液,c(OH﹣)=10﹣4mol/L,根据Ksp=c(Mg2+)c2(OH﹣),所以c(Mg2+)= ![]() =10﹣8 molL﹣1 , 故A正确; B、设AgCl溶解的浓度为xmol/L,则溶液中的银离子浓度为xmol/L,氯离子也为xmol/L,则根据溶度积为1.8×10﹣10=x×x,解得x=1.35×10﹣5mol/L
=10﹣8 molL﹣1 , 故A正确; B、设AgCl溶解的浓度为xmol/L,则溶液中的银离子浓度为xmol/L,氯离子也为xmol/L,则根据溶度积为1.8×10﹣10=x×x,解得x=1.35×10﹣5mol/L
同理设Ag2CrO4溶解的浓度为ymol/L,则溶液中的银离子浓度为2ymol/L,氯离子也为ymol/L,再根据溶度积为1.2×10﹣12=(2y)2×y,解得y=0.8×10﹣4mol/L,故溶解度较小的物质是AgCl,故溶度积小的溶解度反而大,所以Ksp的大小与溶解能力没有一定的关系,故B错误;
C、在饱和AgCl溶液中加入NaI固体,生成溶度积极小的黄色碘化银沉淀,故C错误;
D、铁离子在强酸性溶液中能稳定存在,弱酸性溶液中转化为氢氧化铁沉淀,故D错误;
故选A.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 太阳能电池板与光导纤维的材料主要是晶体硅
B. 可以用澄清石灰水鉴别小苏打溶液与苏打溶液
C. 工业冶炼粗硅的原理:SiO2+C![]() CO2↑+Si
CO2↑+Si
D. 普通玻璃的主要成分是硅酸钠、硅酸钙和二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在水中的电离方程式书写错误的是
A.CaCl2=Ca2++2Cl-B.Ba(OH)2=Ba2++OH2-
C.KOH=K++OH-D.H2SO4=2H++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示在密闭容器中反应:2SO2+O22SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是;bc过程中改变的条件可能是; 若增大压强时,反应速度变化情况画在c~d处 . 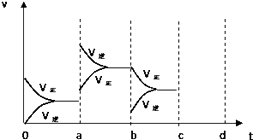
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应A(g)+B(g)C(g)△H<0达到平衡后,据下列图象判断:
达到新的平衡对应的图象 | 平衡移动方向 | |
(i)使用催化剂 | ||
(ii)升温 | ||
(iii)降压 | ||
(iv)增加A的量 | ||
(v)减少C的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~E为中学常见的物质,有如图所示转化关系,已知A为金属单质。请回答:

(1)A的化学式为________。
(2)在B的溶液中加入NaOH溶液后可观察到的现象为_________。C转变为D的化学方程式为_____________。
(3)向E溶液中加入A时发生反应的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】媒化学小组设计了细下的实验装置制取Cl2和SO2,并研究它们的漂白性。请问答:

(1)若用装置A 制取Cl2,可选择二氧化锰固体和浓盐酸,反应的离子方程式为_______。若用装置B制取SO2,可选择亚硫酸钠固体和浓硫酸,反应的化学方程式为__________。
(2)反应开始一段时间后,观察到C、D两个试管中的品红溶液_______(填写序号)。
①都褪色 ②都不褪色 ③C褪色,D不褪色 ④C不褪色,D褪色
停止通气后,取下C、D,再分别给C、D 两个试管加热,两个试管中的现象分别为C:______,D:_______。
(3)烧杯E中可盛装_______(填化学式)溶液,其作用是____________。
(4)某同学将制得的SO2和Cl2等体积混合后通入到品红溶液中,观察到的现象是________,用离子方程式表示产生该现象的原因_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到预期目的是( )
A.用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸
B.用食醋和澄清石灰水验证蛋壳中含碳酸盐
C.直接往淀粉水解液中滴入银氨溶液可产生银镜
D.用分液漏斗分离溴和苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用软锰矿(主要含MnO2,还含有少了SiO2、Al2O3 、Fe2O3等杂质)模拟工业制高锰酸钾流程如下。试回答下列问题。
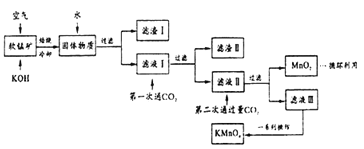
(1)配平焙烧时MnO2参与的化学反应:□MnO2+□_____+□O2 ![]() □K2MnO4+□H2O;第二次通入过量CO2时发生反应的离子方程式为:______________________。
□K2MnO4+□H2O;第二次通入过量CO2时发生反应的离子方程式为:______________________。
(2)滤渣I、II的成分中能与NaOH 反应的是__________________ (填化学式)。产生滤渣II时不能用稀盐酸代替CO2,因为______________________。
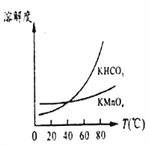
(3)将滤液Ⅲ进行一系列操作可得到KMnO4晶体。由下图可知,从滤液Ⅲ得到KMnO4需经过____、____洗涤等操作。
(4)用重结晶提纯的产品配制成0.10mol·L-1 的酸性KMnO4溶液来测定某草酸样品的纯度(杂质不参与反应,草酸为弱酸,分子式H2C2O4)。
①试给出反应的离子方程式:_______________________。
②若某测定大致共需要230毫升酸性KMnO4溶液,配制时所需玻璃仪器为:___、___烧杯、胶头滴管等。
③取草酸样品5 克,配成100mL溶液,取20mL于适当容器中,用前述所配酸性KMnO4溶液滴定,至反应结束消耗KMnO4溶液20mL,则样品的纯度为: ___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com