
����Ŀ����ҵ�ϳ����ú����ˮ����![]() ��ʵ���ҿ�������װ��
��ʵ���ҿ�������װ��![]() ��ȥ���ּӳ�����
��ȥ���ּӳ�����![]() ģ�����ɹ��̣�
ģ�����ɹ��̣�
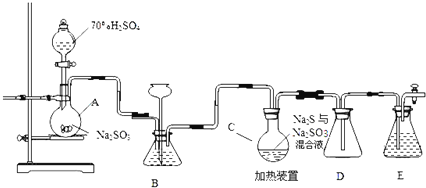
��ƿC�з�����Ӧ���£�
![]()
![]() ��
��![]()
![]()
![]() ��
��![]()
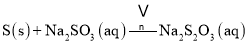
![]() ��
��![]()
(1)װ��A�з����Ļ�ѧ��Ӧ����ʽΪ ______
(2)Ϊ��߲�Ʒ���ȣ�Ӧʹ��ƿC��![]() ��
��![]() ǡ����ȫ��Ӧ������ƿC��
ǡ����ȫ��Ӧ������ƿC��![]() ��
��![]() ���ʵ���֮��Ϊ ______ ��
���ʵ���֮��Ϊ ______ ��
(3)װ��B������֮һ�ǹ۲�![]() ���������ʣ����е�Һ�����ѡ�� ______
���������ʣ����е�Һ�����ѡ�� ______
a.����ˮb.����![]() ��Һ c.����
��Һ c.����![]() ��Һd.����
��Һd.����![]() ��Һ
��Һ
ʵ���У�Ϊʹ![]() ����������ƿC�����õIJ����� ______ ��
����������ƿC�����õIJ����� ______ ��
(4)��֪��Ӧ![]() ��
��![]() ��Խ���������ƿC�з�Ӧ�ﵽ�յ�������� ______ ��װ��E������Ϊ ______
��Խ���������ƿC�з�Ӧ�ﵽ�յ�������� ______ ��װ��E������Ϊ ______
(5)��Ӧ��ֹ����ƿC�е���Һ������Ũ����������![]() �����п��ܺ���
�����п��ܺ���![]() ��
��![]() �����ʣ����������Լ����ʵ�飬����Ʒ���Ƿ����
�����ʣ����������Լ����ʵ�飬����Ʒ���Ƿ����![]() ����Ҫ˵��ʵ�����������ͽ��ۣ� ______ ��
����Ҫ˵��ʵ�����������ͽ��ۣ� ______ ��
��֪��![]() �����ֽ⣺
�����ֽ⣺![]() ��ѡ����Լ���ϡ���ᡢϡ���ᡢϡ���ᡢ
��ѡ����Լ���ϡ���ᡢϡ���ᡢϡ���ᡢ![]() ��Һ��
��Һ��![]() ��Һ��
��Һ��
���𰸡�![]() 2��1 c ���Ƶμ�������ٶ� ��Һ�����
2��1 c ���Ƶμ�������ٶ� ��Һ�����![]() �������ʧ
�������ʧ![]() ����
����![]() ��ֹ��Ⱦ���� ȡ������Ʒ��������ϡ�����У����ã�ȡ�ϲ���Һ
��ֹ��Ⱦ���� ȡ������Ʒ��������ϡ�����У����ã�ȡ�ϲ���Һ![]() ����˺�ȡ��Һ
����˺�ȡ��Һ![]() ���μ�
���μ�![]() ��Һ�������ְ�ɫ������˵������
��Һ�������ְ�ɫ������˵������![]() ����
����
��������
![]() ����װ��ͼ��֪��A�еķ�ӦΪŨ�������������Ʒ�Ӧ���ɶ�������
����װ��ͼ��֪��A�еķ�ӦΪŨ�������������Ʒ�Ӧ���ɶ�������
![]() ��
��![]() ��
��![]() ǡ����ȫ��Ӧ������ձ�C�еķ�Ӧ������
ǡ����ȫ��Ӧ������ձ�C�еķ�Ӧ������
![]() �۲�
�۲�![]() ���������ʣ�װ��B�е���Һ�������������ӦҲ�������ն�������ͨ�����Ƶμ�������ٶȣ����Կ��Ʋ���������������ʣ��ݴ˴��⣻
���������ʣ�װ��B�е���Һ�������������ӦҲ�������ն�������ͨ�����Ƶμ�������ٶȣ����Կ��Ʋ���������������ʣ��ݴ˴��⣻
![]() ����C�з����ķ�Ӧ��֪����ƿC�з�Ӧ�ﵽ�յ㷢���ķ�ӦΪ�����������Ʒ�Ӧ������������ƣ���Ӧβ������δ��Ӧ�Ķ����������壬����Ⱦ������
����C�з����ķ�Ӧ��֪����ƿC�з�Ӧ�ﵽ�յ㷢���ķ�ӦΪ�����������Ʒ�Ӧ������������ƣ���Ӧβ������δ��Ӧ�Ķ����������壬����Ⱦ������
![]() ����Ʒ���Ƿ����
����Ʒ���Ƿ����![]() ���ȼ������ų����ţ��������Ȼ���������������ӡ�
���ȼ������ų����ţ��������Ȼ���������������ӡ�
![]() ����װ��ͼ��֪��A�еķ�ӦΪŨ�������������Ʒ�Ӧ���ɶ�������Ӧ�Ļ�ѧ����ʽΪ��
����װ��ͼ��֪��A�еķ�ӦΪŨ�������������Ʒ�Ӧ���ɶ�������Ӧ�Ļ�ѧ����ʽΪ��![]() ��
��
�ʴ�Ϊ��![]() ��
��
![]() ��
��![]() ��
��![]() ǡ����ȫ��Ӧ����
ǡ����ȫ��Ӧ����![]() ��
��![]()
![]() ��
��![]()
![]() ��
��![]()
��֪��![]() ��
��![]() ��
��![]() ��
��![]() ���õ��ܷ�ӦΪ
���õ��ܷ�ӦΪ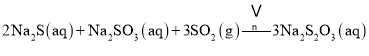 ����C��
����C��![]() ��
��![]() ���ʵ���֮��Ϊ2��1��
���ʵ���֮��Ϊ2��1��
�ʴ�Ϊ��2��1��
![]() �۲�
�۲�![]() ���������ʣ�����ǿ����ȡ����ķ�Ӧ��a�����ɶ�������bd�����ʾ����������Ӧ��ֻ��c�б���
���������ʣ�����ǿ����ȡ����ķ�Ӧ��a�����ɶ�������bd�����ʾ����������Ӧ��ֻ��c�б���![]() ��Һ�ʺ���ȡ��������ͨ�����Ƶμ�������ٶȣ����Կ��Ʋ���������������ʣ�����Ϊʹ
��Һ�ʺ���ȡ��������ͨ�����Ƶμ�������ٶȣ����Կ��Ʋ���������������ʣ�����Ϊʹ![]() ����������ƿC�����õIJ����ǿ��Ƶμ�������ٶȣ�
����������ƿC�����õIJ����ǿ��Ƶμ�������ٶȣ�
�ʴ�Ϊ��c�����Ƶμ�������ٶȣ�
![]() ����C�з����ķ�Ӧ��֪����ƿC�з�Ӧ�ﵽ�յ㷢����ӦΪ�����������Ʒ�Ӧ������������ƣ���Ӧ������Ϊ��Һ�����
����C�з����ķ�Ӧ��֪����ƿC�з�Ӧ�ﵽ�յ㷢����ӦΪ�����������Ʒ�Ӧ������������ƣ���Ӧ������Ϊ��Һ�����![]() �������ʧ
�������ʧ![]() ����Ӧβ������δ��Ӧ�Ķ����������壬����Ⱦ����������Ҫ��Eװ������
����Ӧβ������δ��Ӧ�Ķ����������壬����Ⱦ����������Ҫ��Eװ������![]() ��ֹ��Ⱦ������
��ֹ��Ⱦ������
�ʴ�Ϊ����Һ�����![]() �������ʧ
�������ʧ![]() ������
������![]() ��ֹ��Ⱦ������
��ֹ��Ⱦ������
![]() ����Ʒ���Ƿ����
����Ʒ���Ƿ����![]() ������������ͽ���Ϊȡ������Ʒ��������ϡ�����У����ã�ȡ�ϲ���Һ
������������ͽ���Ϊȡ������Ʒ��������ϡ�����У����ã�ȡ�ϲ���Һ![]() ����˺�ȡ��Һ
����˺�ȡ��Һ![]() ���μ�
���μ�![]() ��Һ�������ְ�ɫ������˵������
��Һ�������ְ�ɫ������˵������![]() ���ʣ�
���ʣ�
�ʴ�Ϊ��ȡ������Ʒ��������ϡ�����У����ã�ȡ�ϲ���Һ![]() ����˺�ȡ��Һ
����˺�ȡ��Һ![]() ���μ�
���μ�![]() ��Һ�������ְ�ɫ������˵������
��Һ�������ְ�ɫ������˵������![]() ���ʡ�
���ʡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(![]() )ΪһԪ���ᣬ�㷺���ڲ�����ҽҩ��ұ��Ƥ��ȹ�ҵ���ش��������⣺
)ΪһԪ���ᣬ�㷺���ڲ�����ҽҩ��ұ��Ƥ��ȹ�ҵ���ش��������⣺
(1)![]() ��BԪ�صĻ��ϼ�Ϊ______��
��BԪ�صĻ��ϼ�Ϊ______��
(2)��֪��![]() ��
��![]() �ĵ��뷽��ʽΪ____�����ԣ�
�ĵ��뷽��ʽΪ____�����ԣ�![]() ___(����������������)
___(����������������)![]() ��
��
(3)![]() ���ȷֽ�õ�
���ȷֽ�õ�![]() ��
��![]() ��þ�ۻ�ϵ�ȼ�ɵõ���B��д�����ɵ���B�Ļ�ѧ����ʽ________���÷�Ӧ���������ͻ�ԭ�����ʵ���֮��Ϊ______��
��þ�ۻ�ϵ�ȼ�ɵõ���B��д�����ɵ���B�Ļ�ѧ����ʽ________���÷�Ӧ���������ͻ�ԭ�����ʵ���֮��Ϊ______��
(4)![]() �����������������NaBH4���漰����Ҫ��ӦΪ��
�����������������NaBH4���漰����Ҫ��ӦΪ��
��.![]()
��.![]()
������Ӧ����������Ϊ______(����)��
a.ȡ����Ӧ b.�ӳɷ�Ӧ c.�Ӿ۷�Ӧ d.������Ӧ
��NaH�ĵ���ʽΪ____________��
���ڼ��������£�NaBH4��CuSO4��Һ��Ӧ�ɵ�Cu��![]() ������HԪ����
������HԪ����![]() ������Ϊ
������Ϊ![]() �ۣ��÷�Ӧ�����ӷ���ʽΪ______��
�ۣ��÷�Ӧ�����ӷ���ʽΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W��Ԫ�����ڱ��е����λ����ͼ��ʾ������Wԭ�ӵ�ԭ��������������������������������˵����ȷ���ǣ�������
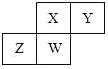
A.ԭ�Ӱ뾶��W��Z��Y��X
B.����������Ӧˮ��������ԣ�Z��W��X
C.�����̬�⻯������ȶ��ԣ�Y��X��W��Z
D.Ԫ��X��Y��Z��W������ϼ۷ֱ����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ͼ���˵����ȷ����

A. ͼ�ױ�ʾ����ij������Һ����μ���NaOH��Һ�����������ɳ��������ʵ�����μ�NaOH��Һ����Ĺ�ϵ
B. ͼ�ұ�ʾ�������ʵ�����NaOH��Na2CO3�Ļ����Һ����μ���ϡ��������������������������μ�HCl��Һ����Ĺ�ϵ
C. ͼ����ʾ����ϡ������Һ��������������������Һ��Fe3�����ʵ����������������ʵ����ı仯��ϵ
D. ��ȥ������������������Ȼ��ƿ��á�����Ũ�������ȹ��ˡ��ķ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��100��ʱ����ij�����ܱ������м���1.6 mol ��L��1��Q��ᷢ�����·�Ӧ��2Q(g) ![]() M(g) ������M�����ʵ���Ũ����ʱ��ı仯��ͼ��ʾ��
M(g) ������M�����ʵ���Ũ����ʱ��ı仯��ͼ��ʾ��
����˵���������
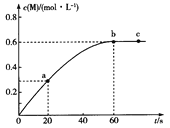
A.�ӷ�Ӧ��ʼ���մﵽƽ��ʱ����ڣ�v(Q)��0.02 mol��L��1��s��1
B.a��b��ʱ������Q�����ʣ�v(a)��v(b)
C.��QŨ�ȱ仯ֵ��ʾ��ab��bc����ʱ���ڵķ�Ӧ���ʣ�v(ab)��v(bc)��0
D.����������ͬ����ʼʱ��0. 2 mol��L��1������Q��ϣ���Ӧ�ﵽƽ������ʱ������60 s
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�������ճ������еijԡ�����ס���С�ҽ��ϵ���У�
��1����֬�����ۡ�������������ʳ�����ṩ��������Ҫ���ʣ��������ڶ��ܷ���ˮ�⡣
����֬������������ˮ������ղ�����_________��_________��
�������������ʲ����߷��ӻ��������_________����Ҫ��������ڵ���ø�������Ѿ�������ˮ�⣬��ȡ����ˮ��ʵ�����Һ����_________�����Լ������ƣ������Ⱥ��ٸ���ʵ�������жϣ���Ҫ�������û����ȫˮ��ģ���ȡ����ˮ����Һ���뼸��________��Ӧ�۲쵽������ɫ��
�۵�������������ˮ������ղ����ǰ����ᣮд�������Ṳͬ���еĹ����ŵĽṹ��ʽ�ֱ�Ϊ_________�ͩ�COOH��
��2������Խ��Խ������г��������Ͻ������ϣ�������������ۣ�����Ҳ���;ã����ܳ���ʹ�õ�ԭ����_________������������̥����Ҫԭ�ϣ���Ȼ��ͨ����ʩʹ�����ת��Ϊ_________���ӽṹ������ǿ�Ⱥ͵��ԣ�
��3���۱�ϩ�橁�ϳ������ֳ�������ë����ϩ��ΪCH2=CHCN����д���۱�ϩ��Ľṹ��ʽ_________�������г����õ���ϵ�������⣬������������һ�ֳ�������������Ҫ����Ϊ��ṹ�к���_________�����ֳ�ǿ�����ԣ�
��4��_________�γɵĺϽ𱻳�Ϊ����������������㷺��Ϊ����ǵIJ��ϣ�Ϊ��ֹ��ҵ�������̲��������������������������Խ��������������������ͨ���������д�����
��5������װ�����õ���Щʯ�Ļ��ͷų�һ�ַ��������ʣ����ڽӴ���������֢�����߹����쳣���÷�����������Ҫ��_________����д�����ʵ����ƣ���
��6������������̼��þ������������θ���������IJ��ʣ���ֱ�д����ط�Ӧ�����ӷ���ʽ����_________��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ʵ���ҽ��а��������Ʊ�������ʵ������װ�ã����̶ֹ�װ��δ������
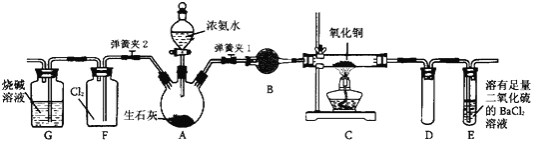
��1������װ��װ�ú���Ҫ����A��Eװ�õ������ԣ������������____��Ȼ����A���۲쵽E��������ð�����ƿ��ƾ��ƻ��ɿ�˫�֣�E�е�����ˮ���γɣ�˵��װ�����������á�
��2��װ��B��ʢ�ŵ��Լ���________��
��3����ȼC���ƾ��ƣ��رյ��ɼ�2�����ɼ�l���ӷ�Һ©���ų�Ũ��ˮ����û��ƿ�й����رշ�Һ©�����Ժ�Ƭ�̣�װ��C�к�ɫ������죬װ��E����Һ����ִ������ݣ�ͬʱ�����ܲ�����������________����E���ݳ�Һ����������ֱ�������������д����C�з�����Ӧ�Ļ�ѧ����ʽ��________��
��4����C�й���ȫ�����ɫ�رյ��ɼ�1�������ƿ��ƾ��ƣ�����ȴ����C�й�������������Ӧǰ��������Ϊ16 g����Ӧ����ع�����������2.4 g��ͨ������ȷ���ù������ijɷ���________���û�ѧʽ��ʾ����
��5���ڹرյ��ɼ�1���ɼ�2�������������F�У��ܿ췢��װ��F�в������̣�ͬʱ����G����ҺѸ�ٵ�������F�С���д���������̵Ļ�ѧ����ʽ��________��Ѹ�ٲ���������ԭ����________��
��6��Ϊ������һˮ�ϰ�������ס�����ͬѧ�ֱ��������ʵ�����̽����
����ͬѧ��pH��ֽ���������0.l mol/L��ˮpHΪ10�����϶�һˮ�ϰ���������ʣ�������________��
����ͬѧȡ��10 mL 0��1 mol/L��ˮ������2�η�̪��Һ���Էۺ�ɫ���ټ���NH4Cl�����������۲쵽��������________����֤��һˮ̨����������ʡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Al-Ag2O�������ˮ�¶�����Դ����ԭ����ͼ��ʾ����ع���ʱ������˵���������

A.������Al�缫ͨ�����·����Ag2O/Ag�缫
B.��ظ���������ҺpH�½�
C.��Һ��OH����Al�缫�ƶ�
D.Al����ӦʽΪ��Al-3e��+3OH��=Al(OH)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��õ�����ζ�����а����nϩ���nϩ�ļ���ʽΪ��![]() ��
��
(1)1 mol�nϩ�����Ը�____ mol H2������Ӧ��
(2)д���nϩ�������ʵ�����Br2�����ӳɷ�Ӧ���ò���Ŀ��ܵĽṹ_______________ (�ü���ʽ��ʾ)��
(3)�л���A���nϩ��ͬ���칹�壬�����к��С�![]() ���ṹ��A���ܵĽṹΪ______���ü���ʽ��ʾ����
���ṹ��A���ܵĽṹΪ______���ü���ʽ��ʾ����
(4)д��![]() ��Cl2����1��4���ӳɷ�Ӧ�Ļ�ѧ����ʽ____________��
��Cl2����1��4���ӳɷ�Ӧ�Ļ�ѧ����ʽ____________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com