
����Ŀ����ѧ�������ճ������еijԡ�����ס���С�ҽ��ϵ���У�
��1����֬�����ۡ�������������ʳ�����ṩ��������Ҫ���ʣ��������ڶ��ܷ���ˮ�⡣
����֬������������ˮ������ղ�����_________��_________��
�������������ʲ����߷��ӻ��������_________����Ҫ��������ڵ���ø�������Ѿ�������ˮ�⣬��ȡ����ˮ��ʵ�����Һ����_________�����Լ������ƣ������Ⱥ��ٸ���ʵ�������жϣ���Ҫ�������û����ȫˮ��ģ���ȡ����ˮ����Һ���뼸��________��Ӧ�۲쵽������ɫ��
�۵�������������ˮ������ղ����ǰ����ᣮд�������Ṳͬ���еĹ����ŵĽṹ��ʽ�ֱ�Ϊ_________�ͩ�COOH��
��2������Խ��Խ������г��������Ͻ������ϣ�������������ۣ�����Ҳ���;ã����ܳ���ʹ�õ�ԭ����_________������������̥����Ҫԭ�ϣ���Ȼ��ͨ����ʩʹ�����ת��Ϊ_________���ӽṹ������ǿ�Ⱥ͵��ԣ�
��3���۱�ϩ�橁�ϳ������ֳ�������ë����ϩ��ΪCH2=CHCN����д���۱�ϩ��Ľṹ��ʽ_________�������г����õ���ϵ�������⣬������������һ�ֳ�������������Ҫ����Ϊ��ṹ�к���_________�����ֳ�ǿ�����ԣ�
��4��_________�γɵĺϽ𱻳�Ϊ����������������㷺��Ϊ����ǵIJ��ϣ�Ϊ��ֹ��ҵ�������̲��������������������������Խ��������������������ͨ���������д�����
��5������װ�����õ���Щʯ�Ļ��ͷų�һ�ַ��������ʣ����ڽӴ���������֢�����߹����쳣���÷�����������Ҫ��_________����д�����ʵ����ƣ���
��6������������̼��þ������������θ���������IJ��ʣ���ֱ�д����ط�Ӧ�����ӷ���ʽ����_________��_________��
���𰸡� ��֬���� ���� ��֬ ����������ͭ��������Һ ��ˮ ��NH2 ���������γ�������������п���ʴ�� ������״���� 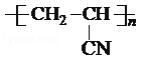 ��O��O��������� �� � Al��OH��3+3H+=Al3++3H2O MgCO3+2H+=Mg2++H2O+CO2��
��O��O��������� �� � Al��OH��3+3H+=Al3++3H2O MgCO3+2H+=Mg2++H2O+CO2��
����������1������֬����������������ˮ��Ϊ��֬��������ͣ�����֬������С��10000�������ڸ߷��ӻ��������ˮ������ղ����������ǣ�����������������������ͭ��������Һ����������Ƿ�ˮ�⣻���õ������۱���ɫ����������Ƿ���ȫˮ�⣻����������һ���������ܷ���ˮ�ⷴӦ������ת��Ϊ�����ᣬ�����Ṳͬ���еĹ����ŵĽṹ��ʽ�ֱ�Ϊ�������Ȼ���
��2������ѧ���ʻ��ã�����������ױ�����Ϊһ�����ܵ�������Ĥ�������ڲ��������ٱ���ʴ����Ȼ��ͨ��������ʹ���ķ���ת��Ϊ������״�ṹ���Ӷ�������ǿ�ȣ�
��3����ϩ��ͨ���Ӿ۷�Ӧ���ɾ۱�ϩ�棻����������һ�ֳ�����ɱ������������ԭ���ǹ�����������к���һ�ֽ������������������ʣ�
��4���Ѻ��ѺϽ����ʣ��������ʴ�ԣ��Ժ�ˮ�����������ɸ�ʴ���ʶ��ȶ��������Ժã�ǿ�ȴ��ܶ�С���ֳ������������
��5������װ���о����õ������ҡ�����ʯ�Ȳ��ϣ���Щ��ʯ����ͬ�̶ȵغ��з�����Ԫ�أ�����Щ�����ˡ��ʵĻ����һ��ͷų�����������뱣�
��6��θ�����Ҫ�ɷ�Ϊ���ᣬ�������ʵ����ʽ�����ӷ���ʽ����д������������
��1������֬����������������ˮ��Ϊ��֬��������ͣ�
�ʴ�Ϊ����֬���ᡢ���ͣ�
����֬������С��10000�������ڸ߷��ӻ��������ˮ������ղ����������ǣ����������£���������������ͭ��������Һ����ש��ɫ�������ɻ����������������˵�������Ѿ�ˮ�⣻��Һ�е����ˮ������������˵��������ȫˮ�⣬
�ʴ�Ϊ����֬������������ͭ��������Һ����ˮ��
����������һ���������ܷ���ˮ�ⷴӦ������ת��Ϊ�����ᣬ�����Ṳͬ���еĹ����ŵĽṹ��ʽ�ֱ�Ϊ�������Ȼ����ʴ�Ϊ��-NH2��
��2������ѧ���ʻ��ã�����������ױ�����Ϊһ�����ܵ�������Ĥ�������ڲ��������ٱ���ʴ����Ȼ��ͨ��������ʹ���ķ���ת��Ϊ������״�ṹ���Ӷ�������ǿ�ȣ��ʴ�Ϊ�����������γ�������������п���ʴ�ԣ�������״���ӣ�
��3����ϩ��ͨ���Ӿ۷�Ӧ���ɾ۱�ϩ�棬�۱�ϩ��ĽṹΪ![]() ������������һ�ֳ�����ɱ������������ԭ���ǹ�����������к���һ�ֽ������������������ʣ�
������������һ�ֳ�����ɱ������������ԭ���ǹ�����������к���һ�ֽ������������������ʣ�
�ʴ�Ϊ��![]() ��-O-O-���������
��-O-O-���������
��4���Ѻ��ѺϽ����ʣ��������ʴ�ԣ��Ժ�ˮ�����������ɸ�ʴ���ʶ��ȶ��������Ժã�ǿ�ȴ��ܶ�С���ֳ�������������ʴ�Ϊ���ѣ�
��5������װ���о����õ������ҡ�����ʯ�Ȳ��ϣ���Щ��ʯ����ͬ�̶ȵغ��з�����Ԫ�أ�����Щ�����ˡ��ʵĻ����һ��ͷų�����������뱣�
�ʴ�Ϊ��뱣�
��6��θ�����Ҫ�ɷ�Ϊ���ᣬθ��������������Ӧ�����Ȼ�����ˮ����Ӧ�����ӷ���ʽΪAl��OH��3+3H+=Al3++3H2O��
θ����̼��þ��Ӧ�����Ȼ�þ�Ͷ�����̼�����ˮ����Ӧ�����ӷ���ʽΪMgCO3+2H+=Mg2++H2O+CO2����
�ʴ�Ϊ��Al��OH��3+3H+=Al3++3H2O �� MgCO3+2H+=Mg2++H2O+CO2����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��ʵ����������AgNO3����Һʱ������AgNO3���������ڽ�Ũ�������У�Ȼ����������ˮϡ�͵������Ũ�ȣ���Ŀ����_________________________________________________��
��2��FeCl3��ˮ��ԭ���ǣ������ӷ���ʽ��ʾ����______________________________��AlCl3��Һ���ɣ����գ����õ�����Ҫ���������_________ ��
��3���ô�����Һ����ϴ����,��ԭ���ǣ������ӷ���ʽ��ʾ����_________________________
��4����ĭ�������װ��NaHCO3������Һ������Һ���ּ��Ե�ԭ���ǣ������ӷ���ʽ��ʾ��______�����������һ������װ��Al2��SO4��3��Һ������Һ�����Ե�ԭ���ǣ������ӷ���ʽ��ʾ����_________________________��������ʧ��ʱ��ʹ��ĭ�����������ҡ������ʹҩҺ��ϣ���������İ�ɫ��ĭ����ֹ�������ӣ�����ص����ӷ���ʽΪ��__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��������ϩ�������ұ������ⷴӦ���������������Ӧ����������������ʱ������˵����ȷ���ǣ�������

A. �����ʵ�������������߱���ϩ�IJ���
B. �ڱ������һ���������£�����϶���ұ�����������ұ���ת����
C. ����ƽ���ƶ��ĽǶȷ�������ҵ��������ϩѡ���ѹ�������ں�������
D. �����ұ�����Ӧ�ﵽƽ������У���������ƽ����Է���������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ����
A. �ø�����ر���Һ�ζ����2MnO4����16H����5C2O42��===2Mn2����10CO2����8H2O
B. Cl2��FeBr2��Һ��Ӧ����n(Cl2):n(FeBr2)=1:1ʱ��2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
C. ���Ե缫���MgCl2��Һ��2Cl+2H2O![]() Cl2��+2OH-+ H2��
Cl2��+2OH-+ H2��
D. ��NaHSO4��Һ�е���Ba(OH)2��Һ�����ԣ�H++SO42-+Ba2++OH- ===BaSO4��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���A ��ũҩ�����е�һ���м��壬�ṹ��ʽ����ͼ��ʾ��������������ȷ����
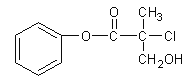
A��1mol A�������4mol H2�����ӳɷ�Ӧ
B���л���A������һ����������HBr������Ӧ
C���л���A��Ũ�����ϼ��ȣ����Է�����ȥ��Ӧ
D��1mol A��������NaOH��Һ��Ӧ������������2mol NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ۺϴ�����Ӧ�ü����ǿ�����Ա����Ҫ�о����⣬CO��SO2��NO2����Ҫ�Ĵ�����Ⱦ���塣
��1���������CO����ȡ������Դ������(CH3OCH3)��ԭ�ϡ�
��֪��CO(g)+H2O(g) CO2(g)+H2(g) ��H1= -41.0 kJ/mol
��CO2(g)+3H2(g) CH3OH(g)+H2O(g) ��H2= -49.0 kJ/mol
��CH3OCH3(g)+H2O(g) 2CH3OH(g) ��H3= +23.5 kJ/mol
��Ӧ2CO(g)+4H2(g) CH3OCH3(g)+H2O(g)����H=________.
��2����֪973 Kʱ,SO2��NO2��Ӧ����SO3��NO����������徭�����������SO3�������Ʊ����ᡣ
��973 Kʱ�����:NO2(g) NO(g)+ ![]() O2(g) K1=0.018��SO2(g) +
O2(g) K1=0.018��SO2(g) + ![]() O2(g) SO3(g) K2=20����ӦSO2(g)+NO2(g) SO3(g)+NO(g)��K3=________
O2(g) SO3(g) K2=20����ӦSO2(g)+NO2(g) SO3(g)+NO(g)��K3=________
��973Kʱ,���ݻ�Ϊ2 L���ܱ������г���SO2��NO2 ��0.2mol��ƽ��ʱSO2��ת����Ϊ______��
�ۺ�ѹ�£�SO2�ķ�ѹPSO2���¶ȵı仯��ͼ��ʾ:
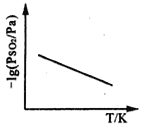
���¶�����ʱ,SO2(g)+NO2(g) SO3(g)+NO(g)�Ļ�ѧƽ�ⳣ��______(����������������С��)�� �ж�������______________________��
��3������������ȥ����ˮ�е�NO3����
������������ˮ��NO3����Ӧ�����ӷ���ʽΪ4Fe+NO3��+10H+=4Fe2++NH4++3H2O���о����֣���pHƫ�ͽ��ᵼ��NO3����ȥ�����½�����ԭ����______________________��
����ͬ�����£���������ȥ����ͬˮ���е�NO3���������нϴ���졣�±������������������ԭ�������________________________________________������0~20min����NO3����ʾ��ƽ����Ӧ����Ϊ______________mol��L��l��min��1��
��Ӧʱ��/min | 0 | 10 | 20 | 30 | 40 | |
�� | c(NO3��)/10��4 mol��L��1 | 8 | 3.2 | 1.6 | 0.8 | 0.64 |
�� | c(NO3��)/10��4 mol��L��1 (������Cu2+) | 8 | 0.48 | 0.32 | 0.32 | 0.32 |
��4����NaOH��Һ����SO2�ɵ�NaHSO3��Һ,��NaHSO3��Һ�и�����Ũ�ȵĹ�ϵ�����з�������������___��(��֪������K1(H2SO3)=1.5��10��2��,K2(H2SO3)=1.02��10��7)
A��c(Na+)+c(H+)=c(HSO3��) +2c(SO32��) +c(OH��)
B��c(Na+) =c(HSO3��) +c(SO32��) +c(H2SO3)
C��c(Na+) >c(SO32��) >c(HSO3��) > (OH��)c>c(H+)
D��c(H+) +c(SO32��) =c(OH��) +c(H2SO3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧҪ�����о������ӵĽṹ��Ϊ��Ŀ��һ��̽���������������¼�����㲹ȫ��ȱ���ݡ�
��1�������Ʋ⣺�����ݱ��Ŀ�����ʽ________���Ʋⱽ�����������ֲ�ͬ��̼̼������________��________���������ʹ��ɫ��________��Һ��ɫ��
��2��ʵ����֤����ȡ������������Һ�����Թ��У�Ȼ����뱽�����������_____________________��
��3��ʵ����ۣ������������Ʋ���________(������ȷ������������)�ġ�
��4����ѯ���ϣ��������й����ϣ����ֱ�����������̼ԭ��֮��ļ�________(������ͬ��������ͬ��)����һ������ļ����������е�����̼ԭ�Ӻ�������ԭ��________(������������������)ͬһ��ƽ���ϣ�Ӧ����________��ʾ�����ӵĽṹ��������
��5���������⣺��������������ˮ��ʱ�������������ʹ��ˮ��ɫ�����Ǹ�ͬѧ��Ϊ��������������ͬ�����Ľ�����____��Ϊʲô��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̼���ơ�̼�����ơ��������ơ��Ȼ����ͱ����������ʵ���Һ������֮������ͼ��ʾ ת����ϵ��ͼ��ÿ�������˵����ʾ����Է�����Ӧ�� �����жϺ�������

A. Xһ����̼��������Һ B. Y������Ϊ�Ȼ�����Һ
C. Z����Ϊ����������Һ D. M��N�ض���Ϊ���ӡ�����������Һ�е�ijһ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��һ����Ҫ�Ļ���ԭ�ϣ��������ʼ�ת����ϵ����ͼ��

��ش�
��1��D�й����ŵ�������_____________��
��2��A��B�ķ�Ӧ������________________��
A��ȡ����ӦB���ӳɷ�Ӧ C��������Ӧ D����ԭ��Ӧ
��3��д��A��C��Ӧ�Ļ�ѧ����ʽ_______________________��
��4��ij��X��B��ͬϵ�������̼�����������Ϊ36:7����ѧ������������ơ���ȡ��֧�Թܣ��ֱ����������ˮ��ʵ��������������£�
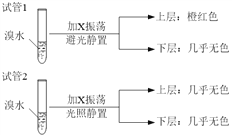
�й�X��˵����ȷ����_______________________��
A����ͬ�����£�X���ܶȱ�ˮС
B��X��ͬ���칹�干��6��
C��X����Br2�����ӳɷ�Ӧʹ��ˮ��ɫ
D��������Թ�2�е��л������ϲ㻹���²㣬��ͨ����ˮȷ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com