
【题目】工业上用氟硅酸钠(Na2SiF6)生产冰晶石(Na3AlF6)的工艺流程如下:

(1)分解过程发生的反应为:Na2SiF6+4NH3H2O═2NaF+4NH4F+X↓+2H2O。工业上把滤渣X叫白炭黑,其化学式为______________________。
(2)分解时白炭黑产率和冰晶石纯度与pH的关系如图所示,分解时需要控制溶液的pH=________;能提高其分解速率的措施有___________ (填标号)。

A.快速搅拌B.加热混合液至100℃C.降低氨水浓度
(3)流程中可循环利用的物质为_________(写化学式);冰晶石在电解冶炼铝中的作用是降低氧化铝的熔融温度、________________________和提髙产率。
(4)水浴加热过程中生成冰晶石的化学方程式为_____________________________。
【答案】 SiO2 8.5 A NH3(或NH3·H2O) 减少能源消耗(或降低生产成本) 2NaF+4NH4F+NaAlO2 ![]() NaAlF6↓+4 NH3↑+2 H2O
NaAlF6↓+4 NH3↑+2 H2O
【解析】(1)分解过程发生的反应为:Na2SiF6+4NH3H2O=2NaF+4NH4F+X↓+2H2O,化学反应前后原子守恒,则X为SiO2;(2)从图可知,pH为8.5时,冰晶石中白炭黑的含量较低,冰晶石纯度较高;能提高其分解速率的措施有A.快速搅拌可以加快反应速率,A正确;B.加热混合液至100℃,氨水受热分解,反应物浓度小,化学反应速率减慢,B错误;C.降低氨水浓度,化学反应速率减慢,C错误;答案选A;(3)第二次过滤所得滤液为氨气水溶液,可循环使用;冰晶石降低氧化铝的熔融温度,减少能源消耗(或降低生产成本);(4)根据以上分析可知水浴加热过程中生成冰晶石的化学方程式为2NaF+4NH4F+NaAlO2 ![]() NaAlF6↓+4 NH3↑+2H2O。
NaAlF6↓+4 NH3↑+2H2O。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某芳香烃的分子式为C10H14 ,不能使溴水褪色,但可使酸性KMnO4溶液褪色,分子结构中含有两个烷基,则此烃的结构共有( )
A. 6种 B. 7种 C. 8种 D. 9种
查看答案和解析>>
科目:高中化学 来源: 题型:
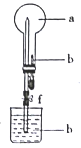
【题目】在下图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。下表中所列出的 a、b物质不符合要求的是
a(干燥气体) | b(液体) | |
A | NO2 | 水 |
B | SO2 | 饱和酸性高锰酸钾溶液 |
C | Cl2 | 饱和NaOH馆液 |
D | NH3 | 2 mol/L.盐酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池的电池反应为:Fe+2Fe3+===3Fe2+,与此电池反应不符的原电池是
A. 铜片、铁片、FeCl3 溶液组成的原电池
B. 石墨、铁片、Fe(NO3)3 溶液组成的原电池
C. 铁片、锌片、Fe2(SO4)3 溶液组成的原电池
D. 铜片、铁片、Fe(NO3)3 溶液组成的原电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加工橘子罐头,采用酸碱处理脱去中果皮(橘络),会产生严重污染。目前使用酶解法去除橘络,可减少污染。下列生长在特定环境中的4类微生物,不能大量产生所用酶的有( )
A. 生长在麦麸上的黑曲霉 B. 生长在酸奶中的乳酸菌
C. 生长在棉籽壳上的平菇 D. 生长在木屑上的木霉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池是利用燃料(如CO、H2、CH4等)与氧气反应,将反应产生的化学能转变为电能的装置,通常用氢氧化钾作为电解质溶液.完成下列关于甲烷(CH4)燃料电池的填空:
(1)甲烷与氧气反应的化学方程式为:
(2)已知燃料电池的总反应式为CH4+2O2+2KOH=K2CO3+3H2O,电池中有一极的电极反应为CH4+10OH﹣﹣8e﹣=CO32﹣+7H2O,这个电极是燃料电池的(填“正极”或“负极”),另一个电极上的电极反应式为:
(3)随着电池不断放电,电解质溶液的碱性(填“增大”、“减小”或“不变”)
(4)通常情况下,甲烷燃料电池的能量利用率(填“大于”、“小于”或“等于”)甲烷燃烧的能量利用率.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的氢氧化物是两性氢氧化物;E的阳离子与A的阴离子核外电子层结构相同.请回答下列问题: 
(1)A在元素周期表中的位置 .
B的最高价氧化物化学式为 .
写出C元素气态氢化物的电子式 .
(2)D的单质与水反应的化学方程式为 .
(3)五种元素中原子半径最小的是(填元素符号),这些元素的最高价氧化物的对应水化物中酸性最强.
(4)C的一种氧化物是常见的大气污染物.为防止大气污染,某化工厂用NaOH溶液、石灰和O2处理含C的上述氧化物的尾气,使其转化为石膏(CaSO42H2O).假设在转化过程中C元素不损失,每天处理1120m3(标准状况下)含2%(体积分数)上述氧化物的尾气,理论上可以得到多少千克石膏(请写出计算过程).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】—块ll.0g的铁铝合金,加入一定量的稀硫酸后合金完全溶解,然后加H2O2至溶液中无Fe2+存在,加热除去多余的H2O2,当加入200mL6 mol·L-1 NaOH溶液时沉淀量最多, 且所得沉淀质量为26.3g,下列说法不正确的是
A. 该合金中铁的质量为5.6g
B. 所加的稀硫酸中含0.6mol H2SO4
C. 合金与稀硫酸反应共生成0.45molH2
D. 该合金与足量氢氧化钠反应,转移的电子数为0.6NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com